Salicilato de metilo: estructura, propiedades, usos, síntesis
¿Qué es el salicilato de metilo?
El salicilato de metilo es una sustancia química, de naturaleza orgánica, considerada como el compuesto con mayor toxicidad entre los salicilatos conocidos, a pesar de su apariencia incolora y de olor agradable con un ligero toque dulce. Esta especie es mejor conocida por el nombre aceite de gaulteria. Su fórmula es C8H8O3.
Se encuentra en estado líquido en condiciones estándar de temperatura y presión (25 °C y 1 atm), constituyendo un éster orgánico que se origina de manera natural por una gran variedad de plantas. A partir de la observación y el estudio de su producción en la naturaleza, se pudo proceder a la síntesis de salicilato de metilo.
Esta síntesis se realizó por medio de una reacción química entre el éster procedente del ácido salicílico y su combinación con metanol. De esta manera, este compuesto forma parte de la salvia, el vino blanco, y frutas como la ciruela y la manzana, entre otras halladas de manera natural.
De forma sintética, el salicilato de metilo se utiliza en la producción de agentes aromatizantes, así como en ciertas comidas y bebidas.
Estructura química
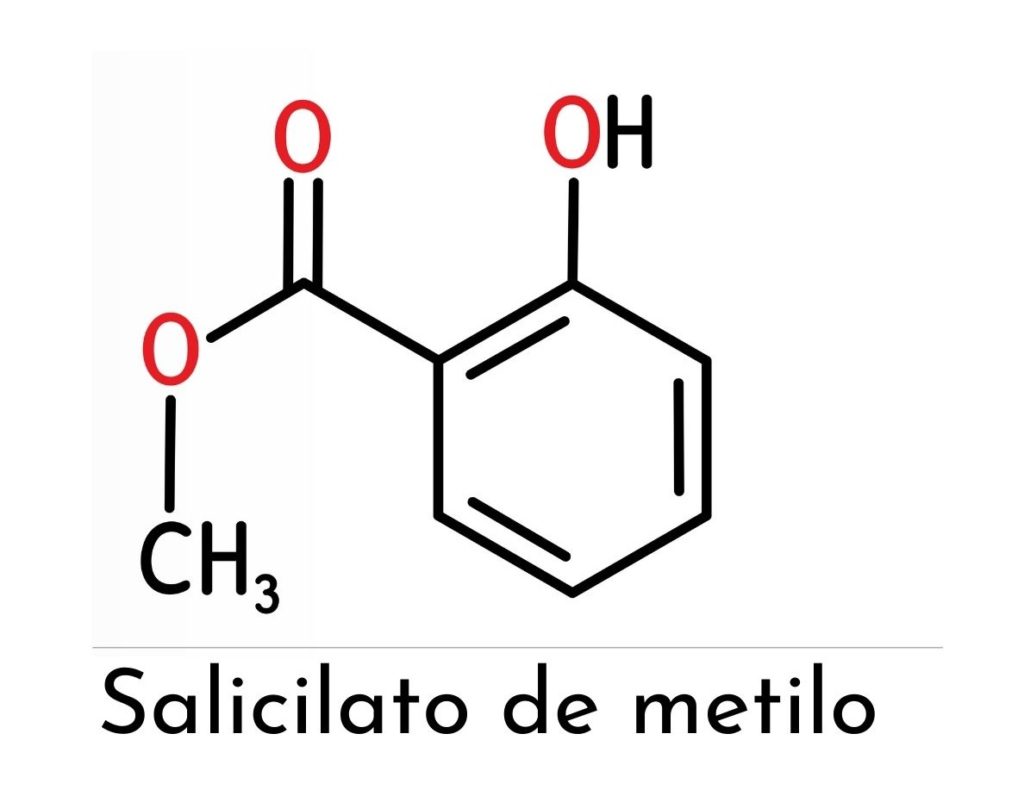
La estructura química del salicilato de metilo está constituida por dos grupos funcionales principales (un éster y un fenol unido a este), tal como se muestra en la imagen superior.
Se observa que está constituido por un anillo bencénico (el cual representa una influencia directa sobre la reactividad y estabilidad del compuesto), procedente del ácido salicílico del cual se deriva.
Para nombrarlos de manera separada, se puede decir que están unidos en posición orto (1,2) un grupo hidroxilo y un éster metílico al anillo antes mencionado.
Entonces, como el grupo OH está unido al anillo bencénico, se forma un fenol, pero el grupo que tiene mayor “jerarquía” en esta molécula es el éster, otorgándole una estructura particular a este compuesto y, por lo tanto, características bastante específicas.
De este modo, su nombre químico se presenta como el 2-hidroxibenzoato de metilo, otorgado por la IUPAC aunque empleado con menor frecuencia al referirse a este compuesto.
Propiedades del salicilato de metilo
– Es una especie química que pertenece al grupo de los salicilatos, los cuales son productos de origen natural procedentes del metabolismo de algunos organismos vegetales.
– Se tiene conocimiento de las propiedades terapéuticas de los salicilatos en tratamientos médicos.
– Este compuesto está presente en ciertas bebidas como el vino blanco, té, salvia y ciertas frutas como la papaya o la cereza.
– Se encuentra de manera natural en las hojas de una gran cantidad de plantas, especialmente en ciertas familias.
– Pertenece al grupo de los ésteres orgánicos que se pueden sintetizar en el laboratorio.
– Se obtiene en estado líquido, cuya densidad es de aproximadamente 1,174 g/ml en condiciones estándar de presión y temperatura (1 atm y 25 °C).
– Forma una fase líquida incolora, amarillenta o rojiza, considerada como soluble en agua (que es un solvente inorgánico) y en otros solventes de tipo orgánico.
– Su punto de ebullición es de aproximadamente 222 °C, manifestando su descomposición térmica alrededor de los 340 a 350 °C.
– Presenta múltiples aplicaciones, que van desde agente aromatizante en la industria de las golosinas hasta analgésico y otros productos en la industria farmacéutica.
– Su fórmula molecular se representa como C8H8O3 y posee una masa molar de 152,15 g/mol.
Usos/aplicaciones
Debido a sus características estructurales, siendo un éster metílico procedente del ácido salicílico, el salicilato de metilo posee una gran cantidad de usos en distintas áreas.
Uno de los usos principales (y el más conocido) de esta sustancia es el de agente aromatizante en diferentes productos: desde la industria cosmética como fragancia hasta la industria alimenticia como saborizante en golosinas (goma de mascar, caramelos, helados, entre otros).
También se utiliza en la industria cosmética como agente de calentamiento y para masajes musculares en aplicaciones deportivas. En este último caso actúa como rubefaciente; es decir, ocasiona el enrojecimiento superficial de la piel y las membranas de naturaleza mucosa al entrar en contacto con estas.
Del mismo modo, se emplea en crema para uso tópico, por sus propiedades analgésicas y antiinflamatorias en tratamientos para condiciones reumáticas.
Otra de sus aplicaciones incluye su uso líquido en sesiones de aromaterapia, debido a sus características de aceite esencial.
Además de su utilización como agente de protección contra la radiación ultravioleta en protectores solares, se investigan sus propiedades frente a la luz para aplicaciones tecnológicas, tales como la producción de rayos láser o la creación de especies sensibles a almacenar información dentro de las moléculas.
Síntesis del salicilato de metilo
En primer lugar, debe mencionarse que el salicilato de metilo se puede obtener de manera natural a partir de la destilación de las ramas de ciertas plantas, como las de la gaulteria (Gaultheria procumbens) o el abedul dulce (Betula lenta).
Esta sustancia se extrajo y aisló por primera vez en el año 1843 gracias al científico de origen francés llamado Auguste Cahours; a partir de la gaulteria, en la actualidad se obtiene a través de síntesis en laboratorios e incluso a nivel comercial.
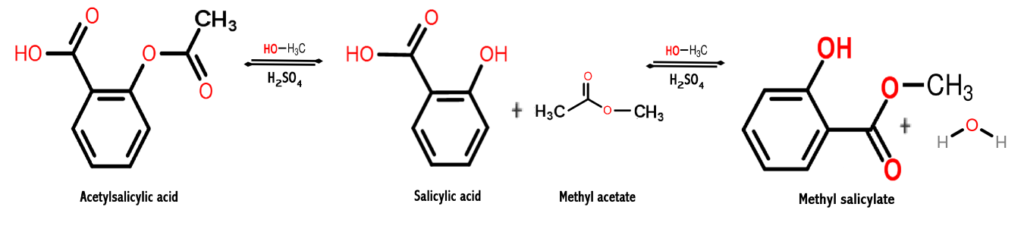
La reacción que se da para obtener este compuesto químico es un proceso denominado esterificación, en el cual se obtiene un éster mediante la reacción entre un alcohol y un ácido carboxílico. En este caso se da entre el metanol y el ácido salicílico, como se muestra a continuación:
CH3OH + C7H6O3 → C8H8O3 + H2O
Cabe destacar que la parte de la molécula de ácido salicílico que se esterifica con el grupo hidroxilo (OH) del alcohol es el grupo carboxilo (COOH).
Entonces, lo que ocurre entre estas dos especies químicas es una reacción de condensación, debido a que se remueve la molécula de agua presente entre los reactantes mientras que las demás especies reactantes son condensadas con el fin de obtener el salicilato de metilo.
En la siguiente imagen se observa la síntesis de salicilato de metilo a partir de ácido salicílico, donde se muestran dos reacciones sucesivas.