Ácido húmico: estructura, propiedades, obtención, usos
Ácido húmico es el nombre genérico de una familia de compuestos orgánicos que forman parte de las sustancias húmicas. Poseen diversos grupos funcionales, entre los que se pueden mencionar los carboxílicos, los fenólicos, los anillos tipo azúcares, las quinonas y los derivados de aminoácidos.
Las sustancias húmicas, de las cuales forman parte los ácidos húmicos, están distribuidas en suelos, aguas naturales y sedimentos, pues son el resultado de la descomposición de residuos vegetales, animales y naturales.

Los ácidos húmicos forman parte del humus y tienen la capacidad de mejorar el crecimiento de las plantas y su nutrición, pues permiten retener los nutrientes por más tiempo en el suelo para que estén disponibles para las plantas.
Son compuestos anfifílicos, esto es, poseen partes que son afines al agua y porciones que rechazan el agua, todo dentro de la misma molécula.
Por sus grupos –OH y –COOH pueden formar complejos con iones de metales o cationes.
Gracias a sus cadenas hidrocarbonadas o porciones aromáticas pueden solubilizar y encerrar dentro de sí moléculas aromáticas policíclicas que son tóxicas. Además, poseen un uso potencial en medicina contra el cáncer y en la preparación de productos farmacéuticos más efectivos.
Índice del artículo
Los ácidos húmicos contienen diferentes grupos funcionales cuyas cantidades dependen del origen geográfico del ácido húmico, edad, condiciones ambientales y biológicas y clima en el cual se produjo la molécula. Por esta razón, su caracterización precisa se ha hecho difícil.
Sus principales grupos funcionales son fenólico, carboxílico, enólico, quinona, éter, azúcares y péptidos.
Los grupos funcionales que le dan sus principales características son los grupos fenólicos, carboxílicos y quinonas.
La gran estructura de un ácido húmico se compone de porciones hidrofílicas formadas por grupos –OH y porciones hidrofóbicas constituidas por cadenas alifáticas y anillos aromáticos.
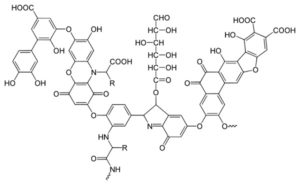
– Ácidos húmicos.
– HA o HAs (siglas del inglés Humic Acids).
Sólidos amorfos.
Sus pesos moleculares van desde 2,0 hasta 1300 kDa.
Un Da o Dalton vale 1,66 x 10-24 gramos.
Los ácidos húmicos son la fracción de las sustancias húmicas que es soluble en medio acuoso alcalino. Son parcialmente solubles en agua. Insolubles en medio ácido.
Su disolución en agua es compleja porque los ácidos húmicos no son un componente individual sino una mezcla de componentes, en donde solo algunos de ellos son solubles en agua.
Su solubilidad puede variar dependiendo de su composición, el pH y la fuerza iónica del solvente.
Las moléculas de los ácidos húmicos poseen generalmente una parte hidrofílica, o afín al agua, y una parte hidrofóbica, que rechaza el agua. Por ello se dice que son anfifílicas.
Debido a su carácter anfifílico, los ácidos húmicos forman, en un medio neutro o ácido, unas estructuras parecidas a las de las micelas, llamadas pseudo-micelas.
Son ácidos débiles, lo que es causado por los grupos fenólicos y carboxílicos.
Los grupos tipo quinona son los responsables de la formación de especies de oxígeno reactivo, pues se reducen a semiquinonas y luego a hidroquinonas que son muy estables.
La presencia de grupos fenólicos y carboxílicos en las moléculas de los ácidos húmicos les confiere la capacidad de mejorar el crecimiento de las plantas y su nutrición. Tales grupos también pueden favorecer la formación de complejos con metales pesados. Y además explican su actividad antiviral y antiinflamatoria.
Por otra parte, la presencia de los grupos quinona, fenol y carboxílico se relaciona con sus capacidades antioxidantes, fungicidas, bactericidas y antimutagéncias o desmutagénicas.
En medio alcalino los grupos carboxílicos y fenólicos sufren la pérdida de protones H+, lo que deja la molécula cargada negativamente en cada uno de esos grupos.
Debido a esto ocurre repulsión de las cargas negativas y la molécula se estira.
Al disminuir el pH, los grupos fenólicos y carboxílicos son nuevamente protonados y cesan los efectos de repulsión, haciendo que la molécula adopte una estructura compacta, parecida a la de las micelas.
En este caso las porciones hidrofóbicas se tratan de situar en el interior de la molécula y las porciones hidrofílicas están en contacto con el medio acuoso. Se dice que estas estructuras son pseudo-micelas.
Por este comportamiento se afirma que los ácidos húmicos tienen características de detergencia.
Además, forman agregados intramoleculares (dentro de su propia molécula), seguidos de agregación intermolecular (entre diferentes moléculas) y precipitación.
Los ácidos húmicos pueden solubilizar hidrocarburos aromáticos policíclicos los cuales son tóxicos y carcinogénicos y son relativamente insolubles en agua.
Estos hidrocarburos son solubilizados en el corazón hidrofóbico de las pseudo-micelas de los ácidos húmicos.
Los ácidos húmicos interaccionan con los iones de metales en medio alcalino donde los cationes o iones positivos actúan neutralizando las cargas negativas de la molécula de ácido húmico.
A mayor carga del catión, mayor es su efectividad de formar pseudo-micelas. Los cationes se ubican en lugares termodinámicamente preferidos en la estructura.
Este proceso genera complejos ácidos húmicos-metal que adquieren una forma esférica.
Esta interacción depende del metal y del origen, peso molecular y concentración del ácido húmico.
Los ácidos húmicos pueden obtenerse de la materia orgánica del suelo. Sin embargo, las estructuras de las diversas moléculas de ácidos húmicos varían de acuerdo con la ubicación del suelo, su edad y condiciones climáticas.
Hay diversos métodos de obtención. A continuación se describe uno de estos.
Se trata el suelo con una solución acuosa de NaOH 0,5 N (0,5 equivalentes por litro) bajo atmósfera de nitrógeno durante 24 horas a temperatura ambiente. Se filtra el conjunto.
El extracto alcalino se acidifica con HCl 2 N hasta un pH 2 y se deja reposar durante 24 horas, a temperatura ambiente. El material coagulado (ácidos húmicos) se separa del sobrenadante por centrifugación.
La utilización de los ácidos húmicos en la agricultura es conocida prácticamente desde los comienzos de la actividad agrícola debido a que forman parte del humus.

Los ácidos húmicos mejoran el crecimiento y nutrición de las plantas. Además actúan como bactericidas del suelo y fungicidas protegiendo las plantas. Los ácidos húmicos inhiben los hongos fitopatógenos y se ha correlacionado algunos de sus grupos funcionales con esta actividad.

La presencia de azufre (S) y grupos carbonilo C=O en la molécula de ácido húmico favorecen la actividad fungistática. Por el contrario, un alto contenido de oxígeno, grupos C-O aromáticos y ciertos átomos de carbono pertenecientes a azúcares inhiben la fuerza fungistática del ácido húmico.
Recientemente (2019), se ha estudiado el efecto de la aplicación de fertilizantes nitrogenados de liberación lenta en la estabilización de los ácidos húmicos presentes en los suelos y su influencia sobre las cosechas.
Se encontró que la urea recubierta de biocarbono mejora la estructura y estabilidad de los ácidos húmicos presentes en el suelo, favoreciendo la retención de nitrógeno y carbono por el suelo y mejorando el rendimiento de las cosechas.
Por su capacidad de formar pseudo-micelas en medio neutro o ácido se ha explorado por muchos años su utilidad en la remoción de contaminantes de aguas residuales y de suelos.
Los metales son unos de los contaminantes que pueden ser removidos por los ácidos húmicos.
Algunos estudios demuestran que la eficiencia de sorción de metales por parte de los ácidos húmicos en solución acuosa tiende a aumentar al subir el pH y la concentración de ácido húmico y al disminuir la concentración del metal.
También se determinó que los iones metálicos compiten por los sitios activos de la molécula de ácido húmico, que son generalmente los grupos –COOH y –OH fenólicos en este.
Se ha probado su utilidad para aumentar la solubilidad en agua de medicamentos hidrofóbicos.
Se prepararon nanopartículas de plata (Ag) recubiertas de ácidos húmicos, las cuales lograron permanecer estables durante al menos un año.
Estas nanopartículas de plata y ácido húmico, junto con las propiedades antibacteriales de estos últimos, poseen un alto potencial para la preparación de fármacos.
Igualmente se han probado complejos de carbamazepina, una medicina antiepiléptica, con ácidos húmicos para aumentar la solubilidad de esta, y ha resultado que el fármaco se vuelve mucho más soluble y efectivo.
El mismo efecto de mejoramiento de solubilidad y biodisponibilidad se logró con complejos de ácidos húmicos y β-caroteno, un precursor de la vitamina A.
Los ácidos húmicos son fuertes aliados en el tratamiento de varias enfermedades.
Contra algunos virus
Se ha observado actividad antiviral de los ácidos húmicos contra el citomegalovirus y los virus de inmunodeficiencia humana HIV-1 y HIV-2, entre otros.
Las moléculas de los ácidos húmicos pueden inhibir la replicación del virus al unir su carga negativa en medio alcalino con ciertos lugares catiónicos del virus, que son necesarios para que el virus se una a la superficie de la célula.
Contra el cáncer
Se ha encontrado que los ácidos húmicos ejercen propiedades curativas de lesiones cancerígenas. Se atribuye esto a la presencia de quinonas en su estructura.
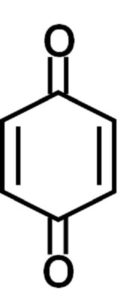
Las quinonas generan especies reactivas de oxígeno las cuales producen estrés oxidativo e inducen la apoptosis de las células cancerígenas a través de la fragmentación de su ADN.
Contra la mutagénesis
Los ácidos húmicos son inhibidores de la mutagénesis dentro de la célula y fuera de esta. La mutagénesis es la alteración estable del material genético de una célula que puede ser transmitida a las células hijas.
Se ha encontrado que la capacidad de inhibir la mutagénesis varía con la composición de los ácidos húmicos y su concentración.
Por otra parte, ejercen efecto desmutagénico sobre sustancias mutagénicas como el benzopireno (hidrocarburo poliaromático presente en algunos alimentos), el 2-nitrofluoreno (hidrocarburo poliaromático producto de la combustión) y el 2-aminoantraceno.
El mecanismo de este efecto reside en la adsorción del mutágeno, por lo cual los ácidos húmicos con estructuras más grandes son los más efectivos. El mutágeno es adsorbido por el ácido húmico y pierde su actividad mutagénica.
Se estima que esto puede ser importante para la protección contra la carcinogénesis.
Debido a su habilidad para absorber rayos UV y visibles, los ácidos húmicos han sido propuestos para ser utilizados en bloqueadores solares, cremas antienvejecimiento y productos de cuidado de la piel.
También se pueden emplear como conservantes de productos cosméticos.
Por sus propiedades antioxidantes se ha sugerido su uso como conservantes de alimentos y como suplementos nutricionales.
- Gomes de Melo, B.A. et al. (2016). Humic acids: Structural properties and multiple functionalities for novel technological developments. Materials Science and Engineering C 62 (2016) 967-974. Recuperado de sciencedirect.com.
- Wei, S. et al. (2018). Fungistatic Activity of Multiorigin Humic Acids in Relation to Their Chemical Structure. Journal of Agricultural and Food Chemistry 2018, 66, 28, 7514-7521. Recuperado de pubs.acs.org.
- Kerndorff, H. and Schnitzer, M. (1980). Sorption of metals on humic acid. Geochimica et Cosmochimica Acta Vol 44, pp.1701-1708. Recuperado de sciencedirect.com.
- Sato, T. et al. (1987). Mechanism of the desmutagenic effect of humic acid. Mutation Research, 176 (1987) 199-204. Recuperado de sciencedirect.com.
- Cheng, M.-L. et al. (2003). Humic Acid Induces Oxidative DNA damage, Growth Retardation, and Apoptosis in Human Primary Fibroblasts. Exp Biol Med (Maywood) 2003 Apr; 228(4):413-23. Recuperado de ncbi.nlm.nih.gov.
- Li, M. et al. (2019). Organic carbon sequestration in soil humic substances as affected by application of different nitrogen fertilizers in a vegetable-rotation cropping system. Journal of Agricultural and Food Chemistry, 2019, 67, 11, 3106-3113. Recuperado de pubs.acs.org.
