Uretano: estructura, propiedades, obtención, usos
El uretano es un término de química orgánica que se utiliza, normalmente, para referirse al carbamato de etilo, o al grupo funcional carbamato. Por lo tanto, el carbamato de etilo suele considerarse como el uretano por defecto, el cual es un compuesto muy soluble en agua, utilizado como solvente en reacciones de síntesis orgánica.
El carbamato de etilo se emplea asimismo como pesticida y fungicida. Hasta 1943 se había utilizado como antineoplásico. Pero al descubrirse su acción cancerígena en animales de experimentación, se desechó esta aplicación.
El uretano es producido industrialmente por la reacción en caliente de la urea con el etanol. Se trata de un compuesto volátil e inflamable que presenta una densidad de vapor tres veces superior al del aire. Además, el uretano experimenta sublimación.
El poliuretano, por otra parte, es un polímero cuya producción industrial se encuentra orientada a la obtención de espumas, utilizadas en muebles y como aislantes en neveras. A pesar de su nombre, el poliuretano no es un polímero del uretano en sí mismo, sino que está formado por unidades orgánicas distintas.
El uretano, bajo la forma de carbamato (H2NCOO–), solamente sirve de puente de unión entre las unidades química que constituyen el poliuretano.
Índice del artículo
- 1 Estructura del uretano
- 2 Propiedades del uretano
- 2.1 Nombres
- 2.2 Fórmula química
- 2.3 Masa molar
- 2.4 Apariencia física
- 2.5 Sabor
- 2.6 Olor
- 2.7 Densidad
- 2.8 Punto de fusión
- 2.9 Punto de ebullición
- 2.10 Solubilidad en agua
- 2.11 Solubilidad en otros solventes
- 2.12 Densidad de vapor
- 2.13 Presión de vapor
- 2.14 Coeficiente de partición octanol/agua
- 2.15 Punto de ignición
- 2.16 Índice de refracción
- 2.17 Sublimación
- 2.18 Perfil de reactividad
- 3 Obtención
- 4 Toxicidad
- 5 Usos
- 6 Referencias
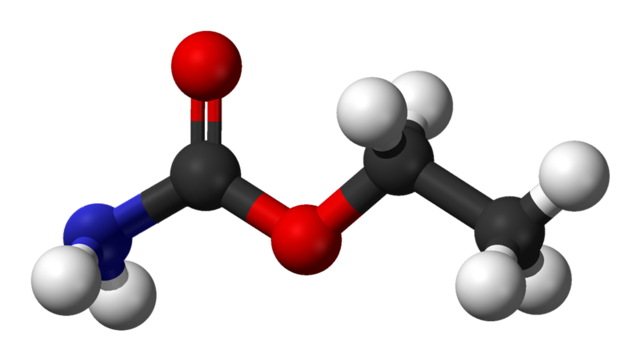
En la primera imagen tenemos la estructura molecular del uretano. Al lado izquierdo tenemos al grupo carbamato: R2NCOO-, con sus grupos alquílicos R sustituidos por H, y el segmento COO- enlazado al sustituyente etilo. Como se aprecia, es una molécula simple, la cual no ofrece por sí sola muchas opciones de polimerización.
-Uretano
-Carbamato de etilo (nombre IUPAC)
-Ester etílico de ácido carbámico
-Etiluretano
C3H7NO2 o NH2COOC2H5
89.094 g/mol
Cristales blancos o incoloros. Polvo blanco de naturaleza granular.
Sabor salino refrescante
Inodoro
1.056 g/cm3
46 a 50 ºC
182 a 185 ºC
4.8·105 mg/L a 15º C. Es muy soluble, ya que es una molecular bastante polar.
1 gramo de uretano se disuelve por separado en: 0.8 mL de alcohol, 1.5 mL de éter, 0.9 mL de cloroformo, 2.5 mL de glicerol, y 32 mL de aceite de oliva.
3.07 en relación al aire como unidad.
3 Pa a 20 ºC.
Log P = – 0,15
92 ºC
1.4144 a 51 ºC
Sublima rápidamente a una temperatura de 103 ºC y a una presión de 54 mm de Hg.
El uretano es incompatible con los álcalis, ácidos, hidratos de coral, alcanfor, mentol y timol. También es incompatible con antipirina y salol. Reacciona con el pentacloruro de fósforo para producir un explosivo.
El uretano es producido por la reacción, en caliente, de la urea con el alcohol etílico:
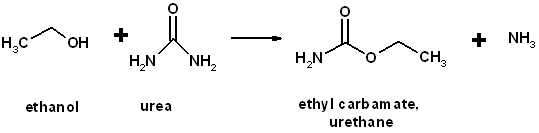
El uretano asimismo es producido por la reacción del cloroformato de etilo con el amoníaco.
El uretano presente en algunas bebidas fermentadas proviene de la reacción de la urea, originada por el metabolismo del aminoácido arginina y liberada por las levaduras, con el alcohol etílico. Entonces, el uretano es un producto lateral de la fermentación de las levaduras de la glucosa presente en las frutas.
La reacción de producción del uretano en las bebidas alcohólicas es espontánea, aunque su formación se ve favorecida por la presencia de una luz con una longitud de onda comprendida entre 375 y 475 nm.
Los productores de bebidas alcohólicas hacen una determinación de la presencia de uretano, procediendo a descartar los lotes de bebidas que presenten niveles superiores a lo permitido, ya que el uretano es un agente cancerígeno.
Además de ser demostrada la acción cancerígena del uretano en animales de experimentación, ha sido posible poner en evidencia numerosos efectos tóxicos sobre los seres humanos. Es nocivo por inhalación, absorción cutánea o por ingestión.
El uretano produce ardor de la garganta, diarrea acuosa o sanguinolenta, dolor abdominal, disminución de la formación y excreción de orina, hipotensión arterial, colapso cardiovascular, delirio, convulsiones, debilidad muscular con insuficiencia respiratoria, y finalmente depresión del sistema nervioso y de la médula ósea.
Anteriormente el uretano era usado en el tratamiento de algunos tipos de cánceres, especialmente el de la leucemia crónica y el del mieloma múltiple. En el año 1943 se obtuvo evidencias de que el uretano tenía, por el contrario, una acción cancerígena, por lo que se desechó este uso.
Asimismo, se usaba como analgésico, aplicación que también se abandonó. Sin embargo, en el Japón se continuó su uso para aliviar los dolores postoperatorios hasta el año 1975.
Actualmente se utiliza el uretano como anestésico en animales utilizados en actividades experimentales, hallándose en algunos casos una acción anestésica que se prolonga por más de 24 horas.
El uretano formaba parte, junto con la sulfonamida, de una solución esclerosante usada en el tratamiento de las venas varicosas.

Los poliuretanos son polímeros que tienen como monómeros usuales al diol y el diisocianato. Es decir, el poliuretano no es un polímero del uretano (carbamato de etilo), sino de otro compuesto químico referido como uretano: el carbamato (H2NCOO–), el cual sirve de enlace entre las unidades químicas que constituyen el poliuretano.
Se usan como espuma en la fabricación de asientos adaptables a la presión, en paneles de aislamientos de equipos de refrigeración en forma de espuma rígida, como sellos y juntas de espuma microcelular.
También se usan en la fabricación de ruedas y neumáticos de gran dureza, empleados en escaleras mecánicas, carritos para compras en los supermercados, ruedas de patinetas. Además, se utiliza poliuretanos en la fabricación de bujes de suspensión para automóviles.
Se emplean en compuestos para recubrir materiales eléctricos, en revestimientos y selladores de superficie, como base para la colocación de alfombras, y como piezas de plástico duro. Asimismo, se utilizan en la elaboración de piezas de vestir, tales como el recubrimiento de los sostenes.
El uretano se utiliza en la producción de aminorresinas. Estas son utilizadas como sustancias adhesivas en la fabricación de aglomerados de madera y contraenchapados, usados en la construcción de viviendas y en la fabricación de muebles.
El uretano se utiliza como solvente en reacciones de síntesis orgánica. También se emplea como fungicida y pesticida, así como también en la industria textil para la elaboración de productos que intervienen en el prensado permanente.
- Graham Solomons T.W., Craig B. Fryhle. (2011). Organic Chemistry. (10th edition.). Wiley Plus.
- Carey F. (2008). Química Orgánica. (Sexta edición). Mc Graw Hill.
- Morrison y Boyd. (1987). Química orgánica. (Quinta edición). Addison-Wesley Iberoamericana.
- Wikipedia. (2020). List of polyurethane applications. Recuperado de: en.wikipedia.org
- Meg Michelle. (24 de abril de 2017). What is Uretane? Recuperado de: sciencing.com
- Polymer Science Learning Center. (2020). Making Polyurethane. Recuperado de: pslc.ws
