.Ácido esteárico (CH3(CH2)16COOH): estructura, propiedades, usos
El ácido esteárico es un compuesto orgánico sólido cuya fórmula química es CH3(CH2)16COOH. Es un ácido carboxílico que pertenece al grupo de ácidos grasos saturados de cadena larga. Es de color blanco amarillento y posee un olor semejante al del sebo o grasa animal.
Se denomina ácido graso porque está presente en muchas grasas y aceites de animales y vegetales. Forma parte del metabolismo de la mayoría de los seres vivos y se encuentra generalmente en forma de éster de glicerina.

El cacao lo posee en alta proporción, así como el sebo de animales vacunos, la grasa de cerdo y la mantequilla. También se encuentra presente en aceites vegetales como el de maíz. Para obtenerlo se hidroliza la triestearina, esto es, se trata con agua y álcali.
La ingestión de ácido esteárico con los alimentos y su efecto sobre la salud presenta actualmente dudas para los investigadores. Parece ser que posee más efectos dañinos que beneficiosos.
Tiene utilidad en la preparación de fármacos, empaques aislantes del agua, velas de parafina, grasas lubricantes, materiales para moldear figuras, cosméticos, ungüentos, cremas, entre muchas otras aplicaciones.
Índice del artículo
- 1 Estructura
- 2 Nomenclatura
- 3 Propiedades físicas
- 4 Propiedades químicas
- 5 Ubicación en la naturaleza
- 6 Obtención
- 7 Usos
- 8 Referencias
La molécula de ácido esteárico posee una cadena lineal de 18 átomos de carbono en la cual el último átomo de carbono forma parte de un grupo carboxílico –COOH. La cadena carbonada posee solo enlaces simples C-C pues es un ácido graso saturado.
Su fórmula expandida es:
CH3—CH2—CH2—CH2—CH2—CH2—CH2—CH2—CH2—CH2—CH2—CH2—CH2—CH2—CH2—CH2—CH2—COOH
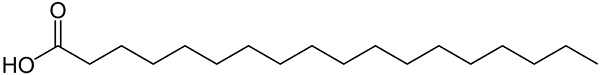
-Ácido esteárico
-Ácido octadecanoico
-Ácido estearofánico
Sólido blanco o ligeramente amarillo, cristalino, con un suave olor parecido al del sebo.
284,5 g/mol
69,3 ºC
383 ºC
196 ºC (método de copa cerrada).
0,9408 g/cm3 a 20 ºC
Insoluble en agua y flota sobre esta. Ligeramente soluble en alcohol. Soluble en éter, acetona y cloroformo.
pKa = 4,75
El ácido esteárico reacciona con hidróxido de sodio (NaOH) y forma estearato de sodio el cual es un jabón. La mayoría de los jabones contiene estearato de sodio.
Se considera al ácido esteárico y al estearato de sodio compuestos generalmente seguros y no tóxicos.
El ácido esteárico es uno de los constituyentes de muchos aceites y grasas de origen vegetal y animal. Generalmente se encuentra en forma de su éster de glicerina.

Está presente en muchas grasas sólidas como el sebo y en menor porcentaje en grasas semisólidas como la manteca de cerdo, la mantequilla y en aceites vegetales como el de maíz y el de algodón.

Es un componente importante de la manteca de cacao (38%) y de karité (árbol africano que produce un tipo de nueces) (38,1%).

Forma parte del metabolismo de muchos seres vivos, como las plantas, mamíferos, seres humanos, crustáceos y algas. Esto significa que, por ejemplo, los seres humanos pueden sintetizarlo en su organismo.
El ácido esteárico, aunque se produce en el organismo humano de forma natural, también se ingiere con los alimentos que lo contienen tanto desde su origen como agregado a su composición.
Hay que resaltar que entre los alimentos procesados industrialmente se han dejado de usar las grasas trans por ser muy dañinas para la salud del ser humano. Estas grasas fueron sustituidas por ácidos grasos saturados, entre estos el ácido esteárico.
Los efectos de esta sustitución aún están bajo estudio. En general los ácidos grasos saturados de cadena larga aumentan los niveles de colesterol de baja densidad, lo que está relacionado con la mortalidad por enfermedad coronaria y del corazón.
Sin embargo, algunos estudios indican que el ácido esteárico disminuye el colesterol de baja densidad lo que sugiere que posee propiedades antiaterogénicas, es decir, que no genera la formación de placas en las arterias, sino que favorece la salud de los vasos sanguíneos.
Por otra parte, otras investigaciones señalan que posee el mayor potencial protrombótico de los ácidos grasos saturados de cadena larga, esto significa que puede promover eventos de taponamiento de los vasos sanguíneos.
Además, se ha determinado que altos niveles de ácido esteárico en la sangre son tóxicos para ciertas células del páncreas, por lo que pueden agravar los síntomas de la diabetes tipo 2. Esta enfermedad es común en personas con mucho sobrepeso.

Es por estas razones que se siguen investigando sus efectos pues no se ha podido aclarar si su acción es favorable o no a la salud del organismo humano.
Puede obtenerse mediante hidrólisis del estearato de glicerina o triestearina C3H5(COOC17H35)3, según la siguiente reacción química:
Triestearina + Hidróxido de sodio → Estearato de sodio + Glicerina
Para producirlo de forma comercial se realiza la hidrogenación de ácidos grasos insaturados de 18 carbonos, como los contenidos en semillas de algodón y otros vegetales.
En otras palabras, se agrega hidrógeno a los dobles enlaces C=C de los ácidos grasos insaturados, quedando como enlaces simples C-C, como se indica a continuación:
–CH=CH– + H2 → –CH2–CH2–
El ácido esteárico es un importante compuesto químico comercial.
Se usa en la industria farmacéutica para la manufactura de diversas medicinas, como supositorios, píldoras recubiertas para afecciones intestinales o para recubrir remedios amargos, entre otros. También es ingrediente de ungüentos o pomadas.
Por ser insoluble en agua se emplea en la industria de los alimentos para empaques aislantes y en la preparación de diversos tipos de materiales a prueba de agua.
También se utiliza como ingrediente en gelatinas, pudines, caramelos y bebidas no alcohólicas porque les confiere cierta viscosidad.
Se usa en la manufactura de velas de estearina y se añade a la cera de parafina en pequeñas cantidades. Por su textura también se emplea en materiales moldeables que sirven para hacer modelos en tres dimensiones.
También sirve en recubrimientos contra la electricidad estática.
Su sal sódica es un jabón y se usa también para el endurecimiento de jabones. Por ser un compuesto inocuo para el ser humano se emplea para hacer cosméticos, como emoliente o agente engrasante de cremas. Sirve también para suavizar plásticos.


El ácido esteárico se utiliza para preparar otros compuestos químicos como ciertos estearatos metálicos, por ejemplo el de aluminio, el cual se emplea para hacer grasas lubricantes al espesar los aceites que las conforman.
Además, es ingrediente de algunos pesticidas, se usa en secadores de barnices y como activador de vulcanización de goma sintética.
El ácido esteárico se ha utilizado con éxito en trampas con luz ultravioleta (UV) para atraer mosquitos transmisores de dengue.
Su olor característico es similar al del ácido láctico que es el que se encuentra en la piel de los seres humanos, por lo que al ser colocado en las trampas atrae a los mosquitos, los cuales quedan atrapados en el dispositivo y mueren.
- Tvrzicka, E. et al. (2011). Fatty acids as biocompounds: Their role in human metabolism, health and disease – A review. Part 1: Classification, dietary sources and biological functions. Biomed Pap Med Fac Univ Palacky Olomouc Czech Repub. 2011 Jun; 155(2):117-130. Recuperado de biomed.upol.cz.
- Tseng, W.-H. et al. (2019). Secondary Freedom Lens Device Design with Stearic Acid for A Low-Glare Mosquito-Trapping System with Ultraviolet Light-Emitting Diodes. Electronics 2019, 8, 624. Recuperado de mdpi.com.
- Van Nostrand’s Encyclopedia of Chemistry (2005). Stearic Acid and Stearates. Recuperado de onlinelibrary.wiley.com.
- U.S. National Library of Medicine. (2019). Stearic acid. Recuperado de: pubchem.ncbi.nlm.nih.gov.
- Lu, H. et al. (2016). Elevated circulating stearic acid leads to a major lipotoxic effect on mouse pancreatic beta cells in hyperlipidaemia via a miR-34a-5p-mediated PERK/p53-dependent pathway. Diabetologia 2016, 59(6):1247-57. Recuperado de ncbi.nlm.nih.gov.
