Biomoléculas inorgánicas: características, funciones, tipos
Las biomoléculas inorgánicas constituyen un amplio grupo de configuraciones moleculares presentes en los seres vivos. Por definición, la estructura básica de las moléculas inorgánicas no está compuesta por un esqueleto carbonado o átomos de carbono enlazados.
Sin embargo, esto no quiere decir que los compuestos inorgánicos deban carecer en su totalidad de carbono para ser incluidos dentro de esta gran categoría, sino que el carbono no debe ser el átomo principal y más abundante de la molécula. Los compuestos inorgánicos que forman parte de los seres vivos son principalmente el agua y una serie de minerales sólidos o en solución.
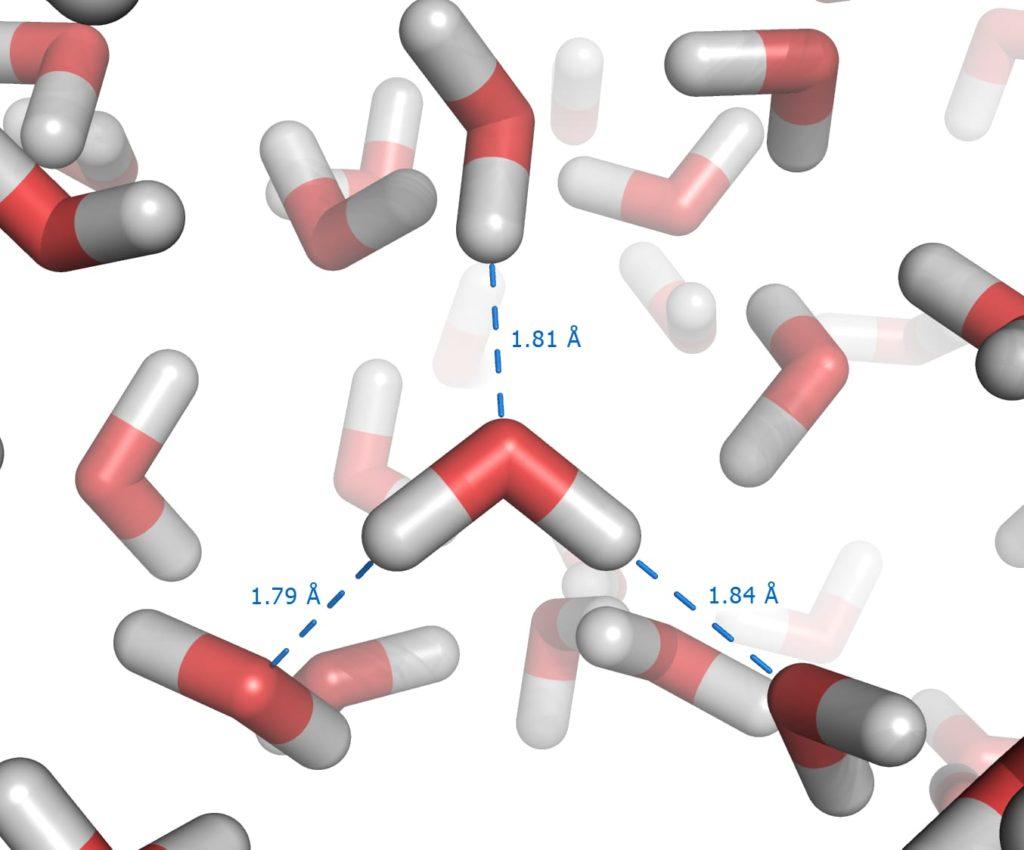
El agua – la biomolécula inorgánica más abundante en los organismos – presenta una serie de características que la convierten en un elemento indispensable para la vida, como un punto de ebullición elevado, constante dieléctrica alta, capacidad para amortiguar los cambios de temperatura y pH, entre otros.
Los iones y gases, por otra parte, están restringidos a funciones muy puntuales dentro de los seres orgánicos, como el impulso nervioso, la coagulación sanguínea, la regulación osmótica, entre otros. Además, son importantes cofactores de ciertas enzimas.
Índice del artículo
- 1 Características
- 2 Clasificación y funciones
- 3 Diferencias entre biomoléculas orgánicas e inorgánicas
- 4 Referencias
La característica distintiva de las moléculas inorgánicas encontradas en la materia viva es la ausencia de ligaduras carbono-hidrógeno.
Estas biomoléculas son relativamente pequeñas e incluyen al agua, gases y una serie de aniones y cationes que participan de manera activa en el metabolismo.
La molécula inorgánica más relevante en la materia viva es, sin lugar a dudas, el agua. Además de esta, otros componentes inorgánicos están presentes y se clasifican en gases, aniones y cationes.
Dentro de los gases tenemos el oxígeno, el dióxido de carbono y el nitrógeno. En los aniones se encuentran los cloruros, los fosfatos, los carbonatos, entre otras. Y en los cationes están el sodio, el potasio, el amonio, el calcio, el magnesio y demás iones positivos.
A continuación describiremos cada uno de estos grupos, con sus características más destacadas y su función dentro de los seres vivos.
El agua es el componente inorgánico más abundante en los seres vivos. Es ampliamente conocido que la vida se desarrolla en un medio acuoso. A pesar de que existen organismos que no viven dentro de un cuerpo de agua, el medio interno de dichos individuos es mayormente hídrico. Los seres vivos se componen entre un 60% y 90% de agua.
La composición de agua en un mismo organismo puede variar, dependiendo del tipo de célula estudiada. Por ejemplo, una célula en un hueso posee, en promedio, un 20% de agua, mientras que una célula del cerebro puede alcanzar fácilmente el 85%.
El agua es tan importante porque la gran mayoría de las reacciones bioquímicas que componen el metabolismo de los individuos tienen lugar en un medio acuoso.
Por ejemplo, la fotosíntesis inicia con la ruptura de los componentes del agua por la acción de la energía luminosa. La respiración celular tiene como resultado la producción de agua al escindir las moléculas de glucosa para lograr la extracción de energía.
Otras rutas metabólicas menos conocidas también implican la producción de agua. La síntesis de los aminoácidos tiene como producto agua.
Propiedades del agua
El agua reúne una serie de características que la convierten en un elemento irreemplazable en el planeta tierra, permitiendo el maravilloso evento de la vida. Entre estas propiedades tenemos:
El agua como disolvente: estructuralmente, el agua se encuentra formada con dos átomos de hidrógeno unidos a un átomo de oxígeno, compartiendo sus electrones mediante un enlace del tipo covalente polar. Así, esta molécula presenta extremos cargados, uno positivo y uno negativo.
Gracias a esta conformación, la sustancia se denomina polar. De este modo, el agua pude disolver sustancias con la misma tendencia polar, ya que las porciones positivas atraen a las negativas de la molécula a disolver y viceversa. A las moléculas que el agua logra disolver se les denomina hidrofílica.
Recordemos que en química, tenemos la regla de que “lo igual disuelve a lo igual”. Esto quiere decir que las sustancias polares se disuelven exclusivamente en otras sustancias que también son polares.
Por ejemplo, los compuestos iónicos, como los carbohidratos y los cloruros, los aminoácidos, los gases y otros compuestos con grupos hidroxilo, logran disolverse fácilmente en agua.
Constante dieléctrica: la elevada constante dieléctrica del líquido vital también es un factor que contribuye a disolver sales inorgánicas en su seno. La constante dieléctrica es el factor por el que se ven separadas dos cargas de signo contrario con respecto al vacío.
Calor específico del agua: amortiguar los cambios violentos de temperatura es una característica indispensable para el desarrollo de la vida. Gracias al elevado calor específico del agua, los cambios de temperatura se estabilizan, creando un ambiente apto para la vida.
Un calor específico elevado se traduce en que una célula puede recibir cantidades importantes de calor y la temperatura de esta no incrementa de manera significativa.
Cohesión: La cohesión es otra propiedad que evita los cambios bruscos de temperatura. Gracias a las cargas opuestas de las moléculas de agua, estas se atraen unas a otras, creando lo que se denomina cohesión.
La cohesión permite que la temperatura de la materia viva no incremente demasiado. La energía calórica rompe los enlaces de hidrógeno entre las moléculas, en vez de acelerar las moléculas individuales.
Control del pH: además de regular y mantener constante la temperatura, el agua es capaz de hacer lo mismo con el pH. Existen ciertas reacciones metabólicas que requieren un pH específico para que puedan llevarse a cabo. De la misma forma, las enzimas también requieren de pH específicos para trabajar con máxima eficiencia.
La regulación del pH ocurre gracias a los grupos hidroxilo (-OH) que son usados junto a los iones hidrógeno (H+). El primero se relaciona con la formación de un medio alcalino, mientras que el segundo contribuye a la formación de un medio ácido.
Punto de ebullición: el punto de ebullición del agua es 100°C. Esta propiedad permite que exista agua en estado líquido a un amplio rango de temperatura, desde los 0°C hasta 100°C.
El alto punto de ebullición se explica por la capacidad de formar cuatro enlaces de hidrógeno por cada molécula de agua. Esta característica también explica los elevados puntos de fusión y calor de vaporización, si los comparamos con otros hidruros, como el NH3, el HF o el H2S.
Esto permite la existencia de algunos organismos extremófilos. Por ejemplo, existen organismos que se desarrollan cerca a los 0°C y se denominan psicrofílos. De la misma manera, los termofílicos se desarrollan cerca de los 70 u 80°C.
Variación de la densidad: la densidad del agua varía de una manera muy particular al cambiar la temperatura del ambiente. El hielo presenta una red cristalina abierta, en contraste con el agua en estado líquido presenta una organización molecular más aleatoria, más apretada y más densa.
Esta propiedad permite que el hielo flote en el agua, actué como aislante término y permita la estabilidad de las grandes masas oceánicas.
Si esto no fuese así, el hielo quedaría hundido en las profundidades de los mares, y la vida, tal y como la conocemos, sería un evento sumamente improbable, ¿cómo podría surgir la vida en grandes masas de hielo?
Papel ecológico del agua
Para finalizar con el tema del agua, es menester mencionar que el líquido vital no solo tiene un papel relevante en el interior de los seres vivos, también moldea el entorno donde estos viven.
El océano es el reservorio más grande de agua en la tierra, el cual se ve afectado por las temperaturas, favoreciendo los procesos de evaporación. Cantidades enormes de agua están en un constante ciclo de evaporación y precipitación de agua, creando lo que se conoce como ciclo del agua.
Si comparamos las extensas funciones del agua en los sistemas biológicos, el papel del resto de las moléculas inorgánicas queda restringido solamente a papeles muy puntuales.
De manera general, los gases transitan por las células en diluciones acuosas. Algunas veces son usados como sustratos de reacciones químicas, y en otros casos son el producto de desecho de la vía metabólica. Los más relevantes son el oxígeno, el dióxido de carbono y el nitrógeno.
El oxígeno es el aceptor final de electrones en las cadenas transportadoras de los organismos con respiración aeróbica. Asimismo, el dióxido de carbono es un producto de desecho en animales y un sustrato para las plantas (para los procesos fotosintéticos).
Al igual que los gases, el papel de los iones en los organismos vivos aparece restringido a eventos muy particulares, pero indispensables para el funcionamiento adecuado de un individuo. Se clasifican dependiendo de su carga en aniones, iones con cargas negativas, y cationes, iones con cargas positivas.
Algunos de estos se requieren solamente en cantidades muy pequeñas, como los componentes metálicos de las enzimas. Otros se necesitan en cantidades más elevadas, como el cloruro de sodio, potasio, magnesio, hierro, yodo, entre otros.
El cuerpo humano está en constante pérdida de estos minerales, por medio de la orina, las heces y el sudor. Estos componentes deben ser ingresados nuevamente al sistema por medio de los alimentos, principalmente frutas, vegetales, y carnes.
Funciones de los iones
Cofactores: los iones pueden actuar como cofactores de reacciones químicas. El ión cloro participa en la hidrólisis del almidón por las amilasas. El potasio y el magnesio son iones indispensables para el funcionamiento de enzimas muy importantes en el metabolismo.
Mantenimiento de la osmolaridad: otra función de gran importancia es el mantenimiento de las condiciones osmóticas óptimas para el desarrollo de los procesos biológicos.
La cantidad de metabolitos disueltos debe estar regulada de manera excepcional, ya que si este sistema falla, la célula podría explotar o podría perder cantidades importantes de agua.
En los humanos, por ejemplo, el sodio y el cloro son elementos importantes que contribuyen en el mantenimiento del equilibrio osmótico. Estos mismos iones también favorecen el equilibrio ácido base.
Potencial de membrana: en los animales, los iones participan de manera activa en la generación del potencial de membrana en la membrana de las células excitables.
Las propiedades eléctricas de las membranas afectan eventos cruciales, como la capacidad de las neuronas para transmitir la información.
En estos casos, la membrana actúa análogamente a un condensador eléctrico, donde se acumulan y almacenan las cargas gracias a las interacciones electrostáticas entre los cationes y los aniones en ambos lados de la membrana.
La distribución asimétrica de los iones en solución en cada uno de los lados de la membrana se traduce en un potencial eléctrico – dependiendo de la permeabilidad de la membrana a los iones presentes. La magnitud del potencial puede ser calculada siguiendo la ecuación de Nernst o la de Goldman.
Estructurales: algunos iones desempeñan funciones estructurales. Por ejemplo, el hidroxiapatito condiciona la microestructura cristalina de los huesos. El calcio y el fósforo, por su parte, es un elemento necesario para la formación de huesos y dientes.
Otras funciones: por último, los iones participan en funciones tan heterogéneas como la coagulación de la sangre (por los iones de calcio), la visión y la contracción de los músculos.
Aproximadamente, un 99% de la composición de los seres vivos incluyen solamente cuatro átomos: hidrógeno, oxígeno, carbono y nitrógeno. Estos átomos funcionan como piezas o bloques, que pueden arreglarse en una amplia gama de configuraciones tridimensionales, formando las moléculas que permiten la vida.
Mientras que los compuestos inorgánicos suelen ser pequeños, simples y poco diversos, los compuestos orgánicos suelen ser más notables y variados.
Aunado a esto, la complejidad de las biomoléculas orgánicas incrementa ya que, además del esqueleto carbonado, poseen grupos funcionales que determinan las características químicas.
No obstante, ambos son igualmente necesarios para el óptimo desarrollo de los seres vivos.
Ahora que describimos la diferencia entre ambos tipos de biomoléculas, es necesario aclarar que usamos estos términos de manera vaga e imprecisa en la vida cotidiana.
Cuando designamos a las frutas y vegetales como “orgánicas” – lo cual es muy popular en la actualidad – no quiere decir que el resto de los productos sean “inorgánicos”. Como la estructura de estos elementos comestibles es un esqueleto carbonado, la definición de orgánica es considerada redundante.
De hecho, el término orgánico surge de la capacidad de organismos para sintetizar dichos compuestos.
- Audesirk, T., Audesirk, G., & Byers, B. E. (2003). Biología: La vida en la Tierra. Pearson educación.
- Aracil, C. B., Rodríguez, M. P., Magraner, J. P., & Pérez, R. S. (2011). Fundamentos de bioquímica. Universitat de València.
- Battaner Arias, E. (2014). Compendio de enzimología. Ediciones Universidad de Salamanca.
- Berg, J. M., Stryer, L., & Tymoczko, J. L. (2007). Bioquímica. Reverté.
- Devlin, T. M. (2004). Bioquímica: libro de texto con aplicaciones clínicas. Reverté.
- Díaz, A. P., & Pena, A. (1988). Bioquímica. Editorial Limusa.
- Macarulla, J. M., & Goñi, F. M. (1994). Bioquímica humana: curso básico. Reverté.
- Macarulla, J. M., & Goñi, F. M. (1993). Biomoléculas: lecciones de bioquímica estructural. Reverté.
- Müller–Esterl, W. (2008). Bioquímica. Fundamentos para medicina y ciencias de la vida. Reverté.
- Teijón, J. M. (2006). Fundamentos de bioquímica estructural. Editorial Tébar.
- Monge-Nájera, J. (2002). Biología general. EUNED.
