Bomba sodio potasio: estructura, función, mecanismo, importancia
La bomba sodio potasio es una estructura proteica incluida en un conjunto más amplio de moléculas presentes en muchas membranas celulares, y que se encargan del transporte activo de iones u otras moléculas pequeñas en contra de sus gradientes de concentración. Utilizan la energía liberada por la hidrólisis del ATP y por eso se denominan genéricamente ATPasas.
La bomba sodio potasio es una Na+/K+ATPasa porque libera la energía contenida en la molécula de ATP para mover el sodio de adentro hacia afuera de la célula, introduciendo, al mismo tiempo, potasio.
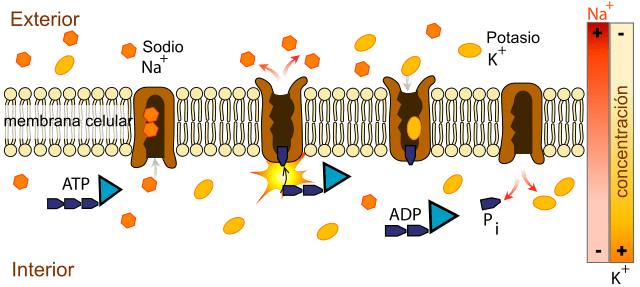
En el interior de la célula el sodio está menos concentrado (12 mEq/L) que en el exterior (142 mEq/L), mientras que potasio está más concentrado afuera (4 mEq/L) que adentro (140 mEq/L).
Las bombas ATPasas se clasifican en tres grandes grupos:
- Bombas iónicas de tipo F y V: son estructuras bastante complejas, pueden estar conformadas por 3 tipos distintos de subunidades transmembranales y hasta 5 polipéptidos asociados en el citosol. Funcionan como transportadores de protones.
- Superfamilia ABC (del inglés ATP-Binding Cassette = casete de unión al ATP): integrada por más de 100 proteínas que pueden funcionar como transportadoras de iones, monosacáridos, polisacáridos, polipéptidos y hasta de otras proteínas.
- Bombas iónicas de la clase P: formadas por al menos una subunidad catalítica alfa transmembranal que tiene un sitio de unión para el ATP y una subunidad β menor. Durante el proceso de transporte la subunidad α se fosforila y de allí su nombre “P”.
Las bomba sodio potasio (Na+/K+ATPasa) pertenece al grupo de las bombas iónicas de la clase P y fue descubierta en 1957 por Jens Skou, un investigador danés, cuando estudiaba el mecanismo de acción de unos anestésicos en los nervios de un cangrejo (Carcinus maenas); trabajo por el cual le fue otorgado el premio nobel en química en 1997.
Índice del artículo
- 1 Estructura de la bomba sodio potasio
- 2 Función de la bomba de potasio
- 3 Mecanismo (proceso)
- 4 Importancia
- 5 Referencias
La bomba sodio potasio se trata de una enzima que desde el punto de vista de su estructura cuaternaria está formada por 2 subunidades proteicas de tipo alfa (α) y dos de tipo beta (β).
Es, por tanto, un tetrámero de tipo α2β2, cuyas subunidades son proteínas integrales de membrana, es decir, atraviesan la bicapa lipídica y tienen dominios tanto intra como extra citosólicos.
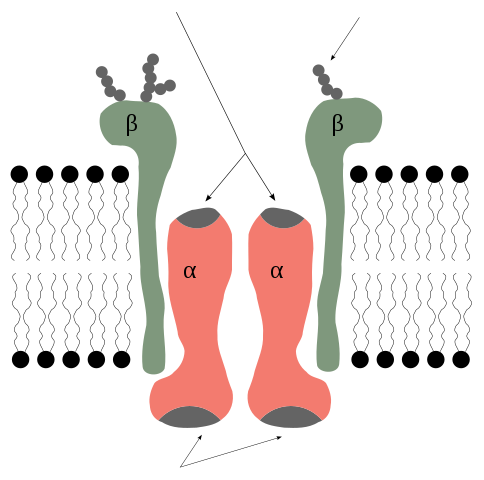
Las subunidades α son las que contienen los sitios de unión para el ATP y para los iones Na+ y K+ y representan el componente catalítico de la enzima y el que ejerce la función de bomba propiamente dicha.
Las subunidades α son polipéptidosde gran tamaño, con un peso molecular de 120 kDa, 10 segmentos transmembranales y con sus extremos N- y C-terminales ubicados del lado citosólico.
Poseen del lado intracelular sitios de unión para el ATP y para el Na+, así como un residuo de aspartato en la posición 376 que representa el sitio que sufre el proceso de fosforilación durante la activación de la bomba.
El sitio de unión para el K+ aparentemente se encuentra en el lado extracelular.
Las subunidades β no parecen tener una participación directa en la función de bombeo, pero en su ausencia dicha función no se produce.
Las subunidades β poseen un peso molecular de unos 55 kDa cada una y son glicoproteínas con un solo dominio transmembranal cuyos residuos glucídicos se encuentran insertados en la región extracelular.
Parecen ser necesarias en el retículo endoplasmático, en donde contribuirían al plegamiento adecuado de las subunidades α, y luego, a nivel ya de la membrana, para estabilizar el complejo.
Ambos tipos de subunidades son heterogéneas y se han descrito hasta el momento isoformas α1, α2 y α3 para la una, y β1, β2 y β3 para la otra. La α1 se encuentra en las membranas de la mayoría de las células, mientras que la α2 está presente en músculo, corazón, tejido adiposo y cerebro y la α3 en corazón y cerebro.
La isoforma β1 es la de distribución más difusa, aunque está ausente en algunos tejidos como las células vestibulares del oído interno y las células musculares glicolíticas de respuesta rápida. Estas últimas contienen solo β2.
Las diferentes estructuras de las subunidades que componen la bomba Na+/K+ en los diferentes tejidos tal vez obedezcan a especializaciones de tipo funcional aún no dilucidadas.
Para cualquier momento que se considere, la membrana plasmática constituye un límite de separación entre el compartimiento correspondiente al interior de una célula y aquel que representa el líquido extracelular en el cual se encuentra inmersa.
Ambos compartimentos tienen una composición que puede resultar cualitativamente diferente, puesto que en el interior de las células hay sustancias que no se encuentran fuera de ellas y el líquido extracelular contiene sustancias que no están presentes intracelularmente.
Sustancias que se hallan presentes en ambos compartimientos pueden encontrarse en concentraciones diferentes, y esas diferencias pueden poseer una significación fisiológica. Tal es el caso de muchos iones.
La bomba Na+/K+ cumple una función fundamental en el mantenimiento de la homeóstasis intracelular mediante el control de las concentraciones de los iones sodio y potasio. Este mantenimiento de la homeóstasis lo consigue gracias a:
- Transporte de iones: introduce iones de sodio y expulsa iones de potasio, proceso a través del cual también impulsa el movimiento de otras moléculas a través de otros transportadores que dependen bien sea de la carga eléctrica o de la concentración interna de estos iones.
- Control del volumen celular: la introducción o salida de iones implica también movimientos de agua dentre de la célula, por lo que la bomba participa en el control del volumen celular.
- Generación del potencial de membrana: las expulsión de 3 iones de sodio por cada 2 iones de potasio que son introducidos hace que la membrana permanezca cargada negativamente en la cara interna, lo que genera una diferencia de cargas entre el interior y el exterior celular. Esta diferencia se conoce como potencial de reposo.
El Na+ tiene una concentración extracelular de unos 142 mEq/L, mientras que su concentración intracelular es de solo 12 mEq/L; el K+, por su lado, está más concentrado dentro de la célula (140 mEq/L) que por fuera de ella (4 mEq/L).
Aunque la carga eléctrica de estos iones no permite su paso a través de la membrana, existen canales iónicos que sí lo permiten (selectivamente), los cuales propician el movimiento si las fuerzas que ordinariamente mueven estos iones también están presentes.
Ahora bien, estas diferencias de concentración tienen una gran importancia en la conservación de la homeostasis del organismo y deben mantenerse en una especie de equilibrio que de perderse se producirían alteraciones orgánicas importantes.
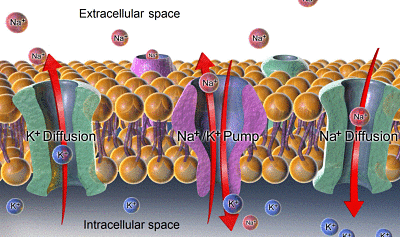
- La diferencia de concentración para el Na+ entre el interior y el exterior de la célula crea un gradiente químico que empuja al sodio hacia dentro y hace que constantemente este ión esté entrando y tienda a disipar esa diferencia, es decir, a igualar las concentraciones en ambos lados.
- El gradiente de potasio es mantenido en sentido contrario, es decir, de dentro hacia afuera, permitiendo la salida constante del ión y su reducción interna e incremento externo.
La función de la bomba Na+/K+ permite la extracción del sodio que ha entrado por difusión a través de canales o por otras vías de transporte y la reintroducción del potasio que haya difundido hacia afuera, permitiendo la conservación de las concentraciones intra y extracelulares de estos iones.
El mecanismo de acción de la ATPasa Na+/K+ consiste en un ciclo catalítico que implica reacciones de transferencia de un grupo fosforilo (Pi) y cambios conformacionales de la enzima que pasa de un estado E1 a un estado E2 y viceversa.
La operación requiere de la presencia de ATP y de Na+ en el interior de la célula y de K+ en el líquido extracelular.
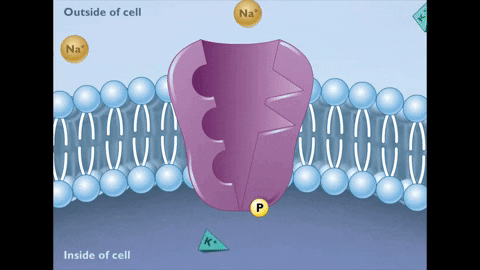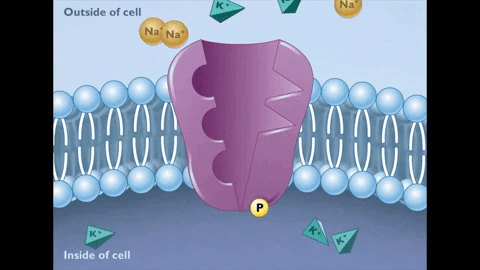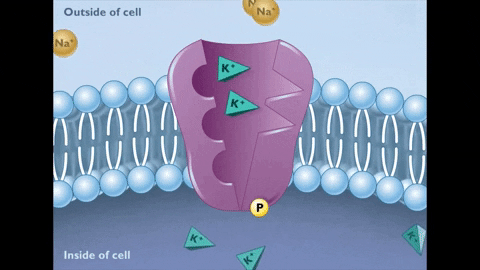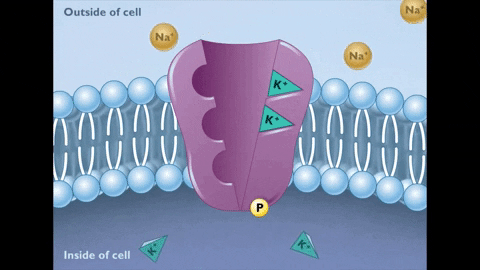
El ciclo se inicia en el estado de conformación E1 de la enzima, en el cual existen 3 sitios citosólicos de unión al Na+ y de alta afinidad (Km de 0,6 mM) que son ocupados en su totalidad porque la concentración intra del ion (12 mM) lo permite.
En este estado (E1) y con el Na+ fijado a sus sitios de unión, el ATP se fija a su sitio en el sector citosólico de la molécula, se hidroliza y se transfiere un grupo fosfato al aspartato 376, formándose un acilfosfato de alta energía que induce un cambio conformacional al estado E2.
El cambio conformacional al estado E2 implica que los sitios de unión al Na+ pasen al exterior, su afinidad por el ión disminuya muchísimo y se libere en el líquido extracelular, mientras que, al mismo tiempo, la afinidad de los sitios de unión al K+ aumenta y estos iones se unen por fuera a la bomba.
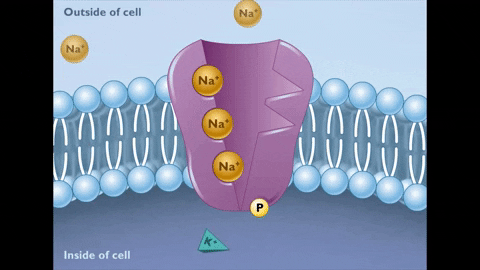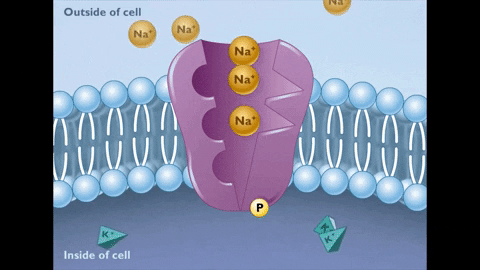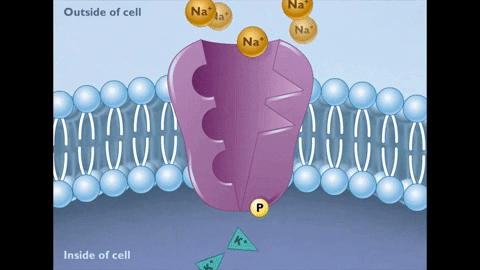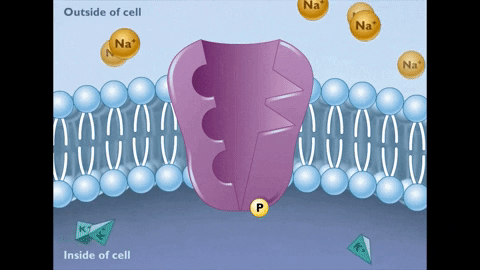
Una vez liberado el Na+ y unido el K+ se produce la hidrólisis del fosfato de aspartilo y se revierte el cambio conformacional del estado E2 al estado E1, con la reintroducción de los sitios de unión para el Na+ vacíos y los de K+ ocupados.
Al producirse este cambio, los sitios para el Na+ recuperan su afinidad y los de K+ la pierden, con lo cual el K+ es liberado en el interior de la célula.
La bomba Na+/K+ se haya presente en la mayoría, si no en todas, las células de los mamíferos, en las cuales reviste una importancia de índole general al contribuir a mantener su osmolaridad y por ende su volumen.
La entrada continua de iones sodio al interior de la célula va condicionando un aumento en el número intracelular de partículas osmóticamente activas, lo cual induce la entrada de agua y el incremento de volumen que terminaría provocando la ruptura de la membrana y el colapso celular.
Como estas bombas introducen solo 2 K+ por cada 3 Na+ que sacan, estas se comportan electrogénicamente, lo que quiere decir que “descompensan” las cargas eléctricas internas, favoreciendo la producción del potencial de membrana característico de las células corporales.
Su importancia también es evidente en relación con las células que componen los tejidos excitables, en los cuales los potenciales de acción se caracterizan por la entrada del ion Na+, que despolariza la célula, y la salida de K+, que la repolariza.
Estos movimientos iónicos son posibles gracias a la operación de las bombas de Na+/K+, que contribuyen a la producción de los gradientes químicos que mueven a los iones implicados.
Sin estas bombas, que operan en sentido contrario, los gradientes de concentración de estos iones se disiparían y la actividad excitatoria desaparecería.
Otro aspecto que destaca la importancia extrema de las bombas sodio-potasio, está en relación con la función renal, que sin ellas sería imposible.
La función renal implica la filtración diaria de más o menos 180 litros de plasma y de grandes cantidades de sustancias, algunas de las cuales deben ser excretadas, pero muchas tienen que ser reabsorbidas para que no se pierdan por la orina.
La reabsorción del sodio, del agua y de muchas de las sustancias filtradas depende de estas bombas, las cuales se encuentran ubicadas en la membrana basolateral de las células que conforman los epitelios de los distintos segmentos tubulares de las nefronas del riñón.
Las células epiteliales que tapizan los túbulos renales tienen una cara que está en contacto con la luz del túbulo y que se llama cara apical, y otra que está en contacto con el intersticio alrededor del túbulo y llamada basolateral.
El agua y las sustancias que se reabsorben deben pasar primero al interior de la célula a través de la apical y luego al intersticio por la basolateral.
La reabsorción de Na+ es clave tanto en relación con él, como en relación con la del agua y la de otras sustancias que dependen de la de él. La entrada apical de Na+ a la célula requiere que exista un gradiente que lo mueva y que implica una muy baja concentración del ión en el interior de la célula.
Esa baja concentración intracelular de Na+ la producen las bombas de sodio de la membrana basolateral que trabajan intensamente para sacar el ión desde las células hacia el intersticio.
- Ganong WF: The General & Cellular Basis of Medical Physiology, in: Review of Medical Physiology, 25th ed. New York, McGraw-Hill Education, 2016.
- Guyton AC, Hall JE: Substance Transport Across the Cell Membrane, in: Textbook of Medical Physiology, 13th ed, AC Guyton, JE Hall (eds). Philadelphia, Elsevier Inc., 2016.
- Lodish H, Berk A, Zipursky SL, Matsudaira P, Baltimore D, Darnell J: Transport across the Cells Membranes, In: Molecular and Cell Biology, 4th ed.
- Nelson, D. L., Lehninger, A. L., & Cox, M. M. (2008). Lehninger principles of biochemistry. Macmillan.
- Alberts, B., Bray, D., Hopkin, K., Johnson, A. D., Lewis, J., Raff, M., … & Walter, P. (2013). Essential cell biology. Garland Science.
