Anetol: estructura, propiedades, usos, toxicidad
El anetol es un compuesto orgánico de fórmula molecular C10H22O, derivado del fenilpropeno. Presenta un olor característico del aceite de anís y un sabor dulce. Naturalmente se encuentra en algunos aceites esenciales.
Los aceites esenciales son líquidos a temperatura ambiente, siendo los responsables del olor de las plantas. Se encuentran principalmente en plantas de la familia de las labiadas (menta, lavanda, tomillo y romero) y las umbelíferas (anís e hinojo); de estas últimas se extrae, por arrastre de vapor, el anetol.

El anís y el hinojo son plantas que contienen el anetol, un éter fenólico, que en el caso del anís se encuentra en su fruto. Este compuesto se utiliza como diurético, carminativo y expectorante. Además se adiciona a los alimentos para darles sabor.
Se sintetiza por esterificación de p-cresol con alcohol metílico, y condensación subsiguiente con aldehído. El anetol puede ser extraido de las plantas que lo contienen por destilación en corriente de vapor de agua.
El anetol tiene efectos tóxicos, pudiendo provocar irritación en la piel, en los ojos, en el tracto respiratorio o en el tracto digestivo, dependiendo del sitio de contacto.
Índice del artículo
- 1 Estructura del anetol
- 2 Propiedades
- 2.1 Nombres
- 2.2 Fórmula molecular
- 2.3 Descripción física
- 2.4 Punto de ebullición
- 2.5 Punto de fusión
- 2.6 Punto de Ignición
- 2.7 Solubilidad en agua
- 2.8 Solubilidad en solventes orgánicos
- 2.9 Densidad
- 2.10 Presión de vapor
- 2.11 Viscosidad
- 2.12 Índice de refracción
- 2.13 Estabilidad
- 2.14 Temperatura de almacenamiento
- 2.15 pH
- 3 Usos
- 4 Toxicidad
- 5 Referencias
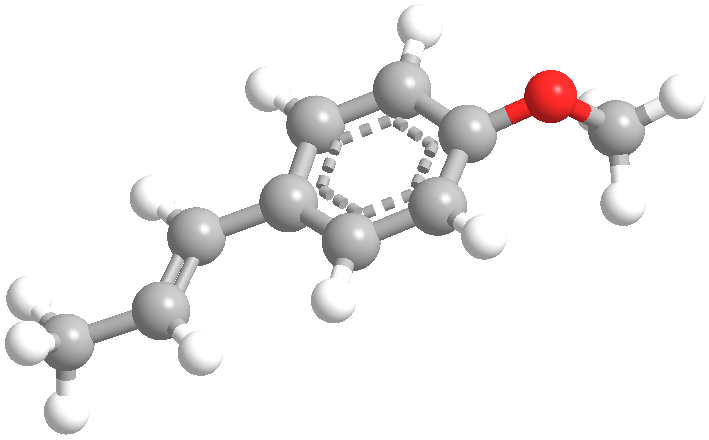
Se muestra en la imagen superior la estructura de una molécula de anetol en un modelo de esferas y barras.
Aquí se puede ver por qué se trata de un éter fenólico: a la derecha está el grupo metoxi, –OCH3, y si se ignora por un momento el CH3, se tendrá el anillo fenólico (con un sustituyente propeno) sin hidrógeno, ArO–. Por lo tanto, de forma resumida su fórmula estructural podría visualizarse como ArOCH3.
Es una molécula cuyo esqueleto carbonado puede situarse en un mismo plano, por tener casi todos sus átomos hibridación sp2.
Su fuerza intermolecular es de tipo dipolo-dipolo, con la mayor densidad electrónica ubicada hacia la región del anillo y el grupo metoxi. Nótese además, el carácter relativamente anfifílico del anetol: el –OCH3 es polar, y el resto de su estructura es apolar e hidrofóbica.
Este hecho explica su baja solubilidad en agua, comportándose como cualquier grasa o aceite. Asimismo, explica su afinidad por otras grasas presentes en fuentes naturales.
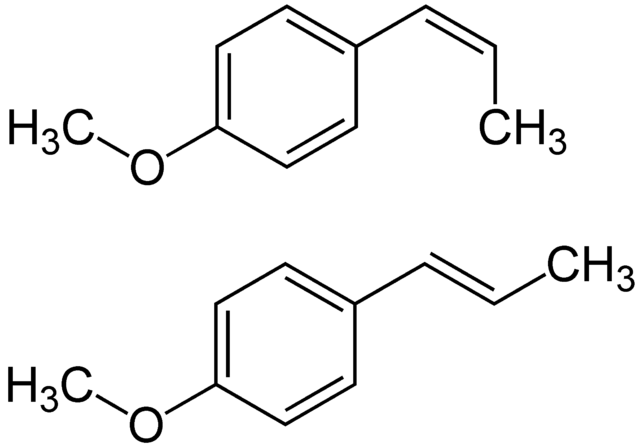
El anetol puede estar presente en dos formas isoméricas. En la primera imagen de la estructura se mostró la forma trans (E), la más estable y abundante. Nuevamente, en la imagen superior se muestra esta estructura, pero acompañada por su isómero cis (Z), en la parte de arriba.
Nótese la diferencia entre ambos isómeros: la posición relativa del –OCH3 con respecto al anillo aromático. En el isómero cis del anetol, el –OCH3 está más cercano al anillo, resultando en un impedimento estérico, el cual desestabiliza la molécula.
De hecho, tal es la desestabilización, que propiedades como el punto de fusión se ven alterados. Como regla general, las grasas cis presentan puntos de fusión menores, y sus interacciones intermoleculares son menos eficientes frente a los de las grasas trans.
anexol y 1-metoxi-4-propenil benceno
C10H22O
Cristales blancos o líquido incoloro, a veces amarillo pálido.
454,1 ºF a 760 mmHg (234 ºC).
704 ºF (21,3 ºC).
195 ºF.
Es prácticamente insoluble en agua (1,0 g/l) a 25 ºC.
En proporción 1:8 en etanol al 80%; 1:1 en etanol al 90%.
Miscible con el cloroformo y el éter. Alcanza una concentración 10 mM en dimetil sulfóxido. Soluble en benceno, acetato de etilo, disulfuro de carbono y éter de petróleo.
0,9882 g/ml a 20 º C.
5,45 Pa a 294 ºK.
2,45 x 10-3 Poise.
1,561
Estable, pero es un compuesto combustible. Incompatible con agentes oxidantes fuertes.
Entre 2 y 8 ºC.
7,0.
Al anetol tritiona (ATT) se le atribuyen numerosas funciones, entre ellas el aumento de la secreción salival, la cual ayuda en el tratamiento de la xerostomía.
En el anetol, y en las plantas que lo contienen, se ha demostrado una actividad relacionada con el aparato respiratorio y con el aparato digestivo, además de poseer una acción antiinflamatoria, anticolinesterásica y quimiopreventiva.
Existe una relación entre el contenido de anetol de una planta y su acción terapéutica. Por ello, la acción terapéutica se le atribuye al atenol.
Las actividades terapéuticas de las plantas que contienen anetol, hace que todas ellas sean antiespasmódicas, carminativas, antisépticas y expectorantes. También presentan propiedades eupépticas, secretolíticas, galactógogas y, a dosis muy elevadas, actividad emenógoga.
El anetol presenta una semejanza estructural con la dopamina, por lo que se señala que puede interaccionar con los receptores del neurotransmisor, induciendo la secreción de la hormona prolactina; responsable de la acción galactógoga que se le atribuye al atenol.
El anís estrellado, un aromatizante culinario, se usa en el tratamiento de dolores de estómago. Además, se le atribuyen propiedades analgésicas, neurotrópicas y de disminución de la fiebre. Se usa como carminativo y en el alivio de los cólicos en los niños.
El anís se usa contra los insectos áfidos (pulgones), los cuales chupan las hojas y brotes produciendo su enroscamiento.
El anetol actúa como insecticida sobre las larvas de las especies de mosquitos Ochlerotatus caspices y Aedes egypti. Además actúa como pesticida sobre el ácaro (arácnido). Tiene una acción insecticida en la especie de cucaracha Blastella germanica.
Asimismo, actúa sobre varias especies adultas de gorgojos. Por último, el anetol es un agente repelente de insectos, especialmente de los zancudos.
El anetol actúa sobre la bacteria Salmonella entérica, actuando en forma bactericida y bacteriostática. Presenta actividad antifúngica, especialmente sobre las especies Saccharomyces cerevisiae y Candida albicans, siendo esta última un especie oportunista.
El anetol ejerce una acción antihelmíntica in vitro sobre los huevos y larvas de la especie de nematodo Haemonchus contortus, localizado en el tracto digestivo de las ovejas.
El anetol, así como las plantas que presentan un alto contenido del compuesto, se emplea como saborizante en muchos alimentos, bebidas y confiterías, por lo agradable de su sabor dulce. Se utiliza en bebidas alcohólicas como el ouzo, raki y Pernoud.
Debido a su baja solubilidad en agua, el anetol es responsable del efecto ouzo. Al agregarle agua al licor ouzo, se forman gotas minúsculas de anetol que enturbian el licor. Esta es una prueba de su autenticidad.
Puede causar por contacto irritación de los ojos y de la piel, manifestándose en la piel en eritema y edema causante de descamación. Por ingestión puede producir estomatitis, un signo que acompaña la toxicidad del anetol. Mientras que por inhalación hay irritación de las vías respiratorias.
El anís estrellado (alto contenido de anetol) puede producir alergia, sobre todo en los bebés. Asimismo, el consumo excesivo de anetol puede inducir la aparición de síntomas, tales como espasmos musculares, confusión mental y somnolencia debido a su acción narcótica.
La intoxicación por anís estrellado aumenta cuando se usa intensamente en forma de aceites esenciales puros.
- Graham Solomons T.W., Craig B. Fryhle. (2011). Organic Chemistry. Amines. (10th edition.). Wiley Plus.
- Drugbank. (2017). Anethole trithione. Recuperado de: drugbank.ca
- Be Kind Botanicals. (2017). Fennel & other essential oils with (E)-anethole. Recuperado de: bkbotanicals.com
- Chemical Book. (2017). trans-Anethole. Recuperado de: chemicalbook.com
- PubChem. (2019). Anethole. Recuperado de: pubchem.ncbi.nlm.nih.gov
- Wikipedia. (2019). Anethole. Recuperado de: en.wikipedia.org
- María E. Carretero. (s.f.). Plantas medicinales con aceite esencial rico en anetol. [PDF]. Recuperado de: botplusweb.portalfarma.com
- Admin. (21 de octubre de 2018). What is anethole? Trusted Health Products. Recuperado de: trustedhealthproducts.com
