Sulfito de sodio (Na2SO3): qué es, estructura, propiedades, usos
¿Qué es el sulfito de sodio?
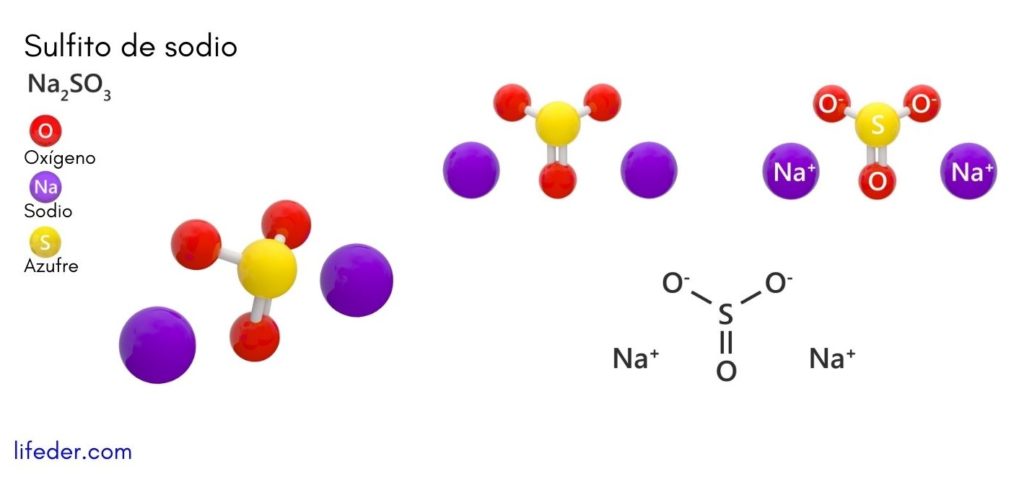
El sulfito de sodio o sulfito sódico, cuya fórmula química es Na2SO3, es una sal soluble de sodio que se obtiene como producto de la reacción del ácido sulfuroso (u óxido de azufre (IV)) con hidróxido de sodio.
Entre 1650 y 1660, Glauber comenzó a fabricar el sulfito de sodio a partir de sal común (NaCl) y ácido sulfúrico concentrado. Este proceso es considerado como el inicio de la industria química.
El proceso de sulfito produce pulpa de madera, que se observa como fibra de celulosa casi pura mediante el uso de varias sales de ácido sulfuroso para extraer la lignina de astillas de madera.
Así, los sulfitos poseen un gran número de aplicaciones de distintos tipos, incluyendo en la industria de alimentos como aditivo. Entre sus funciones más relevantes destaca su capacidad de inhibición del pardeamiento enzimático y no enzimático, el control e inhibición del crecimiento microbiano, la prevención del enranciamiento oxidativo y la modificación de las propiedades reológicas de los alimentos.
Preparación del sulfito de sodio
Generalmente, a escala de laboratorio, el sulfito de sodio se produce a partir de la reacción de la solución de hidróxido de sodio con gas de dióxido de azufre (2NaOH + SO2 → Na2SO3 + H2O).
Luego la evolución del SO2 mediante la adición de unas gotas de ácido clorhídrico concentrado indicará si el hidróxido de sodio está casi desaparecido, convertido en sulfito de sodio acuoso (Na2SO3 + 2HCl → 2NaCl + SO2 + H2O).
Por otro lado, este compuesto químico se obtiene industrialmente haciendo reaccionar el dióxido de sulfuro con una solución de carbonato de sodio.
La combinación inicial genera bisulfito de sodio (NaHSO3), que al reaccionar luego con hidróxido de sodio o carbonato de sodio es convertido en sulfito de sodio. Estas reacciones pueden resumirse en la reacción global SO2 + Na2CO3 → Na2SO3 + CO2.
Estructura química
Todas las formas del sulfito de sodio se caracterizan por ser sólidos blancos, cristalinos e higroscópicos, los cuales tienen la capacidad de atraer y retener fácilmente las moléculas de agua del entorno circundante, que normalmente están a temperatura ambiente.
El tipo de estructura cristalina está ligado a la presencia de agua en el compuesto. El sulfito de sodio anhídrido presenta una estructura ortorrómbica o hexagonal y, en caso de que exista presencia de moléculas de agua en el compuesto, cambia su estructura (por ejemplo, el sulfito de sodio heptahidratado presenta una estructura monoclínica).
Propiedades
Esta especie posee determinadas propiedades físicas y químicas que la diferencian de otras sales, las cuales se describen a continuación:
Propiedades químicas
Como solución acuosa saturada, esta sustancia tiene un pH aproximado de 9. Además, las soluciones expuestas al aire eventualmente se oxidan a sulfato de sodio.
Por otro lado, si se deja cristalizar el sulfito de sodio de la solución acuosa a temperatura ambiente o inferior, lo hace como un heptahidrato. Los cristales de heptahidratos eflorescen en aire caliente y seco, también se oxidan en el aire para formar el sulfato.
En este sentido, la forma anhidra es mucho más estable contra la oxidación por aire. El sulfito es incompatible con ácidos, fuertes oxidantes y altas temperaturas. Además es insoluble en amoníaco y en cloro.
Propiedades físicas
El sulfito de sodio anhídrido tiene una masa molar de 126,43 g/mol, una densidad de 2,633 g/cm3, un punto de fusión de 33,4 °C (92,1 °F o 306,5 K), un punto de ebullición de 1,429 °C (2,604 °F o 1,702 K), y no es inflamable. Asimismo, la solubilidad (medida a una temperatura de 20 °C) es de 13,9 g/100 ml.
Usos/aplicaciones
Por sus propiedades reactivas, el sulfito de sodio es muy versátil y actualmente y utilizando ampliamente en diferentes tipos de industrias.
- Es ampliamente empleado en el tratamiento de aguas y eliminación de oxígeno disuelto en el agua para calderas.
- También tiene aplicaciones en la industria del papel (pulpa semilíquida).
- En fotografía se utiliza en la fabricación de reveladores.
- En grado adecuado se usa en la conservación de alimentos y antioxidante.
- En la industria textil se emplea en los procesos de blanqueo y anticloro.
- Igualmente es utilizado como agente reductor.
- Además, se usa en la recuperación secundaria de pozos petrolíferos.
- Incluso es empleado en la manufactura de compuestos orgánicos, colorantes, tintas, rayón viscosa y cauchos.
- Es utilizado en la manufactura de numerosos químicos, incluyendo sulfato de potasio, sulfito de sodio, silicato de sodio, hiposulfito de sodio y sulfato de aluminio sodio.
Riesgos
Efectos por exposición al compuesto
La exposición prolongada o reiterada a esta sustancia puede provocar dermatitis y reacciones de sensibilidad. La exposición en personas sensibles al sulfito, asmáticas y atópicas puede provocar broncoconstricción grave y reducir los niveles del volumen espiratorio forzado.
De igual manera, la descomposición ácida del sulfito de sodio puede liberar humos tóxicos y peligrosos de óxidos de azufre, incluyendo el dióxido de azufre, que puede provocar deterioro pulmonar permanente debido a la exposición crónica y aguda.
Similarmente, el envenenamiento agudo por dióxido de azufre es poco frecuente porque el gas se detecta fácilmente. Es tan irritante que no se puede tolerar el contacto.
Entre los síntomas, se incluyen tos, ronquera, estornudos, lagrimeo y dificultad para respirar. Sin embargo, los empleados con una alta exposición inevitable pueden sufrir daño pulmonar importante y posiblemente mortal.
Ecotoxicidad
El sulfito de sodio es una solución no peligrosa, que se usa comúnmente como agente de decloración del agua residual. Las altas concentraciones contribuyen a la demanda elevada de oxígeno químico en ambientes acuáticos.
Consumo de alimentos con conservantes
Uno de los aditivos que puede causar problemas en personas sensibles es el grupo conocido como agentes de sulfitación, que incluyen varios aditivos inorgánicos de sulfito (E220-228), entre ellos el sulfito sódico (SO2).
En personas hipersensibles o asmáticas, el consumo de alimentos con sulfitos o la inhalación de dióxido de azufre, puede resultar tóxico.
Estos compuestos son los responsables de la bronco-constricción que se traduce en dificultad para respirar. El único tratamiento para esta reacción desmedida es evitar los alimentos y las bebidas que contengan sulfitos.
