Ósmosis: proceso, tipos, diferencias con difusión y ejemplos
La ósmosis es un fenómeno pasivo de desplazamiento del agua a través de una membrana. Esta puede ser una membrana de una célula, un epitelio o una membrana artificial. El agua se moviliza desde una región de baja presión osmótica (o donde el agua es más abundante) hasta la región con presiones osmóticas mayores (o donde el agua es menos abundante).
Este proceso es de relevancia biológica y orquesta una serie de procesos fisiológicos, tanto en animales como en plantas.
El primer investigador en reportar el fenómeno osmótico fue Abbé Jean Antoine Nollet. En el año 1748, Nollet estaba trabajando con membranas de células animales y notó que cuando se colocaba agua pura de un lado de la membrana y del otro lado una solución con electrolitos diluidos, el agua se desplazaba hacia la región con solutos.
Así, se describió el paso del agua a favor de su gradiente de concentración y se denominó ósmosis. El término proviene de las raíces griegas osmos, que quiere decir empujar.
En 1877, Wilhelm Pfeller realizó los primeros estudios sobre la presión osmótica. Su diseño experimental involucraba el uso de una “membrana” de ferrocianuro de cobre sobre la superficie de una copa de arcilla porosa, dando origen a una membrana que permitía el paso de moléculas de agua.
Las membranas artificiales de Pfeller eran lo suficientemente fuertes como para soportar presiones osmóticas significativas y no colapsar. Este investigador pudo concluir que la presión osmótica es proporcional a la concentración de soluto.
Índice del artículo
- 1 Proceso
- 2 Presión osmótica
- 3 ¿Cómo se controla el flujo de agua en las células?
- 4 Cuantificación
- 5 Diferencias con difusión
- 6 Ejemplos
- 7 Referencias
El movimiento del agua a través de una membrana desde una zona de baja concentración a una zona de alta concentración recibe el nombre de ósmosis. Este proceso ocurre desde una zona con la menor presión osmótica hacia la mayor presión osmótica.
Al principio, esta afirmación puede ser confusa – y hasta contradictoria. Estamos acostumbrados al movimiento pasivo de “alto a bajo”. Por ejemplo, el calor se puede desde temperaturas altas a bajas, la glucosa difunde desde regiones de alta concentración a zonas menos concentradas, y así sucesivamente.
Como mencionamos, el agua que experimenta el fenómeno de ósmosis se desplaza de presiones bajas a presiones alta. Esto ocurre porque el agua es más abundante por unidad de volumen donde el soluto es menos abundante.
Es decir, durante la ósmosis el agua se moviliza donde ella (el agua) es más abundante a donde es menos abundante. Por ello, el fenómeno debe entenderse desde la perspectiva del agua.
Es importante recordar que la ósmosis gobierna el movimiento del agua a través de las membranas y no afecta el movimiento de los solutos directamente. Cuando los solutos difunden, lo hacen siguiendo los gradientes de su propia concentración química. Solo el agua sigue el gradiente de concentración de la presión osmótica.
Uno de los aspectos más confusos a la hora de comprender el proceso de ósmosis es el uso de la palabra presiones. Para evitar desconciertos, es importante aclarar que una solución por sí sola no ejerce una presión hidrostática debido a su presión osmótica.
Por ejemplo, una solución de glucosa a concentración 1 M tiene una presión osmótica de 22 atm. Sin embargo, la solución no “explota” las botellas de vidrios y puede almacenarse de la misma manera que el agua pura porque una solución aislada no se traduce en una presión hidrostática.
El término presiones se usa solamente por un accidente histórico, ya que los primeros científicos que estudiaron estos fenómenos eran físicos y químicos.
Así, si dos soluciones que difieren en sus presiones osmóticas están separadas por una membrana, se creará una presión hidrostática.
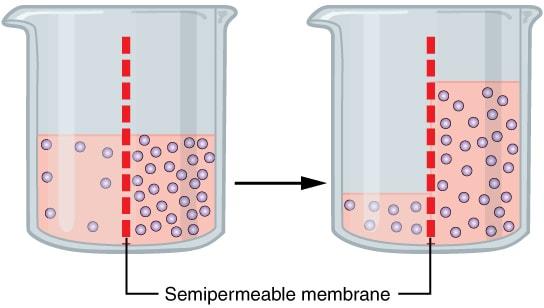
El proceso de ósmosis conduce a la formación de una presión hidrostática. La diferencia de presión lleva al aumento de nivel de la solución más concentrada, a medida que el agua difunde hacia esta. El aumento en el nivel del agua continua hasta que la tasa neta del movimiento de agua se iguala a cero.
Se alcanza un flujo neto cuando la presión hidrostática en el compartimiento II es suficiente para obligar a las moléculas de agua a retroceder al comportamiento I, a la misma tasa que la ósmosis hace que las moléculas se desplacen desde el compartimiento I al II.
A la presión del agua que causa el retroceso de las partículas (desde el compartimiento I al II) se denomina presión osmótica de la solución en el compartimiento II.
Gracias al fenómeno osmótico, el agua puede desplazarse por las membranas de las células de manera pasiva. Históricamente se conoce que los animales carecen de un sistema de transporte activo de agua para controlar el flujo de esta sustancia.
Sin embargo, los sistemas de transporte activo de solutos pueden modificar la dirección del desplazamiento del agua hacia una dirección favorable. De esta manera, el transporte activo de solutos es una manera por la cual los animales usan su energía metabólica para controlar la dirección del transporte de agua.
Existen fórmulas matemáticas que permiten la medición de la tasa a la cual el agua cruzará las membranas por ósmosis. La ecuación para calcularla es la siguiente:
Tasa del transporte osmótica del agua = K (Π1–Π2 / X). Donde Π1 y Π2 son las presiones osmóticas de las soluciones en ambos lados de la membrana y X es la distancia que las separa.
La relación (Π1–Π2 / X) es conocida como gradiente de presión osmótica o gradiente osmótico.
El último término de la ecuación es K es el coeficiente de proporcionalidad que depende de la temperatura y de la permeabilidad de la membrana.
La difusión ocurre por el movimiento térmico aleatorio de las moléculas disueltas o suspendidas, que provoca su dispersión desde las regiones de concentraciones elevadas a las más bajas. La tasa de difusión puede ser calculada por medio de ecuación de Fick.
Es un proceso exergónico debido al incremento de la entropía representado por la distribución al azar de las moléculas.
En caso tal de que la sustancia sea un electrolítico se debe tomar en cuenta – además de las concentraciones – la diferencia total de carga entre los dos compartimientos.
Difusión y ósmosis no son términos contrarios, ni mucho menos conceptos mutuamente excluyentes.
Las moléculas de agua tienen la capacidad de desplazarse con rapidez a través de las membranas celulares. Como explicamos, ellas difunden de una región de baja concentración de soluto a una de alta concentración en un proceso denominado ósmosis.
Nos pareciera extraño hablar de “concentración del agua”, pero esta sustancia se comporta como cualquier otra sustancia. Es decir, difunde a favor de su gradiente de concentración.
Sin embargo, algunos autores usan como sinónimo de osmosis el término “difusión de agua”. Aplicarlo literalmente a los sistemas biológicos puede ser errado, ya que se ha demostrado que la tasa de ósmosis a través de membranas biológicas es mayor que lo que se esperaría por un simple proceso de difusión.
En algunos sistemas biológicos el agua pasa por simple difusión por la membrana celular. No obstante, algunas células poseen canales especiales para el paso de agua. Los más importantes se denominan acuaporinas, incrementando la velocidad del flujo de agua a través de la membrana.
Dentro de los sistemas biológicos, el movimiento del agua a través de las membranas celulares es crucial para entender decenas de procesos fisiológicos. Algunos ejemplos son:
Un ejemplo interesante del papel de la ósmosis en los animales es el intercambio de agua que ocurre en los peces que viven en aguas dulces.
Los animales que habitan cuerpos de agua dulce están en una toma constante de agua desde el rio o estanque donde viven hacia el interior de sus cuerpos, ya que la concentración del plasma sanguíneo y otros fluidos corporales tienen una concentración mucho más elevada que la del agua.
La especie de pez Carassius auratus vive en ambientes de agua dulce. Un individuo que tenga una masa de 100 gramos puede llegar a ganar unos 30 gramos de agua por día gracias al desplazamiento de agua al interior de su cuerpo. El pez cuenta con sistemas – energéticamente costosos – para deshacerse continuamente del exceso de agua.
En el sistema gastrointestinal de los animales debe ocurrir el fenómeno de osmosis para que este funcione correctamente. El tubo digestivo secreta una cantidad de líquido significativa (en el orden litros) que deben ser reabsorbidos por ósmosis por las células que tapizan los intestinos.
En caso de que este sistema no lleve a cabo su labor, se pueden presentar eventos de diarrea intensa. La prolongación de este malfuncionamiento puede traducirse en la deshidratación del paciente.
El volumen de agua del interior de las células depende de la concentración tanto del medio interior como del externo, y el flujo está orquestado por los fenómenos de difusión y ósmosis.
Si se coloca una célula animal (como un eritrocito) en un medio que favorece la entrada de agua, esta podría llegar a reventarse. En contraste, las células vegetales cuentan con una pared que las protege del estrés osmótico.
De hecho, las plantas no leñosas sacan provecho de esta presión generada por la entrada pasiva de agua. Dicha presión ayuda a mantener turgentes a distintos órganos vegetales, como las hojas. En el momento en que el agua empieza a salir de las células, la célula pierde turgencia y se marchita.
- Cooper, G. M., Hausman, R. E., & Hausman, R. E. (2000). The cell: a molecular approach. ASM press.
- Eckert, R., Randall, R., & Augustine, G. (1988). Animal physiology: mechanisms and adaptations. WH Freeman & Co.
- Hill, R. W., Wyse, G. A., Anderson, M., & Anderson, M. (2004). Animal Physiology. Sinauer Associates.
- Karp, G. (2009). Cell and molecular biology: concepts and experiments. John Wiley & Sons.
- Pollard, T. D., Earnshaw, W. C., Lippincott-Schwartz, J., & Johnson, G. (2016). Cell Biology E-Book. Elsevier Health Sciences.
- Schmidt-Nielsen, K. (1997). Animal physiology: adaptation and environment. Cambridge University Press.
