Tenecteplasa: para qué sirve, estructura, mecanismo de acción, dosis
La tenecteplasa es un activador tisular del plasminógeno (tPA) sintetizado por la industria farmacéutica mediante técnicas de ADN recombinante aplicadas en una línea celular obtenida a partir de células ováricas de hámster chino.
El proceso de coagulación de la sangre, que concluye con la formación de un trombo y la retracción del coágulo, se continúa con una fase denominada fibrinólisis. Esta fase está caracterizada por la disolución del trombo mediante la fragmentación del polímero de fibrina en péptidos más pequeños y solubles, y la recanalización del vaso, o los vasos, en donde ocurrió la coagulación.
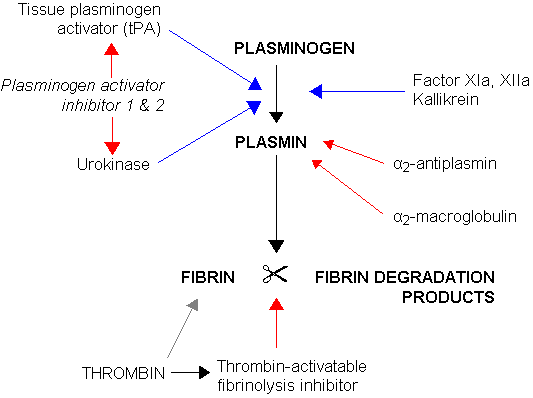
Este proceso fibrinolítico requiere de la participación de una proteína sanguínea del grupo de las globulinas plasmáticas llamada plasminógeno o profibrinolisina, de unos 81 kDa, sintetizada en el hígado y presente normalmente en la sangre circulante. Este plasminógeno queda atrapado durante la coagulación entre las redes de fibrina que conforman el trombo.
El plasminógeno per se carece de cualquier acción fibrinolítica, acción que solo aparece cuando la molécula original es activada y convertida en plasmina o fibrinolisina, la cual es una serino proteasa muy similar a la tripsina, que es la enzima digestiva proteolítica más importante de la secreción pancreática.
La plasmina tiene una gran afinidad por la fibrina, a la cual fragmenta en pequeños péptidos solubles que a su vez inhiben la acción de la trombina y la producción ulterior de más fibrina. Ejerce, además, una acción proteolítica sobre el fibrinógeno, la protrombina y los factores de coagulación V, VIII, IX, XI y XII, con lo cual reduce también la capacidad coagulatoria de la sangre.
De este cuadro expuesto se deduce que la plasmina influye de dos maneras sobre los procesos de coagulación de la sangre, ya que por un lado produce la disolución del trombo mediante su acción fibrinolítica, y por otro interfiere con la coagulación a través de su acción proteolítica sobre factores clave del proceso de coagulación.
Índice del artículo
- 1 ¿Para qué sirve la tenecteplasa?
- 2 Estructura de la molécula
- 3 Mecanismo de acción
- 4 Presentación
- 5 Dosis
- 6 Referencias
La activación del plasminógeno ocurre por la acción individual o combinada de un conjunto de sustancias que se denominan genéricamente activadores del plasminógeno, y las cuales, de acuerdo con su origen, se agrupan en activadores del plasminógeno: sanguíneos, urinarios, tisulares y provenientes de microorganismos.
Tratándose de un activador tisular del plasminógeno que lo convierte en plasmina, y siendo la plasmina el agente fibrinolítico por excelencia, pues se utiliza la tenecteplasa para la fibrinólisis terapéutica en el infarto agudo de miocardio, los accidentes cerebrovasculares tromboembólicos y el tromboembolismo pulmonar.
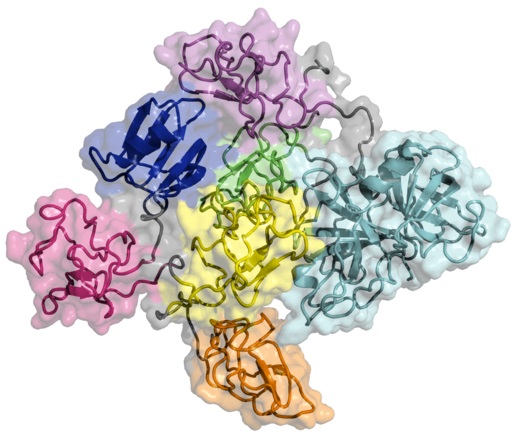
La tenecteplasa es una glicoproteína que posee en su estructura primaria 527 aminoácidos y en la cual se distinguen dos dominios básicos, uno llamado dominio kringle y otro que corresponde al dominio proteasa.
El dominio kringle es una zona de la proteína que se pliega en grandes bucles que logran su estabilización mediante enlaces disulfuro. Este tipo de dominio es muy importante porque permite las interacciones proteína-proteína que se dan con factores de la coagulación de la sangre y recibe su denominación de un pastel escandinavo a cuya forma se asemeja.
El dominio proteasa es la zona de la molécula que posee la actividad proteolítica que le confiere a la enzima su función activadora propiamente dicha.
La estructura de la molécula es muy parecida a la del tPA humano natural, sin embargo, la tecnología del ADN recombinante permitió la introducción de algunas modificaciones en su ADN complementario (ADNc) que le brindan a la proteína en él codificada algunas ventajas terapéuticas.
Dichas modificaciones incluyen la sustitución de la treonina en posición 103 por asparagina y la asparagina 117 por glutamina, cambios que se ubican en el dominio kringle; mientras que en el dominio proteasa se logró un montaje tetra-alanina en el rango posicional 296-299.
El mecanismo de acción de la tenecteplasa es parecido al del tPA natural. Una vez formado el trombo, el plasminógeno en su forma inactiva se une a la fibrina sin ejercer sobre ella ninguna acción proteolítica.
El tPA producido por las células endoteliales se une a la fibrina, con lo cual adquiere su propiedad activadora del plasminógeno en plasmina, sustancia que desencadena la fibrinólisis.
Las modificaciones producidas en la molécula de tPA e incorporadas a la tenecteplasa hacen más sensible a la presencia de fibrina la acción activadora de dicha sustancia sobre el plasminógeno. Especificidad por la fibrina que limita su acción a los sitios en los cuales haya trombos y reduce la activación sistémica de plasminógeno y la degradación resultante del fibrinógeno plasmático.
La dosificación o la potencia de la sustancia se expresa en mg y en unidades (U) de tenecteplasa. Las unidades representan un patrón de referencia específico para la droga y no es comparable con las unidades de otros agentes trombolíticos. Un mg equivale a 200 unidades (U).
Una forma comercial es el Metalyse, el cual viene en dos presentaciones, cada una de las cuales tiene un vial con el producto en forma de un polvo blanco y una jeringa precargada con el solvente, transparente e incoloro, para su reconstitución.
En una de ellas el vial contiene 8000 unidades (40 mg) y la jeringa 8 ml de disolvente. En la otra el vial contiene 10000 U (50 mg) y la jeringa 10 ml. En ambos casos, una vez reconstituida la solución añadiendo el contenido de la jeringa al vial correspondiente, esta contendrá 1000 unidades (5 mg) por cada ml y tendrá un aspecto claro e incoloro, o ligeramente amarillo.
El tratamiento con tenecteplasa debe iniciarse lo más rápidamente posible, en un lapso no mayor de 6 horas después de la aparición de los síntomas. Debido a los riesgos implícitos de sangramientos o hemorragias debe ser prescrito por médicos con experiencia en tratamiento trombolítico y en instituciones con medios para monitorizar y contrarrestar este tipo de efectos colaterales.
La dosificación de la sustancia debe hacerse en función del peso corporal, con una dosis mínima de 6000 unidades, equivalente a 30 mg disueltos en un volumen de 6 ml de la solución reconstituida, a administrar en pacientes con peso corporal por debajo de 60 kg.
La dosis máxima es de 10000 U (50 mg/10 ml de solución) reservada para pacientes con peso corporal de 90 kg para arriba.
El esquema posológico para pacientes cuyos pesos se ubican en el rango entre 60 y por debajo de los 90 kg es el siguiente:
– ≥ 60 a 70 = 7000 U (35 mg/7 ml)
– ≥ 70 a 80 = 8000 U (40 mg/8 ml)
– ≥ 80 a 90 = 9000 U (45 mg/9 ml)
La dosis requerida debe administrarse en forma de un bolo intravenoso único y durante un lapso de unos 10 segundos. Puede administrarse a través de un circuito intravenoso previamente conectado y a través del cual se esté pasando una solución fisiológica de cloruro sódico al 0,9% (9 mg/ml).
La droga es incompatible con las soluciones glucosadas, y aunque de acuerdo a criterios terapéuticos actuales debe administrarse paralelamente tratamiento antitrombótico coadyuvante que pudiera incluir antiagregantes plaquetarios y anticoagulantes, no debe añadirse ningún otro medicamento a la solución inyectable de tenecteplasa.
- Balsera, E. C., Palomino, M. Á. P., Ordoñez, J. M., Caler, C. L., Paredes, T. G., & García, G. Q. (2011). Efectividad y seguridad de la alteplasa frente a la tenecteplasa en la fibrinólisis del síndrome coronario agudo con elevación de ST. Cardiocore, 46(4), 150-154.
- Bauer C and Walzog B: Blut: ein Flüssiges Organsystem, in: Physiologie, 6th ed; R Klinke et al (eds). Stuttgart, Georg Thieme Verlag, 2010.
- Fatovich, D. M., Dobb, G. J., & Clugston, R. A. (2004). A pilot randomised trial of thrombolysis in cardiac arrest (The TICA trial). Resuscitation, 61(3), 309-313.
- Guyton AC, Hall JE: Hemostasis and Blood Coagulation, in: Textbook of Medical Physiology , 13th ed, AC Guyton, JE Hall (eds). Philadelphia, Elsevier Inc., 2016.
- Haley Jr, E. C., Lyden, P. D., Johnston, K. C., Hemmen, T. M., & TNK in Stroke Investigators. (2005). A pilot dose-escalation safety study of tenecteplase in acute ischemic stroke. Stroke, 36(3), 607-612.
- Jelkman W: Blut, in: Physiologie des Menschen mit Pathophysiologie, 31 th ed, RF Schmidt et al (eds). Heidelberg, Springer Medizin Verlag, 2010.
