Hidróxido de estroncio: qué es, estructura química, propiedades y usos

¿Qué es el hidróxido de estroncio?
El hidróxido de estroncio (Sr(OH)₂) es un compuesto químico inorgánico conformado por un ion de estroncio (Sr) y dos iones de hidróxido (OH). Este compuesto se obtiene al combinar una sal de estroncio con una base fuerte, dando como resultado un compuesto de naturaleza alcalina cuya fórmula química es Sr(OH)2.
Por lo general, para la preparación del hidróxido de estroncio se utiliza como base fuerte el hidróxido de sodio (NaOH) o hidróxido de Potasio (KOH). Por otro lado, la sal de estroncio (o ion de estroncio) que reacciona con la base fuerte es el nitrato de estroncio Sr(NO3)2 y el proceso está descrito mediante la siguiente reacción química:
2KOH + Sr(NO3)2 → 2KNO3 + Sr(OH)2
En solución el catión de estroncio (Sr+) se pone en contacto con el anión hidróxido (OH–) formando una sal iónica básica del estroncio. Ya que el estroncio es un metal alcalinotérreo, el hidróxido de estroncio es considerado un compuesto álcali cáustico.
Obtención del hidróxido de estroncio
Además del proceso explicado previamente, se puede decir que una vez llevada a cabo la reacción, el Sr(OH)2 precipita en la solución. Luego esta es sometida al proceso de lavado y secado, obteniéndose finalmente un polvo blanco muy fino.
Un método alternativo para la obtención de hidróxido de estroncio es a partir del calentamiento de carbonato de estroncio (SrCO3) o sulfato de estroncio (SrSO4), con vapor a una temperatura que oscile entre los 500° C y 600° C. La reacción química ocurre como se muestra a continuación:
SrCO3 + H2O → Sr(OH)2 + CO2
SrS + 2H2O → Sr(OH)2 + H2S
Estructura química y propiedades fisicoquímicas
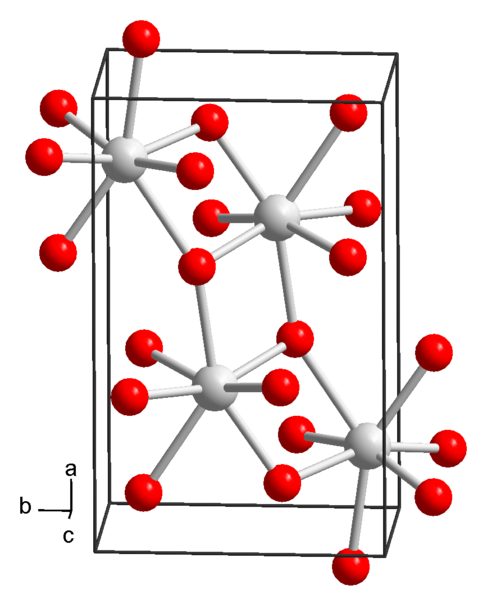
En la actualidad se conocen 3 formas de hidróxido de estroncio: octahidratado, monohidratado y anhidro.
Hidróxido de estroncio octahidratado
A partir de soluciones en condiciones normales de temperatura y presión (25° C y 1 atm), el hidróxido de estroncio precipita de forma octahidratada, cuya fórmula química es Sr(OH)2∙8H2O.
Este compuesto posee una masa molar de 265,76 g/mol, una densidad de 1,90 g/cm y precipita como cristales tetragonales (con grupo espacial P4/ncc) de apariencia prismática cuadrangular e incolora.
Asimismo, el hidróxido de estroncio octahidratado tiene la capacidad de absorber la humedad atmosférica, ya que es un compuesto fácilmente delicuescente.
Hidróxido de estroncio monohidratado
De acuerdo a estudios de microscopía óptica (realizados mediante la técnica de difracción de rayos X), al elevar la temperatura hasta unos 210° C -a una presión atmosférica constante- el Sr(OH)2∙8H2O es deshidratado y transformado en hidróxido de estroncio monohidratado (Sr(OH)2∙H2O).
Esta forma del compuesto tiene una masa molar de 139,65 g/mol y su temperatura de fusión es de -73,15° C (375K). Debido a su configuración atómica, este presenta menor solubilidad en agua que la descrita en su forma octahidratada.
Hidróxido de estroncio anhidro
Al continuar con el incremento de temperatura del sistema hasta unos 480° C, la deshidratación se prolonga hasta obtener un hidróxido de estroncio anhidro.
A diferencia de sus formas hidratadas, este posee una masa molar de 121,63 g/mol y una densidad 3,625 g/cm3. Su punto de ebullición se alcanza a los 710° C (1,310° F o 983 K) mientras que el punto de fusión se encuentra a 535° C (995° F u 808 K).
Solubilidad
El hidróxido octahidratado de estroncio posee una solubilidad en agua de 0,91 gramos por 100 mililitros (medidos a 0° C), mientras su forma anhidra a condiciones similares de temperatura presenta una solubilidad de 0,41 gramos por cada 100 mililitros.
Del mismo modo, esta sustancia se considera insoluble en acetona y totalmente soluble en ácidos y cloruro de amonio.
Reactividad química
El hidróxido de estroncio no es inflamable, su reactividad química permanece estable a temperaturas y presiones moderadas, y es capaz de absorber el dióxido de carbono del aire atmosférico, transformándolo en carbonato de estroncio.
Además, es un compuesto severamente irritante si se pone en contacto con la piel, vías respiratorias u otras mucosas del cuerpo.
Usos del hidróxido de estroncio
Debido a sus características higroscópicas y propiedades básicas, el hidróxido de estroncio es utilizado para diferentes aplicaciones en la industria:
- Extracción de melaza y refinación del azúcar a partir de la remolacha.
- Estabilizador de plásticos.
- Grasas y lubricantes.
Extracción de melaza y refinación del azúcar de remolacha
A comienzos del siglo XXI, en Alemania se empezó a utilizar el hidróxido de estroncio para el refinado de azúcar proveniente de la remolacha, mediante el proceso patentado por Carl Scheibler en 1882.
Este procedimiento consiste en la mezcla del hidróxido de estroncio y la pulpa azucarada de la remolacha, lo cual da como resultado un disacárido insoluble. Esta solución es separada por decantación y una vez llevado a cabo el proceso de refinado, se obtiene el azúcar como producto final.
A pesar de que en la actualidad este procedimiento se sigue utilizando, existen otros métodos con mucha más demanda por ser más económicos, que son empleados en la gran mayoría de las refinerías de azúcar del mundo. Por ejemplo, el método Barsil, que utiliza silicato de bario, o el método Steffen, usando cal como agente extractor.
Grasas de estroncio
Son grasas lubricantes que contienen hidróxido de estroncio. Estas son capaces de adherirse fuertemente a superficies con características metálicas, son resistentes al agua y soportan cambios bruscos de temperatura.
Debido a su buena estabilidad física y química, estas grasas son utilizadas como lubricantes industriales.
Estabilizador de plásticos
La gran mayoría de los plásticos, al estar expuestos a factores climáticos tales como el sol, la lluvia y el oxígeno atmosférico, modifican sus propiedades y se degradan.
Por su considerable resistencia al agua, el hidróxido de estroncio es agregado a estos polímeros -durante la fase de fusión- actuando como estabilizador en la fabricación de productos de plástico para prolongar su vida útil.
Otras aplicaciones
- En la industria de la pintura es utilizado como un aditivo imprescindible para acelerar el proceso de secado en las pinturas comerciales e industriales.
- A partir del hidróxido de estroncio se obtienen las sales o iones de estroncio, que son utilizados como materia prima para la producción de artículos de pirotecnia.
Referencias
- Wikipedia (n.d.). Strontium hydroxide. Recuperado de en.wikipedia.org
- PubChem (s.f.). Strontium Hydroxide. Obtenido de pubchem.ncbi.nlm.nih.gov
- Lambert, I. y Clever, H. L. (2013). Alkaline Earth Hydroxides in Water and Aqueous Solutions. Recuperado de books.google.co.ve
- Krebs, R. E. (2006). The History and Use of Our Earth’s Chemical Elements: A Reference Guide. Obtenido de books.google.co.ve
- Honeywell (s.f.). Strontium Hydroxide Octahydrate. Recuperado de honeywell.com
