Densidad relativa: cálculo, ejemplos, ejercicios
La densidad relativa es la relación adimensional que existe entre la densidad de una sustancia y otra de referencia que generalmente es el agua a 4 ºC (39.2 ºF) para líquidos y sólidos, mientras que para los gases se emplea el aire seco.
En algunos textos se la denomina también gravedad específica (traducción literal de specific gravity en inglés), pero se trata del mismo concepto. Ambas densidades deben estar en el mismo sistema de unidades y haber sido medidas en iguales condiciones de presión y temperatura.

La densidad relativa se calcula matemáticamente de la siguiente manera:
Densidad relativa = densidad del material/densidad del agua
Si bien la densidad de cualquier sustancia depende de las condiciones de presión y temperatura en que se mide, sobre todo cuando se trata de gases, la densidad relativa es un concepto muy útil para caracterizar rápidamente materiales diversos.
Enseguida se aprecia esto, ya que la densidad del agua es aproximadamente de 1 gramo por cada centímetro cúbico: 1 g/cc o 1000 kg /m3, a presión atmosférica y en un buen rango de temperaturas (de 0 a 15 º C).
Dando la densidad relativa de una sustancia se sabe de inmediato cómo de ligera o pesada es con respecto al agua, la sustancia universal.
Además la densidad relativa es un valor fácil de recordar ya que se mide con números pequeños y fáciles de manejar, como se verá en el siguiente apartado, en el que se mencionan los valores de las densidades relativas para algunas sustancias conocidas.
Índice del artículo
La densidad relativa del agua evidentemente es 1, puesto que como se dijo al comienzo, es el patrón de referencia para líquidos y sólidos. Líquidos como el café, la leche o los refrescos tienen densidades relativas muy cercanas a la del agua.
En cuanto a los aceites, no existe un valor único de densidad relativa aplicable a todos, ya que depende de su origen, composición y procesamiento. La mayoría de las densidades relativas para aceites están en un rango de entre 0.7 y 0.95.
Los gases son mucho más livianos, así que en muchas aplicaciones la referencia que se toma es la densidad del aire, de tal forma que la densidad relativa señala cómo de liviano o pesado un gas respecto al aire. En comparación con el agua, la densidad relativa del aire es 0.0013.
Veamos algunos valores de densidad relativa para sustancias y materiales conocidos.
– Cuerpo humano: 1.07.
– Mercurio: 13.6.
– Glicerina: 1.26.
– Gasolina: 0.68.
– Agua de mar: 1.025.
– Acero: 7.8.
– Madera: 0.5.
– Hielo: 0.92.
El valor de la densidad relativa informa de inmediato sobre si una sustancia o material flota en agua o por el contrario se hunde.
En vista de esto, una capa de aceite quedará encima de una de agua, puesto que casi todos los aceites tienen densidad relativa menor que la de este líquido. Un cubo de madera en agua podrá tener una porción fuera de la misma, de igual manera que el hielo.
La densidad absoluta es el cociente entre la masa de una sustancia y el volumen que ocupa. Como el volumen a su vez depende de la temperatura (al calentarse la mayoría de sustancias se dilatan) y la presión, la densidad a su vez depende de estas dos magnitudes. Matemáticamente se tiene:
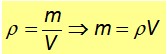
Donde ρ es la densidad, cuyas unidades en el Sistema Internacional son Kg/m3, m es la masa y V es el volumen.
Debido a la relación que tiene el volumen con la temperatura y la presión, los valores de densidad absoluta que aparecen en las tablas suelen estar especificados a presión atmosférica y en ciertos rangos de temperatura.
Así, en condiciones normales para los gases: 1 atmósfera de presión y 0º C de temperatura, la densidad del aire se establece en 1.293 Kg/m3.
Pese a que su valor experimenta estas variaciones, es una cantidad muy apropiada para determinar el comportamiento de las sustancias, sobre todo en medios considerados continuos.
La diferencia con la densidad relativa es que la absoluta sí tiene dimensiones, en cuyo caso sus valores dependen del sistema de unidades seleccionado. De esta manera la densidad del agua a 4º C de temperatura es:
ρagua = 1 g /cm3 = 1000 Kg/m3 = 1.94 slug/pie3
Encuentre el volumen ocupado por 16 gramos de aceite cuya densidad relativa es 0.8.
Solución
Primero encontramos la densidad absoluta ρaceite del aceite. Denotando como sg su densidad relativa se tiene:
ρaceite = 0.8 x Densidad del agua
Para la densidad del agua se usará el valor dado en el apartado anterior. Cuando se conoce la densidad relativa, la absoluta se recupera inmediatamente multiplicando este valor por la densidad del agua. Así:
Densidad del material = Densidad relativa x Densidad del agua (en condiciones normales).
Por lo tanto, para el aceite de este ejemplo:
ρaceite = 0.8 x 1 g/cm3= 0.8 g/cm3
Puesto que la densidad es el cociente entre masa m y volumen V, este quedará de la siguiente forma:
V = m/ρ = 16 g / 0.8 g/cm3= 20 cm3
Una roca posee gravedad específica de 2.32 y un volumen de 1.42 x 10 -4 m3. Encuentre el peso de la roca en unidades del Sistema Internacional y en el sistema técnico.
Solución
Se usará el valor de la densidad del agua como 1000 Kg/m3:
ρroca = 2.32 x 1000 Kg/m3= 2.32 x 103 Kg/m3
La masa m de la roca es en kilogramos:
m = rroca . V=2.32 x 103 Kg/m3. 1.42 x 10 -4 m3 = 0.33 Kg.
El peso en unidades del sistema técnico es 0.33 Kilogramo-fuerza. Si se prefiere en el sistema internacional, entonces la unidad es Newton, para lo cual se multiplica la masa por el valor de g, la aceleración de gravedad.
P = m. g = 0.33 Kg. 9.8 m/s2 = 3.23 N.
Un picnómetro es un recipiente con el cual puede determinarse la densidad relativa de una sustancia a cierta temperatura.

Para determinar la densidad de un líquido desconocido en el laboratorio se siguió este procedimiento:
– Se pesó el picnómetro vacío y la lectura fue de 26.038 g
– Luego se llenó el picnómetro con agua a 20º C (densidad del agua 0.99823 g/cc) y se pesó, obteniéndose un valor de 35.966 g.
– Finalmente se pesó el picnómetro lleno del líquido desconocido y la lectura obtenida fue de 37.791 g.
Se pide deducir una expresión para calcular la densidad del líquido y aplicarla con los datos obtenidos.
Solución

La masa tanto del agua como la del fluido se determinan restando la lectura del picnómetro lleno de la del picnómetro vacío:
masa H2O = 35.966 g – 26.038 g = 9.928 g; masa fluido = 37.791 g – 26.038 g = 11.753 g
Finalmente se sustituye en la expresión que se dedujo:
ρfluido = (11.753 g / 9.928 g) . 0.99823 g/cc = 1.182 g/cc.
- Enciclopedia Británica. Specific gravity. Recobrado de: britannica.com.
- Giancoli, D. 2006. Physics: Principles with Applications. 6th.. Ed Prentice Hall.
- Mott, R. 2006. Mecánica de Fluidos. 4ta. Edición. Pearson Educación. 12-21.
- Valera Negrete, J. 2005. Apuntes de Física General. UNAM. 44-45.
- White, F. 2004. Mecánica de Fluidos. 5ta Edición. Mc Graw Hill. 17-18.
