Benzoato de sodio: estructura, propiedades, usos y riesgos
El benzoato de sodio es una sal orgánica cuya fórmula química es C6H5COONa. Se produce o genera mediante la reacción de neutralización entre el ácido benzoico y el hidróxido de sodio. El resultado es un sólido blanco (imagen inferior) soluble en el agua y que se descompone por calentamiento a 120 ºC.
Esta sal puede encontrarse naturalmente en varias frutas y otras partes de vegetales, tales como: arándanos, ciruelas, pasas, canela, clavos de olor y manzanas. Asimismo, es un metabolito de las algas y de las plantas.

El benzoato de sodio no se acumula en el organismo, ya que se combina rápidamente con el aminoácido glicina para formar el ácido hippúrico, el cual se excreta libremente en la orina.
Este compuesto es utilizado con conservante de alimentos, siendo más eficiente su acción a un pH ácido. Esto se debe a la presencia de ácidos orgánicos que le confieren a los alimentos un pH adecuado para la acción del benzoato de sodio; que como tal, termina protonándose a ácido benzoico.
Esta sal también se utiliza en el tratamiento de desórdenes metabólicos hereditarios del ciclo de la urea, lo cual produce la acumulación de un metabolito intermedio, para el cual la enzima que lo procesa está deficiente.
El Programa Internacional Sobre la Seguridad Química no encontró ningún efecto nocivo del benzoato de sodio sobre los seres humanos, para un consumo comprendido entre 647 – 825 mg/kg de masa corporal.
Sin embargo, ha sido reportado que el benzoato de sodio puede producir reacciones pseudoalérgicas y exacerbar los síntomas en pacientes con episodios de urticaria frecuentes y asma.
Índice del artículo
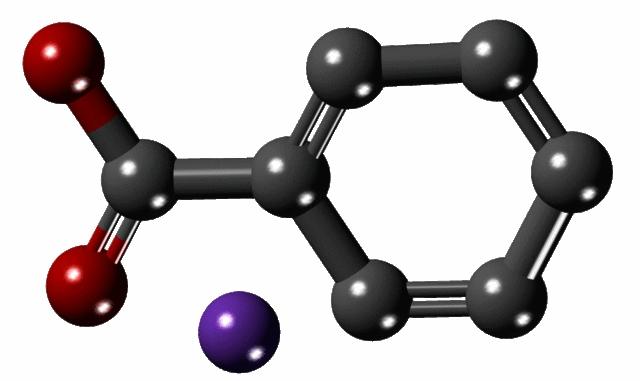
En la imagen superior se muestra la estructura del benzoato de sodio con un modelo de esferas y barras. Puede notarse a simple vista el anillo aromático, con el grupo carboxilato, -COO–, enlazado a él (el de las esferas rojas); y este último, a su vez, atrae electrostáticamente al catión Na+ (esfera morada).
Como la diferencia de tamaño entre ambos iones es grande (compárense en la imagen), no es extraño que la energía reticular de los cristales de benzoato de sodio sea baja. Esto provoca que sus cristales tengan una tendencia natural a solubilizarse en solventes polares o sufrir una serie de reacciones químicas.
El C6H5COO– puede aceptar dos puentes de hidrógeno provenientes de dos moléculas de agua, lo que favorece su hidratación. Mientras, el Na+ también termina solvatado por el agua, venciendo las fuerzas electrostáticas que lo mantiene unido al C6H5COO–.
Así pues, esta sal se compone de iones C6H5COO– y Na+, los cuales se disponen de manera ordenada para construir cristales. En la literatura no se consigue información al respecto de su estructura cristalina, por lo que se desconoce cuál es el tipo de celda unitaria para esta sal.
-Benzoato de sodio
-Sal sódica del ácido benzoico
-Sobenato
-Antimol.
Gránulos blancos o polvo cristalino. Polvo cristalino incoloro.
Inodoro.
Agridulce, astringente y desagradable.
> 100 ºC.
> 500 ºC.
1,50 g/cm3.
-Soluble en amonio líquido y en piridina.
-Poco soluble en etanol: 8,22 g/100 g a 25 ºC.
-En metanol es más soluble que en etanol: 8,22 g/100 g a 15 ºC.
Es estable bajo las condiciones recomendadas de almacenamiento. Puede ser sensible a la humedad, hidrolizándose a ácido benzoico. Incompatible con agentes oxidantes fuertes, álcalis y ácidos minerales.
Cuando se calienta a descomposición a 120 ºC (248 ºF), emite un humo acre de óxido de sodio y otros componentes que pueden ser tóxicos y carcinógenos.
Al descomponerse a 120 ºC, impide que pueda determinarse con precisión sus puntos de ebullición y fusión, siendo los valores reportados de estos parámetros estimaciones teóricas.
Cercano a 8, disuelto en agua. Es decir, que se trata de una sal básica. Esto se debe a que se hidroliza para liberar iones OH–.
72,9 mN/cm a 20 ºC en una solución de 1 g/l de agua.
El ácido benzoico que interviene en la síntesis del benzoato de sodio se produce principalmente por tres métodos:
-El naftaleno se oxida con pentóxido de vanadio para formar el anhídrido ftálico. Este compuesto puede someterse a descarboxilación para originar el ácido benzoico, ya que en su estructura con dos anillos aromáticos aparenta tener dos grupos –COO condensados entre sí.
-El tolueno es oxidado a ácido benzoico mediante la adición de ácido nítrico. En esta reacción el grupo metilo “simplemente” se oxida al grupo carboxilo:
C6H5CH3 => C6H5COOH
-Y por último, el benzotricloruro se hidroliza por la acción de ácidos minerales, originando el ácido benzoico.
Obtenido el ácido benzoico por cualquiera de estos tres métodos, se disuelve luego en hidróxido de sodio. Estos compuestos experimentan una reacción de neutralización, produciéndose benzoato de sodio y agua.
C6H5COOH + NaOH => C6H5COONa + H2O
La reacción también puede llevarse a cabo con carbonato de sodio, aunque su rendimiento puede que sea menor al deseado.
El benzoato de sodio es un agente conservante de los alimentos, siendo capaz de inhibir o retardar el proceso de fermentación, la acidificación o cualquier proceso que produzca un deterioro de los mismos. Además, el benzoato de sodio tiene una acción fungicida.
Esta sal es capaz de eliminar las levaduras, bacterias y hongos presentes en los alimentos. Su acción conservante es más eficiente a pH 6; es decir, en condiciones ácidas. Por esta razón es usado en conservas y en aliños de ensaladas que contienen vinagre (ácido acético).
El benzoato de sodio también se utiliza en la conservación de las bebidas carbonatadas y refrescos, en los que está presente el ácido carbónico. También en las mermeladas, ricas en ácido cítrico, y en general, en alimentos con ácidos presentes que establezcan un medio ácido.
Además, se utiliza en el pienso con una concentración de benzoato de sodio del 0,1 %. La máxima cantidad de ácido benzoico y benzoato de sodio usados, como preservativos en los alimentos, no excede a 2.000 mg/kg del alimento.
Hiperamonemia aguda
El fenilacetato sódico y el benzoato de sodio son usados, bajo la forma de terapias adyuvantes, en el tratamiento de una hiperamonemia aguda y una encelopatía asociada en pacientes con alteraciones del ciclo de la urea.
Estos compuestos son clasificados como drogas huérfanas. Esta denominación se aplica a fármacos que no son rentables desde el punto de vista económico.
Esquizofrenia
El benzoato de sodio se ha utilizado experimentalmente en el tratamiento de la esquizofrenia. La parte central de la investigación es el papel que en el tratamiento cumple la inhibición de las enzimas oxidasas de los D-aminoácidos, actividad que cumple el benzoato de sodio.
Aciduria arginosuccínica
El benzoato de sodio se emplea en el tratamiento de la aciduria arginosuccínica, un desorden metabólico hereditario que puede causar en los pacientes una elevación en la concentración de amonio, capaz de afectar el sistema nervioso central.
Inhibidor
-Es un inhibidor de la enzima araquidonato 15-lipoxigenasa, una enzima que es investigada por la industria farmacéutica por estar involucrada en las coronariopatías.
-Inhibe la acción de la enzima lipasa de triacilglicéridos, enzima que actúa produciendo la liberación del glicerol y los ácidos grasos en el intestino delgado, permitiendo así la absorción de estos lípidos presentes en los alimentos.
Quizás sea posible la utilización del benzoato de sodio para regular la absorción intestinal de lípidos como los triacilglicéridos.
Desórdenes hereditarios
El benzoato de sodio se utiliza en el tratamiento de varios desórdenes hereditarios, relacionados con el metabolismo de los aminoácidos, entre los cuales se citan: tratamiento de la hiperargininemia, y el tratamiento de la deficiencia de la enzima translocasa de la ornitina.
-Se usa en enjuagues de base alcohólica y en el pulimento de la plata. Además, se emplea en la elaboración de compuestos pirotécnicos, siendo responsable del silbido producido cuando son encendidos.
-Se emplea como anticorrosivo, que es una las principales demandas en la producción de esta sal. También se usa en refrigerantes, anticongelantes y otros sistemas en base de agua.
-En la formulación de plásticos como el polipropileno, se utiliza para mejorar su resistencia y claridad.
-Sirve como estabilizador en baños y procesos fotográficos.
El benzoato de sodio es clasificado por la FDA como “generalmente seguro”, a dosis de 0,1 % del peso de los alimentos. No se le considera irritante al contacto con la piel y los ojos, por lo que puede decirse que la toxicidad aguda es baja.
Sin embargo, el benzoato de sodio puede producir reacciones no inmunológicas (pseudoalergia) por contacto. Este efecto es raro en personas normales, pero en pacientes con episodios de urticarias frecuentes o síntomas de asma, puede producirse un aumento de la frecuencia de estos síntomas.
En estudios realizados en ratas y ratones, no se encontró indicios de una acción carcinogénica del benzoato de sodio.
Se ha señalado la inconveniencia de su uso en presencia de ácido ascórbico, que pudiese producir el benceno; compuesto tóxico, señalado como carcinogénico.
- Net Industries. (2019). Sodium benzoate production. Recuperado de: science.jrank.org
- Wikipedia. (2019). Sodium benzoate. Recuperado de: en.wikipedia.org
- PubChem. (2019). Sodium benzoate. Recuperado de: pubchem.ncbi.nim.nih.gov
- Hanes T. (2019). Facts on sodium benzoate. Livestrong. Recuperado de: livestrong.com
- Chemical Book. (2017). Sodium benzoate. Recuperado de: chemicalbook.com
- Lane H. y col. (2013) Jama Psichiatry. 70(12):1267 – 1275.
- World Health Organization Geneva. (12 de abril de 2005). Benzoic acid and sodium benzoate. [PDF]. Recuperado de: who.int
