Rojo de fenol: características, preparación, aplicaciones
El rojo de fenol es una sustancia de naturaleza orgánica que tiene la propiedad de cambiar de color cuando pasa de alcalino a ácido y viceversa. Por esta característica es utilizado como indicador ácido-base. También se le conoce con el nombre de fenolsulfonftaleína, y su fórmula química es C19H14O5S.
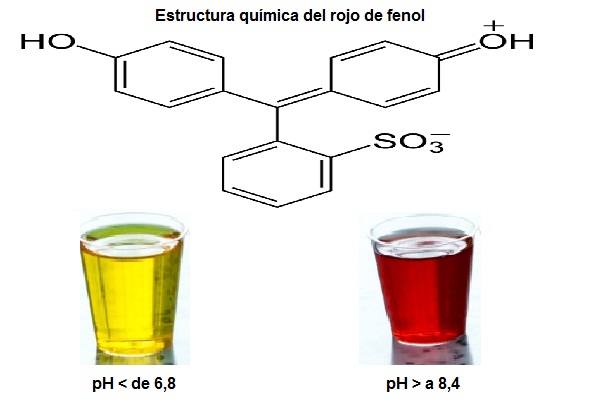
Este indicador de pH es de color amarillo por debajo de 6,8, y de color rojo por encima de 8,4. Esta sustancia no es carcinogénica, pero sí es capaz de irritar la piel y las mucosas. El rojo de fenol es uno de los indicadores de pH más utilizado en los laboratorios.
Se usa en la preparación de importantes pruebas bioquímicas en el diagnóstico e identificación de microorganismos bacterianos. Entre las pruebas bioquímicas y medios de cultivo que usan el rojo de fenol como indicador de pH se encuentran: el agar triple azúcar hierro (TSI), el Kligler, la urea, el agar manitol salado, el agar XLD, el agar verde brillante y el agar Vogel-Johnson.
También se ha usado el rojo de fenol en el diagnóstico de infecciones por Helicobacter pylori a través de la metodología diagnóstica conocida como cromoendoscopia.
Recientemente, se ha descubierto que el rojo de fenol tiene actividad estrogénica, debido a que posee una estructura similar. Por tanto, se une a los receptores de estrógeno presentes en algunas células.
Este hallazgo hace que se reconsidere el uso de rojo de fenol en la preparación de medios de cultivo celulares cuando se van a utilizar células sensibles a hormonas.
Índice del artículo
Es indicador rojo de fenol se caracteriza por ser un polvo formado por minúsculas partículas cristalinas de color rojo oscuro brillante. En solución el líquido es traslúcido y de color rojo claro. Es soluble en hidróxidos y carbonatos alcalinos, pero es moderadamente soluble en agua, alcohol etílico y acetona e insoluble en cloroformo.
Su masa molecular es de 354,59 g/mol, y su punto de fusión es de 285°C. Su densidad es de 0,972.
Para preparar la solución es necesario pesar 0.10 g de rojo de fenol y disolver en 14.2 ml de NaOH (hidróxido de sodio) 0.020 M. Luego, completar con agua destilada hasta un volumen final de 250 ml.
Se debe almacenar a temperatura ambiente, en lugar seco y bien ventilado.
Su uso principal está circunscrito a ser añadido a medios de cultivo para el diagnóstico e identificación de microorganismos bacterianos. El indicador de pH rojo de fenol se incluye en aquellos medios en los que se quiere evidenciar si el microorganismo ha sido capaz de fermentar ciertos carbohidratos.
La fermentación de carbohidratos genera la formación de ácidos. Por tanto, las colonias y el medio de cultivo virarán a color amarillo. Si por el contrario no hay fermentación del carbohidrato, entonces el microorganismo usará a las peptonas presentes. Esto alcaliniza el medio, el cual virará al color rojo.
Entre las pruebas bioquímicas que utilizan el rojo de fenol están los siguientes: medio triple azúcar hierro (TSI), Kligler y caldo rojo de fenol. Mientras que los medios de cultivos selectivos y diferenciales que usan el rojo de fenol son el agar manitol salado, el agar XLD, el agar verde brillante y el agar Vogel-Johnson.
Por otra parte, también la prueba de la urea utiliza el rojo de fenol como indicador de pH, pero en este caso lo que se quiere evidenciar es si el microorganismo es capaz de desdoblar la urea, lo que genera un producto que alcaliniza ligeramente al medio (amoníaco). En este caso hay un viraje de color a fucsia.
En caso de que no esté presente la ureasa, el medio quedará del mismo color.
Hernández y colaboradores utilizaron el indicador rojo de fenol al 0,1% más urea al 5% para evaluar la mucosa gástrica y diagnosticar la presencia de Helicobacter pylori. Esta técnica se denomina cromoendoscopia, y forma parte de las pruebas conocidas como reactivas.
Esta técnica tiene la ventaja de localizar eficientemente el sitio de las lesiones, evitar la contaminación y ser de lectura inmediata. La coloración amarilla se interpreta como negativa, y la coloración roja-fucsia se interpreta como una reacción positiva.
Diversas investigaciones han demostrado que el rojo de fenol posee una estructura química similar a ciertos estrógenos no esteroideos; y en medios de cultivo tisulares tiene actividad estrogénica, ya que tiene la propiedad de unirse al receptor de estrógeno cuando se encuentra a concentraciones entre 15 – 45 μg.
Especialmente, se ha visto que se une eficientemente al receptor de estrógeno de las células de cáncer de mama humano MCF-7, con una afinidad del 0,001%.
Esto representa un hallazgo muy importante, ya que los investigadores han tratado de obtener medios celulares libres de estrógeno para que las células no estén estimuladas. Para ello habían tratado de eliminar a los estrógenos del suero, pero jamás imaginaron que una sustancia que formaba parte del medio de cultivo pudiera simular la acción hormonal.
Por tanto, en este sentido, debe reconsiderarse el uso de medios de cultivos celulares que contengan rojo de fenol cuando se utilicen células sensibles al estrógeno.
Para la manipulación del rojo de fenol se recomienda el uso de instrumentos y medidas de bioseguridad.
En caso de derrame accidental, es necesario recoger la sustancia mecánicamente con materiales absorbentes. Desechar en contenedor apropiado. No debe verterse por el desagüe.
La NFPA (National Fire Protection Association) clasifica al rojo de fenol con un riesgo de salud 2. Esto significa un riesgo moderado. Por otro lado, en cuanto a inflamabilidad y reactividad está clasificado como 1 y 0 respectivamente; es decir, hay ligero riesgo de inflamabilidad y no hay riesgo de reactividad.
En cuanto a los daños que ocasiona el rojo de fenol al contacto directo se pueden mencionar la irritación de la piel y de la mucosa ocular. Así mismo, es perjudicial si es ingerido solo en grandes cantidades. No es peligrosa su inhalación y no es cancerígeno.
En el caso del contacto con piel y mucosas se recomienda lavar el área afectada con abundante agua por 15 minutos, levantando los párpados.
A nivel de piel se puede colocar una crema emoliente en la zona afectada para aliviar la irritación. Si la irritación persiste, es necesario acudir al médico.
En caso de ingestión leve debe enjuagarse la boca. Si la ingestión fue en volumen considerable es fundamental buscar asistencia médica inmediata. No provocar vómito, ni dar leche.
Se debe tener cuidado de que el rojo de fenol no se ponga en contacto con las siguientes sustancias con las que es incompatible: percloratos, peróxidos, permanganatos, fosfuros, estaño II, cloruro e hidruros metálicos. Con todos ellos puede reaccionar de forma violenta (explosiva) y causar incendio.
Berthois Y, Katzenellenbogen JA, Katzenellenbogen BS. Phenol red in tissue culture media is a weak estrogen: implications concerning the study of estrogen-responsive cells in culture. Proc Natl Acad Sci U S A. 1986; 83 (8): 2496–2500.
Hoja de seguridad del rojo de fenol MSDS. Universidad Nacional de Heredia. Costa Rica. Escuela de Química. Disponible en: Users/Equipo/Downloads/rojo%20fenol.pdf
ROTH. Ficha de datos de seguridad del rojo de fenol. 2015. España. Disponible en: carlroth.com
Ingenieros Químicos y Asociados. Rojo de fenol pH aguas. Hoja de seguridad. Colombia. Disponible en: recintodelpensamiento.com
Neogen. Base caldo rojo de fenol. Disponible en: foodsafety.neogen.com
Hernández H, Castellanos V, González L, Infante M, Peña K, Andrain Y. Cromoendoscopia con rojo fenol en el diagnóstico de la infección por Helicobacter pylori. Revista Española de Enfermedades Digestivas. 2012; 104 (1). Disponible en: scielo.org
Marín J, Díaz J, Solís J. Cromoendoscopia en la infección por Helicobacter pylori: ¿es tiempo de reacción? Revista española de enfermedades digestivas: órgano oficial de la Sociedad Española de Patología Digestiva. 2011; 104(1):01-03. Disponible en: researchgate.net
