Gases nobles: características, configuración,reacciones, usos
Los gases nobles son un conjunto de elementos que se encuentran integrando el grupo 18 de la tabla periódica. A lo largo de los años se les han llamado también gases raros o inertes, ambas denominaciones inexactas; algunos de ellos son muy abundantes fuera y dentro del planeta Tierra, y también son capaces, bajo condiciones extremas, de reaccionar.
Sus siete elementos integran quizás el grupo más singular de la tabla periódica, cuyas propiedades y escasas reactividades impresionan tanto como la de los metales nobles. Entre ellos desfilan el elemento más inerte (neón), el segundo más abundante del Cosmos (helio), y el más pesado e inestable (oganesón).

Los gases nobles son las sustancias más frías de la naturaleza; resisten temperaturas muy bajas antes de condensarse. Aún más difícil es su congelamiento, pues sus fuerzas intermoleculares basadas en la dispersión de London, y la polarizabilidad de sus átomos, son muy débiles como para apenas mantenerlos cohesionados en un cristal.
Debido a su baja reactividad, son gases relativamente seguros de almacenar y no representan demasiados riesgos. No obstante, pueden desplazar al oxígeno de los pulmones y ocasionar asfixia si se les inhalan en exceso. Por otro lado, dos de sus integrantes son elementos altamente radiactivos y, por ende, mortales para la salud.
La baja reactividad de los gases nobles se aprovecha también para proveer a las reacciones de una atmósfera inerte; de modo que ningún reactivo o producto corra el riesgo de oxidarse y afecte el rendimiento de la síntesis. Esto favorece además los procesos de soldadura por arco eléctrico.
Por otro lado, en sus estados líquidos son excelentes refrigerantes criogénicos que garantizan las más bajas temperaturas, indispensables para el correcto funcionamiento de equipos altamente energéticos, o para que algunos materiales alcancen estados de superconductividad.
Índice del artículo
- 1 Características de los gases nobles
- 2 Los 7 gases nobles
- 3 Configuración electrónica
- 4 Polarizabilidad
- 5 Reacciones
- 6 Producción
- 7 Peligros
- 8 Usos
- 9 Referencias
Quizás los gases nobles son los elementos que comparten más cualidades en común, tanto físicas como químicas. Sus características principales son:
– Todos ellos son incoloros, inodoros e insípidos; pero cuando están encerrados en ampollas a bajas presiones, y reciben una descarga eléctrica, se ionizan y despiden luces coloridas (imagen superior).
– Cada gas noble tiene su propia luz y espectro.
– Son especies monoatómicas, las únicas en la tabla periódica que pueden existir en sus respectivos estados físicos sin la participación de enlaces químicos (pues los metales se unen por enlace metálico). Por lo tanto, son perfectos para estudiar las propiedades de los gases, ya que se adaptan muy bien al modelo esférico de un gas ideal.
– Por lo general son los elementos con los menores puntos de fusión y ebullición; tanto es así, que el helio ni siquiera puede cristalizar en el cero absoluto sin un aumento de la presión.
– De todos los elementos son los menos reactivos, aún menos que los metales nobles.
– Sus energías de ionización son las más altas, así como sus electronegatividades, asumiendo que forman enlaces puramente covalentes.
– Sus radios atómicos igualmente son los más pequeños por estar en los extremos derechos de cada período.
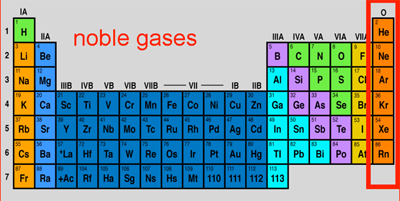
Los siete gases nobles son, de arriba hacia abajo descendiendo por el grupo 18 de la tabla periódica:
-Helio, He

-Neón, Ne

-Argón, Ar
-Kriptón, Kr
-Xenón, Xe

-Radón, Rn
-Oganesón, Og
A todos ellos, exceptuando al inestable y artificial oganesón, se les ha estudiado sus propiedades físicas y químicas. Se cree que el oganesón, debido a su gran masa atómica, ni siquiera sea un gas, sino un líquido o sólido noble. Poco se sabe del radón, a causa de su radiactividad, en relación al helio o argón.
Se ha dicho que los gases nobles tienen su capa de valencia totalmente llena. Tal es así, que sus configuraciones electrónicas se utilizan para simplificar la de otros elementos mediante el uso de sus símbolos encerrados entre corchetes ([He], [Ne], [Ar], etc.). Sus configuraciones electrónicas son:
-Helio: 1s2, [He] (2 electrones)
-Neón: 1s22s22p6, [Ne] (10 electrones)
-Argón: 1s22s22p63s23p6, [Ar] (18 electrones)
-Kriptón: 1s22s22p63s23p63d104s24p6, [Kr] (36 electrones)
-Xenón: 1s22s22p63s23p63d104s24p64d105s25p6, [Xe] (54 electrones)
-Radón: 1s22s22p63s23p63d104s24p64d104f145s25p65d106s26p6, [Rn] (86 electrones)
Lo importante no es recordarlas, sino detallar que terminan en ns2np6: el octeto de valencia. Asimismo, se aprecia que sus átomos tienen muchos electrones, los cuales a raíz de la gran fuerza nuclear efectiva se encuentran en un volumen menor comparado con el de los otros elementos; es decir, sus radios atómicos son más pequeños.
Por lo tanto, sus radios atómicos electrónicamente densos exhiben una característica química que comparten todos los gases nobles: son difíciles de polarizar.
Los gases nobles pueden imaginarse como esferas de nubes electrónicas. Mientras se desciende por el grupo 18, sus radios aumentan, y del mismo modo la distancia que separa al núcleo de los electrones de valencia (los del ns2np6).
Estos electrones al sentir una fuerza de atracción menor por parte del núcleo, se pueden mover con mayor libertad; las esferas se deforman con mayor facilidad mientras más voluminosas sean. En consecuencia de tales movimientos, aparecen regiones de baja y alta densidades electrónicas: los polos δ+ y δ-.
Cuando el átomo de un gas noble se polariza, se convierte en un dipolo instantáneo capaz de inducir otro al átomo vecino; es decir, estamos ante las fuerzas dispersivas de London.
Es por eso que las fuerzas intermoleculares aumentan desde el helio hasta el radón, reflejándose en sus crecientes puntos de ebullición; y no solo eso, sino que también se incrementan sus reactividades.
Al polarizarse más los átomos, existe mayor posibilidad de que sus electrones de valencia participen en reacciones químicas, tras lo cual se generan compuestos de gases nobles.
Entre los gases nobles los menos reactivos son el helio y el neón. De hecho, el neón es el elemento más inerte de todos, aun cuando su electronegatividad (de formar enlaces covalentes) supera a la del flúor.
No se conoce en condiciones terrestres ninguno de sus compuestos; sin embargo, en el Cosmos es bastante probable la existencia del ion molecular HeH+. Asimismo, cuando se excitan electrónicamente son capaces de interaccionar con átomos gaseosos y formar efímeras moléculas neutras llamadas excímeros; tales como HeNe, CsNe y Ne2.
Por otro lado, aunque no se consideren compuestos en un sentido formal, los átomos de He y Ne pueden dar lugar a moléculas de Van der Walls; es decir, compuestos que se mantienen “unidos” simplemente por fuerzas dispersivas. Por ejemplo: Ag3He, HeCO, HeI2, CF4Ne, Ne3Cl2 y NeBeCO3.
Igualmente, tales moléculas de Van der Walls pueden existir gracias a interacciones débiles ion-dipolo inducido; por ejemplo: Na+He8, Rb+He, Cu+Ne3 y Cu+Ne12. Nótese que es posible inclusive que estas moléculas se conviertan en aglomerados de átomos: clústeres.
Y finalmente, los átomos de He y Ne pueden quedar “atrapados” o intercalados en complejos endoédricos de fullerenos o clatratos, sin que lleguen a reaccionar; por ejemplo: [email protected]60, (N2)6Ne7, He(H2O)6 y Ne•NH4Fe(HCOO)3.
Los gases nobles argón y kriptón por ser más polarizables, tienden a presentar más “compuestos” que los de helio y neón. No obstante, una parte de ellos son más estables y caracterizables, pues tienen tiempo de vida más prolongados. Entre algunos de ellos está el HArF, y el ion molecular ArH+, presente en las nebulosas por acción de los rayos cósmicos.
A partir del kriptón comienza la posibilidad de obtenerse compuestos en condiciones extremas, pero sostenibles. Este gas reacciona con el flúor según la siguiente ecuación química:
Kr + F2 → KrF2
Nótese que el kriptón adquiere un número de oxidación de +2 (Kr2+) gracias al flúor. El KrF2 de hecho puede sintetizarse en cantidades comerciables como agente oxidante y fluorante.
El argón y kriptón pueden establecer un amplio repertorio de clatratos, complejos endoédricos, moléculas de Van der Walls, y algunos compuestos en espera de ser descubiertos posterior a su existencia predicha.
El xenón es, entre los gases nobles, el rey de la reactividad. Forma los compuestos verdaderamente estables, comerciables y caracterizables. De hecho, su reactividad se asemeja a la del oxígeno en las condiciones apropiadas.
Su primer compuesto sintetizado fue el “XePtF6”, en 1962 por Neil Bartlett. Esta sal en realidad, según la bibliografía, consistía de una mezcla compleja de otras sales fluoradas de xenón y platino.
No obstante, esto fue más que suficiente para demostrar la afinidad entre el xenón y el flúor. Entre algunos de estos compuestos tenemos: XeF2, XeF4, XeF6 y [XeF]+[PtF5]−. Cuando el XeF6 se disuelve en agua, genera un óxido:
XeF6 + 3 H2O → XeO3 + 6 HF
Este XeO3 puede originar las especies conocidas como xenatos (HXeO4–) o el ácido xénico (H2XeO4). Los xenatos se desproporcionan a perxenatos (XeO64-); y si el medio se acidifica luego, en ácido perxénico (H4XeO6), el cual se deshidrata a tetróxido de xenón (XeO4):
H4XeO6 → 2 H2O + XeO4
El radón debería de ser el más reactivo de los gases nobles; pero es tan radiactivo, que prácticamente apenas tiene tiempo de reaccionar antes de desintegrarse. Los únicos compuestos que se han plenamente sintetizado son su fluoruro (RnF2) y óxido (RnO3).
Los gases nobles se vuelven más abundantes en el Universo a medida que descendemos por el grupo 18. En la atmósfera, sin embargo, es escaso el helio, pues el campo gravitatorio de la Tierra no puede retenerlo a diferencia de otros gases. Es por eso que no se le detectó en el aire sino en el Sol.
En cambio, en el aire hay notables cantidades de argón, proveniente del decaimiento radiactivo del radioisótopo 40K. El aire es la fuente natural de argón, neón, kriptón y xenón más importante del planeta.
Para producirlos, primero el aire debe someterse a licuefacción para que condense en un líquido. Luego, a este líquido se le realiza una destilación fraccionada, separando así cada uno de los componentes de su mezcla (N2, O2, CO2, Ar, etc.).
Dependiendo de qué tan baja debe ser la temperatura y la abundancia del gas, sus precios aumentan, ubicándose el xenón como el más costoso, mientras el helio como el más barato.
El helio, por su parte, se obtiene de otra destilación fraccionada; pero no del aire, sino del gas natural, enriquecido de helio gracias a la liberación de partículas alfa de los minerales radiactivos de torio y uranio.
Asimismo, el radón “nace” del decaimiento radiactivo del radio en sus respectivos minerales; pero debido a su menor abundancia, y al tiempo corto de vida media de los átomos Rn, su abundancia es irrisoria comparada con la de sus congéneres (los otros gases nobles).
Y por último, el oganesón es un “gas” noble artificial, ultramásico y muy radiactivo, que solamente puede existir brevemente en condiciones controladas dentro de un laboratorio.
El riesgo principal de los gases nobles consiste en que limitan la utilización del oxígeno por el hombre, especialmente cuando se produce una atmósfera con alta concentración de ellos. Es por eso que no se recomienda inhalarlos en exceso.
En Estados Unidos se ha detectado una alta concentración del radón en terrenos ricos en uranio, lo cual debido a sus características radiactivas podría ser un riesgo para la salud.
El helio y el argón se usan para crear una atmósfera inerte que sirva de protección durante la soldadura y el corte. Además, se utilizan en la fabricación de semiconductores de silicio. El helio se usa como gas de relleno en termómetros.
El argón, en combinación con el nitrógeno, se usa en la elaboración de lámparas incandescentes. El kriptón mezclado con halógenos, como el bromo y el yodo, se usa en lámparas de descarga. El neón se usa en avisos luminosos, mezclado con fósforos y otros gases para matizar su color rojo.
El xenón se usa en lámparas de arco que emiten una luz que se asemeja a la luz del día, las cuales son utilizadas en los faros de automóviles y proyectores. Los gases nobles se mezclan con halógenos para producir ArF, KrF o XeCl, los cuales se utilizan en la producción de láseres excímeros.
Este tipo de láser produce una luz ultravioleta de onda corta que produce imágenes de alta precisión y se usa en la fabricación de circuitos integrados. El helio y el neón se usan como gases refrigerantes criogénicos.
El helio se usa como sustituto del nitrógeno en la mezcla de gases respiratorios, debido a su baja solubilidad en el cuerpo. Esto evita la formación de burbujas durante la fase de descompresión durante el ascenso, además de eliminarse la narcosis por nitrógeno.
El helio ha reemplazado al hidrógeno como el gas que permite la elevación de globos dirigibles y aerostáticos, debido a que es un gas ligero e incombustible.
El helio se usa en la fabricación de los imanes superconductores que se emplean en los equipos de resonancia magnética nuclear: una herramienta de aplicación múltiple en medicina.
El kriptón se usa en las lámparas de halógeno utilizadas en la cirugía ocular con láser y en la angioplastia. El helio se utiliza para facilitar la respiración en pacientes asmáticos.
El xenón se utiliza como anestésico debido a su alta solubilidad en lípidos, y se piensa que es el anestésico del futuro. También se emplea el xenón en las imágenes médicas pulmonares.
El radón, un gas noble radiactivo, se emplea en la radioterapia de algunos tipos de cáncer.
El argón se usa en la síntesis de compuestos sustituyendo al nitrógeno como atmósfera inerte. El helio se usa como gas acarreador en la cromatografía de gases, así como en los contadores Geiger para medir la radiación.
- Shiver & Atkins. (2008). Química Inorgánica. (Cuarta edición). Mc Graw Hill.
- Whitten, Davis, Peck & Stanley. (2008). Química. (8va ed.). CENGAGE Learning.
- Helmenstine, Anne Marie, Ph.D. (06 de junio de 2019). Noble Gases Properties, Uses and Sources. Recuperado de: thoughtco.com
- Wikipedia. (2019). Noble gas. Recuperado de: en.wikipedia.org
- Philip Ball. (18 de enero de 2012). Impossible chemistry: Forcing noble gases to work. Recuperado de: newscientist.com
- Professor Patricia Shapley. (2011). Noble Gas Chemistry. Recuperado de: butane.chem.uiuc.edu
- Gary J. Schrobilgen. (28 de febrero de 2019). Noble gas. Encyclopædia Britannica. Recuperado de: britannica.com
