Hormonas esteroideas: estructura, síntesis, mecanismo de acción
Las hormonas esteroideas son sustancias elaboradas por glándulas de secreción interna y que son vertidas directamente en el torrente circulatorio, el cual las conduce hasta los tejidos en donde ejercen sus efectos fisiológicos. Su nombre genérico deriva del hecho de poseer en su estructura básica un núcleo esteroideo.
El colesterol es la sustancia precursora a partir de la cual se sintetizan todas las hormonas esteroideas, las cuales se agrupan en los progestagenos (por ejemplo progesterona), los estrógenos (estrona), los andrógenos (testosterona), los glucocorticoides (cortisol), los mineralocorticoides (aldosterona) y la vitamina D.
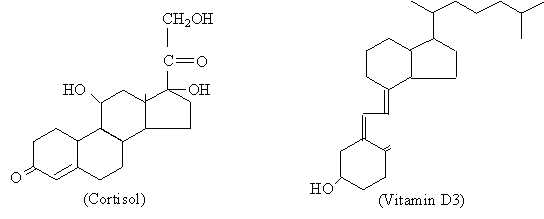
Aunque las distintas hormonas esteroideas presentan entre ellas diferencias moleculares que son las que les confieren sus distintas propiedades funcionales, puede decirse que poseen una estructura básica que les es común y que está representada por el ciclopentanoperhidrofenantreno de 17 átomos de carbono.
Índice del artículo
- 1 Estructura de los esteroides
- 2 Síntesis
- 3 Mecanismo de acción
- 4 La aldosterona como ejemplo
- 5 Referencias
Los esteroides son compuestos orgánicos de muy diversa índole que poseen en común lo que podría considerarse como un núcleo progenitor consistente en la fusión de tres anillos de seis átomos de carbono (ciclohexanos) y uno de cinco átomos de carbono (ciclopentano).
Esta estructura se conoce también como “ciclopentanoperhidrofenantreno”. Como los anillos están unidos mutuamente, el total de átomos de carbono que la conforman es de 17; sin embargo, la mayor parte de los esteroides naturales poseen en los carbonos 13 y 10 sendos grupos metilo que representan los carbonos 18 y 19, respectivamente.

Muchos de los compuestos esteroideos naturales tienen también en la estructura del anillo uno o más grupos con función alcohólica y reciben por eso el nombre de esteroles. Entre ellos está el colesterol, que tiene una función alcohol en el carbono 3 y una cadena hidrocarbonada lateral de 8 átomos de carbono unida al carbono 17; átomos que se numeran del 20 al 27.
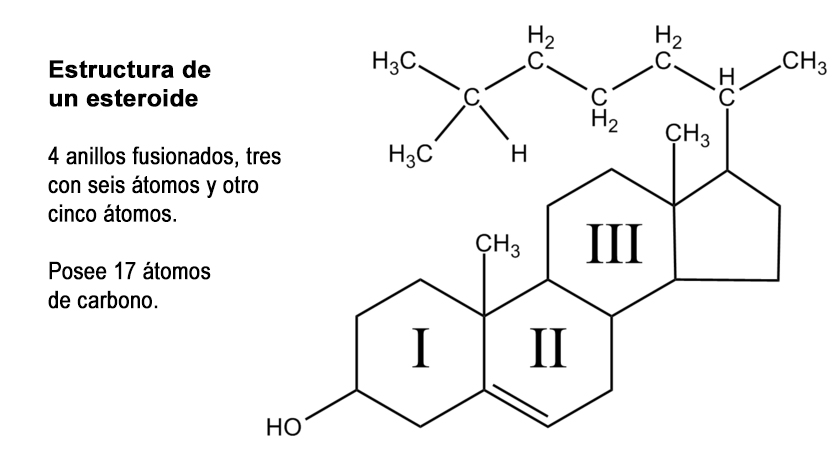
Además de estos 17 carbonos, las hormonas esteroideas pueden poseer en su estructura 1, 2 o 4 más de estos átomos, por lo cual se reconocen tres tipos de esteroides, a saber: C21, C19 y C18.
Los C21, como la progesterona y los corticoides suprarrenales (glucocorticoides y mineralocorticoides), son derivados del “pregnano”. Este posee 21 átomos de carbono porque a los 17 del anillo básico se le suman los dos de los grupos metilos de los carbonos 13 y 10, y dos carbonos de la cadena lateral unida al C17 que originalmente, en el colesterol, era de 8 carbonos.
Los C19 corresponden a hormonas sexuales con actividad androgénica y derivan del “androstano” (19 átomos de carbono), que es la estructura que queda cuando el pregnano pierde los dos carbonos de la cadena lateral del C17, la cual es sustituida por un hidroxilo o un grupo cetónico.
Los esteroides C18 son hormonas femeninas o estrógenos que se sintetizan principalmente en las gónadas femeninas y cuya característica destacada, con respecto a los otros dos tipos de esteroides, es la ausencia del metilo presente en estos últimos unido al carbono en posición 10.
Durante la síntesis a partir del colesterol se van produciendo modificaciones enzimáticas que alteran el número de carbonos y promueven deshidrogenaciones e hidroxilaciones de carbonos especificos de la estructura.
Las células productoras de hormonas esteroideas se localizan fundamentalmente en la corteza de las glándulas suprarrenales, en donde se producen glucocorticoides como el cortisol, mineralocorticoides como la aldosterona y hormonas sexuales masculinas como la dehidroepiandrosterona y la androstenediona.
Las gónadas sexuales masculinas se encargan de la producción de andrógenos que incluyen las hormonas ya citadas y la testosterona, mientras que los folículos ováricos que alcanzan la maduración producen progesterona y estrógenos.
La síntesis de todas las hormonas esteroideas se inicia a partir del colesterol. Esta molécula puede ser sintetizada por las células productoras de hormonas esteroideas, pero en su mayor parte la obtienen estas células a partir de las lipoproteínas de baja densidad (LDL) presentes en el plasma circulante.
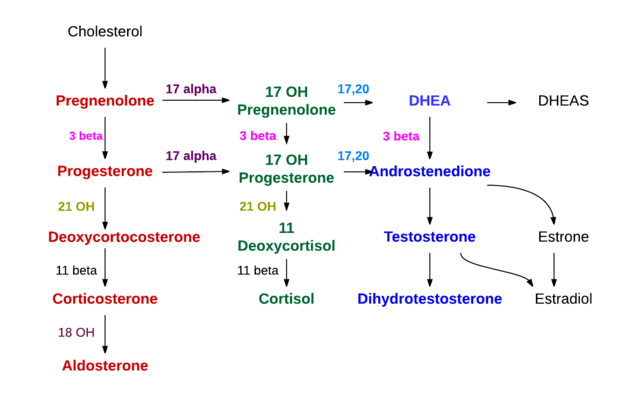
En la corteza suprarrenal se distinguen tres capas, conocidas de afuera hacia dentro como zonas glomerular, fascicular y reticular, respectivamente.
En la glomerular se sintetizan fundamentalmente mineralocorticoides (aldosterona), en la fascicular glucocorticoides como la corticosterona y el cortisol, y en la reticular andrógenos como la dehidroepiandrosterona y la androstenediona.
Síntesis de glucocorticoides
El primer paso en la síntesis se da en la mitocondria y consiste en la acción de una enzima llamada desmolasa de colesterol, perteneciente a la superfamilia del citocromo P450 y conocida también como “P450scc” o “CYP11A1”, que promueve la eliminación de 6 de los átomos de carbono de la cadena lateral unida al C17.
Con la acción de la desmolasa, el colesterol (de 27 átomos de carbono) se convierte en pregnenolona, que es un compuesto con 21 átomos de carbono y representa el primero de los esteroides del tipo C21.
La pregnenolona se desplaza al retículo endoplásmico liso, en donde por acción de la enzima deshidrogenasa de 3β-hidroxiesteroides sufre una deshidrogenación en el hidroxilo del grupo alcohol del carbono 3, y se convierte en progesterona.
Por acción de la 21β-hidroxilasa, llamada también “P450C21” o “CYP21A2”, la progesterona se hidroxila en el carbono 21 y se transforma en 11-desoxicorticosterona, que regresa a la mitocondria, y a la cual la enzima 11β-hidroxilasa (“P450C11” o “CYP11B1”) convierte en corticosterona.
Otra línea de síntesis en la zona fascicular y que termina no ya en corticosterona, sino en cortisol, se da cuando la pregnenolona o la progesterona son hidroxiladas en posición 17 por la 17α- hidroxilasa (“P450C17” o “CYP17”) y convertidas en 17-hidroxipregnenolona o 17-hidroxiprogesterona.
La misma enzima ya mencionada, deshidrogenasa de 3β-hidroxiesteroides, que convierte pregnenolona en progesterona, convierte también 17-hidroxipregnenolona en 17-hidroxiprogesterona.
Esta última es llevada sucesivamente, por las dos últimas enzimas de la vía que produce corticosterona (21β-hidroxilasa y 11β-hidroxilasa) hasta desoxicortisol y cortisol, respectivamente.
Acciones de los glucocorticoides
Los principales glucocorticoides producidos en la zona fascicular de la corteza suprarrenal son la corticosterona y el cortisol. Ambas sustancias, pero especialmente el cortisol, despliegan un amplio espectro de acciones que afectan el metabolismo, la sangre, las respuestas de defensa y de curación de heridas, la mineralización ósea, el tracto digestivo, el sistema circulatorio y los pulmones.
En cuanto al metabolismo, el cortisol estimula la lipólisis y la liberación de ácidos grasos que pueden ser utilizados en el hígado para la formación de cuerpos cetónicos y proteínas de baja densidad (LDL); disminuye la captación de glucosa y la lipogénesis en el tejido adiposo y la captación y utilización de glucosa en el músculo.
Promueve también el catabolismo proteico en la periferia: en el tejido conector, el músculo y la matriz ósea, con lo cual se liberan aminoácidos que pueden ser utilizados en el hígado para la síntesis de proteínas plasmáticas y para la gluconeogénesis. Estimula adicionalmente la absorción intestinal de glucosa aumentando la producción de transportadores SGLT1.
La absorción intestinal acelerada de glucosa, la producción hepática aumentada y la utilización disminuida de este carbohidrato en músculo y tejido adiposo favorece una elevación de los niveles plasmáticos de glucosa.
En cuanto a la sangre, el cortisol favorece el proceso de coagulación, estimula la formación de granulocitos neutrófilos e inhibe la de eosinófilos, basófilos, monocitos y linfocitos T. Inhibe también la liberación de mediadores de la inflamación como prostaglandinas, interleuquinas, linfoquinas, histamina y serotonina.
En líneas generales puede decirse que los glucocorticoides interfieren con la respuesta inmune, por lo cual pueden ser utilizados terapéuticamente en aquellos casos en los cuales esta respuesta es exagerada o inapropiada, como en el caso de las enfermedades autoinmunes o en los trasplantes de órganos para disminuir el rechazo.
La síntesis androgénica a nivel de la corteza suprarrenal se da principalmente a nivel de la zona reticular y a partir de la 17-hidroxipregnenolona y la 17-hidroxiprogesterona.
La misma enzima 17α- hidroxilasa, que produce las dos sustancias recién citadas, tiene también actividad 17,20 liasa, que suprime los dos carbonos de la cadena lateral del C17 y los sustituye por un grupo ceto (=O).
Esta última acción reduce en dos el número de carbonos y produce esteroides del tipo C19. Si la acción se da sobre la 17- hidroxipregnenolona, el resultado es dehidroepiandrosterona; si por el contrario la sustancia afectada es la hidroxiprogesterona, entonces el producto será la androstenediona.
Ambos compuestos forman parte de los llamados 17-cetosteroides, pues tienen un grupo cetónico en el carbono 17.
La deshidrogenasa de 3β-hidroxiesteroides convierte también dehidroepiandrosterona en androstenediona, pero lo más común es que la primera sea convertida en sulfato de dehidroepiandrosterona por una sulfocinasa, presente casi exclusivamente en la zona reticular.
Síntesis de mineralocorticoides (aldosterona)
La zona glomerular carece de la enzima 17α- hidroxilasa, y no puede sintetizar los 17-hidroxiesteroides precursores del cortisol y de las hormonas sexuales. Tampoco posee la 11β-hidroxilasa, pero sí una enzima llamada sintetasa de aldosterona que puede producir secuencialmente corticosterona, 18-hidroxicorticosterona y el mineralocorticoide aldosterona.
Acciones de los mineralocorticoides
El mineralocorticoide más importante es la aldosterona sintetizada en la zona glomerular de la corteza suprarrenal, pero los glucocorticoides despliegan también actividad mineralocorticoide.
La actividad mineralocorticoide de la aldosterona se desarrolla a nivel del epitelio tubular de la nefrona distal, en donde promueve la reabsorción de sodio (Na+) y la secreción de potasio (K+), contribuyendo así a la conservación de los niveles de estos iones en los líquidos corporales.
La síntesis testicular de andrógenos se produce a nivel de las células de Leydig. La testosterona es la principal hormona androgénica producida en los testículos. Su síntesis implica la producción inicial de androstenediona tal y como fue descrita previamente para la síntesis de andrógenos a nivel de la corteza suprarrenal.
La androstenediona es convertida en testosterona por acción de la enzima 17β- hidroxiesteroide deshidrogenasa, que sustituye el grupo cetónico del carbono 17 por un grupo hidroxilo (OH).
En algunos tejidos que sirven de objetivo para la testosterona, esta es reducida por una 5α-reductasa a dihidrotestosterona, con mayor poder androgénico.
Esta síntesis ocurre de manera cíclica acompañando a los cambios que se dan durante el ciclo sexual femenino. La síntesis se da en el folículo que durante cada ciclo madura para liberar un óvulo y producir luego el cuerpo lúteo correspondiente.
Los estrógenos se sintetizan en las células granulosas del folículo maduro. El folículo maduro posee unas células en su teca que producen andrógenos como la androstenediona y la testosterona.
Estas hormonas difunden a las células granulosas vecinas, las cuales poseen la enzima aromatasa que las convierte en estrona (E1) y 17β-estradiol (E2). A partir de ambos se sintetiza estriol.
Acciones de los esteroides sexuales
Los andrógenos y los estrógenos tienen como función principal el desarrollo de los caracteres sexuales masculinos y femeninos respectivamente. Los andrógenos tienen efectos anabolizantes promoviendo la síntesis de proteínas estructurales, mientras que los estrógenos favorecen el proceso de osificación.
Los estrógenos y la progesterona liberados durante el ciclo sexual femenino tienen como objetivo el preparar el organismo de la mujer para un eventual embarazo producto de la fecundación del óvulo maduro liberado durante la ovulación.
Si necesitas refrescar la memoria sobre el mecanismo de acción de las hormonas, se recomienda visualizar el siguiente video antes de seguir leyendo.
El mecanismo de acción de las hormonas esteroideas es bastante similar en todas ellas. Tratándose de compuestos lipofílicos se disuelven sin dificultad en la membrana lipídica y penetran al citoplasma de sus células blanco, las cuales poseen receptores citoplasmáticos específicos para la hormona a la cual deben responder.
Una vez formado el complejo hormona-receptor, este atraviesa la membrana nuclear y se une en el genoma, a la manera de un factor de transcripción, con un elemento de respuesta a la hormona (HRE) o gen de respuesta primaria, que a su vez puede regular a otros genes llamados de respuesta secundaria.
El resultado final es la promoción de la transcripción y la síntesis de RNA mensajeros que son traducidos en los ribosomas del retículo endoplásmico rugoso que terminan sintetizando las proteínas inducidas por la hormona.
La acción de la aldosterona se ejerce fundamentalmente a nivel de la porción final del tubo distal y en los conductos colectores, en donde la hormona promueve la reabsorción de Na+ y la secreción de K+.
En la membrana luminal de las células tubulares principales de esta región existen canales epiteliales de Na+ y canales de K+ de tipo “ROMK” (del inglés Renal Outer Medullary potassium Channel).
La membrana basolateral posee bombas Na+/K+ ATPasas que sacan continuamente Na+ desde la célula hacia el espacio intersticial basolateral e introducen K+ al interior de la célula. Esta actividad mantiene muy baja la concentración intracelular de Na+ y favorece la creación de un gradiente de concentración para este ión entre la luz del túbulo y la célula.
Dicho gradiente permite que el Na+ se mueva hacia la célula por el canal epitelial, y como el Na+ pasa solo, por cada ión que se mueva queda una carga negativa no compensada que hace que la luz del túbulo se haga negativa con respecto al intersticio. Es decir, se crea una diferencia de potencial transepitelial con la luz negativa.
Esta negatividad de la luz favorece la salida de K+ que movido por su mayor concentración en la célula y la negatividad de la luz es secretado hacia la luz del túbulo para ser finalmente excretado. Es esta actividad de reabsorción de Na+ y secreción de K+ la que es regulada por la acción de la aldosterona.
La aldosterona presente en sangre y liberada desde la zona glomerular como respuesta a la acción de la angiotensina II, o a una hiperpotasemia, penetra en el interior de las células principales y se une con su receptor intracitoplasmático.
Este complejo alcanza el núcleo y promueve la transcripción de los genes cuya expresión terminará aumentando la síntesis y la actividad de las bombas Na+/K+, de los canales de Na+ epiteliales y de los canales ROMK de K+, así como otras proteínas más. Respuesta que tendrá como efecto global la retención de Na+ en el organismo y el incremento en la excreción urinaria de K+.
- Ganong WF: The Adrenal Medulla & Adrenal Cortex, 25th ed. New York, McGraw-Hill Education, 2016.
- Guyton AC, Hall JE: Adrenocortical Hormones, in Textbook of Medical Physiology , 13th ed, AC Guyton, JE Hall (eds). Philadelphia, Elsevier Inc., 2016.
- Lang F, Verrey F: Hormone, in Physiologie des Menschen mit Pathophysiologie, 31 th ed, RF Schmidt et al (eds). Heidelberg, Springer Medizin Verlag, 2010.
- Voigt K: Endokrines System, In: Physiologie, 6th ed; R Klinke et al (eds). Stuttgart, Georg Thieme Verlag, 2010.
- Widmaier EP, Raph H and Strang KT: Female Reproductive Physiology, in Vander’s Human Physiology: The Mechanisms of Body Function, 13th ed; EP Widmaier et al (eds). New York, McGraw-Hill, 2014.
