Definición de electroquímica
La electroquímica es la rama de la fisicoquímica centrada en las leyes que se refieren a la generación de electricidad mediante combinaciones de tipo químico. La fisicoquímica, en tanto, es la ciencia que analiza los vínculos entre las propiedades químicas y las propiedades físicas de una materia.
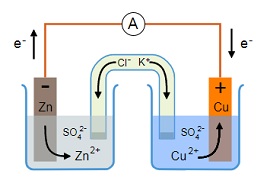 Una de las finalidades de la electroquímica es conocer las reacciones químicas que se producen en la interfaz de un electrodo y un electrolito. El electrodo es el extremo de un conductor eléctrico que está en contacto con un medio y que permite recibir o transmitir una corriente eléctrica. El electrolito, por su parte, es la sustancia sometida a la electrólisis (es decir, a un proceso de descomposición en iones provocado por la corriente).
Una de las finalidades de la electroquímica es conocer las reacciones químicas que se producen en la interfaz de un electrodo y un electrolito. El electrodo es el extremo de un conductor eléctrico que está en contacto con un medio y que permite recibir o transmitir una corriente eléctrica. El electrolito, por su parte, es la sustancia sometida a la electrólisis (es decir, a un proceso de descomposición en iones provocado por la corriente).
Cuando hay transferencia de electrones entre las moléculas que intervienen en una reacción química, se trata de una reacción de reducción-oxidación (reacción redox). Estas reacciones son claves para la producción de electricidad.
La transferencia que se genera en la reacción redox se da entre elementos oxidantes y elementos reductores. En este marco se libera energía que se transforma en electricidad.
Se llama celda electroquímica al dispositivo que parte de una reacción química para conseguir energía eléctrica o viceversa (cuando con la incorporación de energía eléctrica produce una reacción química). Una celda voltaica o celda galvánica, en este contexto, es un tipo de celda electroquímica que adquiere energía eléctrica gracias a las reacciones redox espontáneas que se producen en su interior.
Las pilas son celdas voltaicas simples. Las baterías eléctricas, a su vez, se componen de varias celdas voltaicas conectadas en paralelo o en serie.
