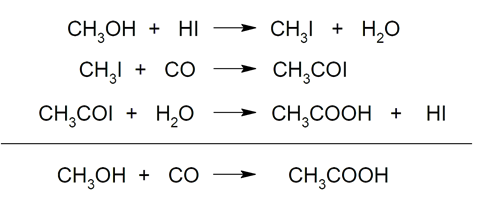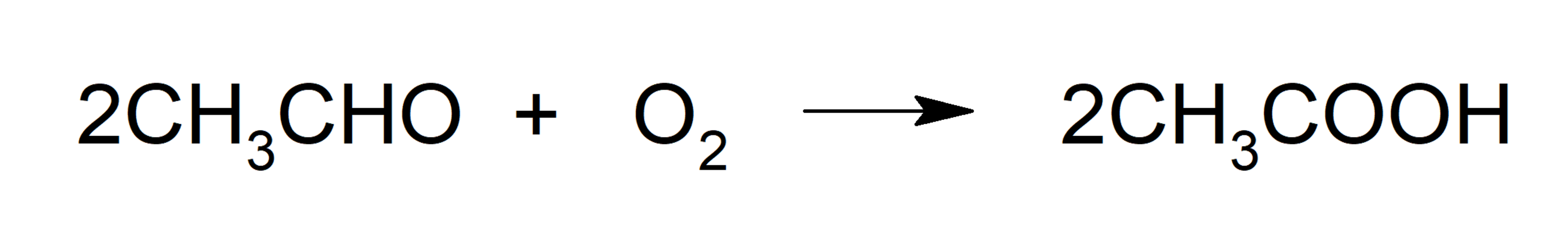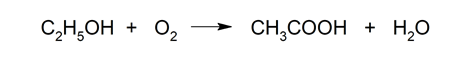Ácido acético
Te explicamos qué es el ácido acético y la fórmula de esta sustancia. Además, sus propiedades físicas, químicas y sus diferentes usos.

¿Qué es el ácido acético?
El ácido acético, también llamado ácido metilcarboxílico o ácido etanoico, es una sustancia orgánica presente en la composición del vinagre, responsable de su típico olor y sabor agrio.
Es un ácido débil, frecuente en diversos procesos de fermentación como los que tienen lugar en el vino (cuando se avinagra) o en ciertas frutas. Se lo emplea ordinariamente en la cocina, como limpiador de vegetales o aderezo de ensaladas (como vinagre, es decir, diluido con agua en un 3 a 5 % de soluto). En proporciones puras puede ser riesgoso para la salud.
Ver además: Ácido sulfúrico
Fórmula del ácido acético
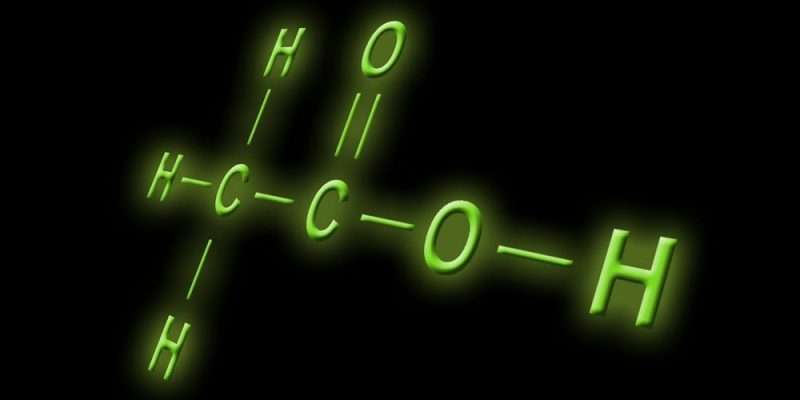
El ácido acético responde a la fórmula química C2H4O2, y su fórmula semidesarrollada es CH3COOH.
Visto así, no es más que un grupo metilo (CH3-) con un grupo carboxilo (-COOH) enlazados por un enlace simple entre sus átomos de carbono.
Propiedades físicas del ácido acético
La apariencia del ácido acético es cristalina, al menos cuando se lo encuentra como su ion acetato (una sal o éster del ácido). Posee un punto de fusión de 16,6 ºC y un punto de ebullición de 117,9 ºC, gracias al cual es posible separarlo del agua mediante destilación. Tiene además una densidad de 1049 kg/m³ y una acidez moderada de 4,8 pKa.
Es un material inflamable y corrosivo a la vez, lo cual hace delicado su manejo, pues es capaz de irritar gravemente la piel, los ojos, y el tracto digestivo (por ingestión) o respiratorio (por inhalación).
Propiedades químicas del ácido acético
El ácido acético pertenece a los ácidos carboxílicos (caracterizados por la presencia de un grupo químico funcional carboxilo: -COOH), y se lo suele ubicar en las clasificaciones entre el ácido fórmico o metanoico (que posee un único átomo de carbono) y el ácido propanoico (que posee ya una cadena de tres átomos de carbono).
Se trata de un ácido débil, común como metabolito biológico y como sustrato de las enzimas acetiltransferasas. Se lo suele obtener mediante cuatro métodos distintos:
- Carbonilación del metanol. Reacción del metanol con el monóxido de carbono, utilizando yodometano y un catalizador.
![]()
- Oxidación del acetaldehído. Oxidación del acetaldehído por el oxígeno utilizando catalizadores.
![]()
- Fermentación oxidativa. Fermentación producida por bacterias del género acetobacter (bacterias que pueden convertir el etanol en ácido acético en un entorno con aire).
![]()
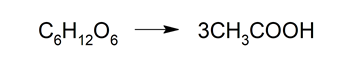
- Fermentación anaeróbica. Algunas bacterias anaerobias (que no utilizan O2 para realizar su metabolismo) producen ácido acético a partir de azúcares.
![]()
Aplicaciones y usos

El ácido acético tiene numerosas aplicaciones en la industria:
- Control de las polillas de la cera (galleriosis) en la apicultura.
- Componente importante (en sales o ésteres) para la fabricación de nailon, rayón, celofán y otros filmes.
- Componente de sustancias fijadoras en la preservación de tejidos orgánicos en laboratorio.
- Parte de los químicos empleados en el revelado fotográfico.
- Tinte médico para revelar las lesiones del Virus del Papiloma Humano (VPH).
- Componente de limpiadores y desmanchadores de uso general.
- Usos culinarios (vinagre).