Papila renal: características, histología, funciones
Las papilas renales son las estructuras anatómicas del parénquima renal en donde se completa el procesamiento del líquido tubular filtrado en los glomérulos. El líquido que abandona las papilas y entra a los cálices menores es la orina final, que se conducirá sin modificaciones hasta la vejiga urinaria.
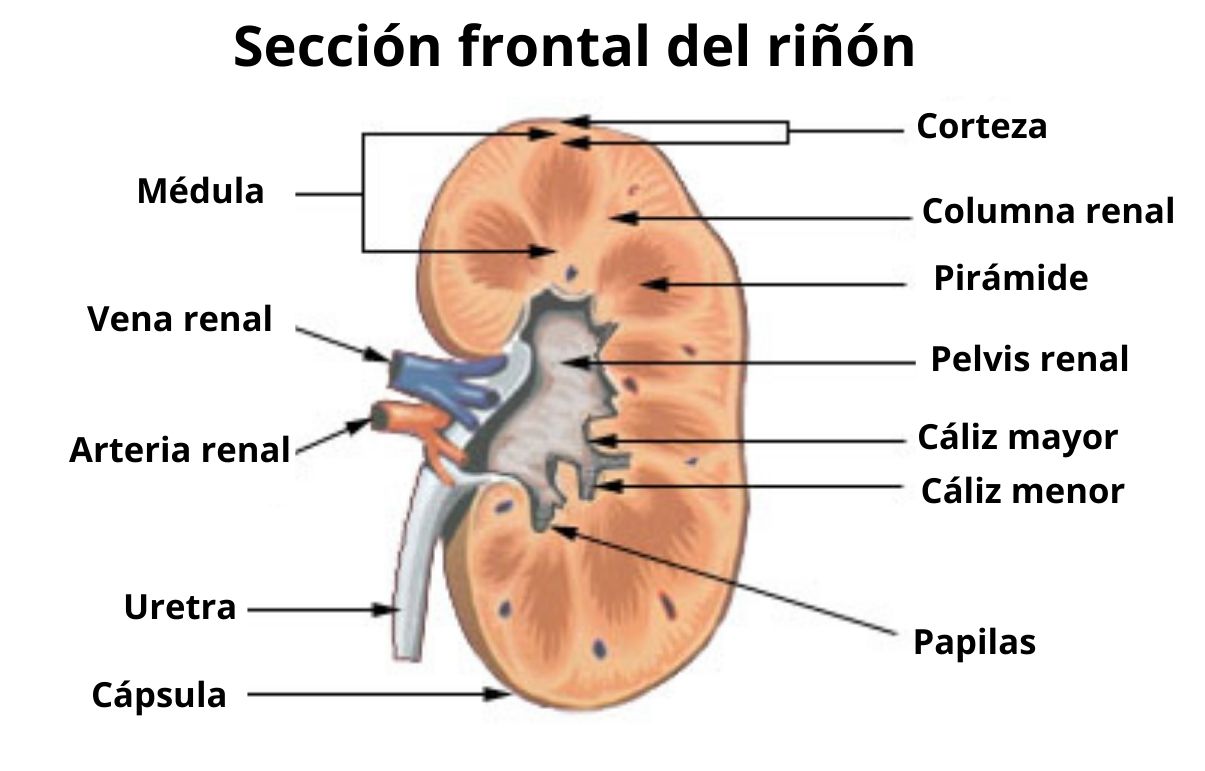
Como las papilas forman parte del parénquima renal, es necesario conocer cómo se organiza este último. Un corte del riñón a lo largo de su eje mayor permite reconocer dos bandas: una superficial -llamada corteza y otra más profunda conocida como médula, de la cual forman parte las papilas.

Dentro mismo de la corteza un par de miles de estos conductos conectores (nefronas) desembocan en un conducto más grueso llamado colector cortical, que se dirige radialmente en profundidad y se introduce en la médula renal. Este conducto con las nefronas que recibe es un lobulillo renal.
La médula renal no es una capa continua, sino que se organiza como en masas de tejido en forma de pirámides o conos cuyas bases anchas se orientan hacia fuera, hacia la corteza, con la cual limitan, mientras que sus vértices apuntan radialmente hacia dentro introduciéndose en los cálices menores.
Cada una de estas pirámides medulares representa un lóbulo renal y recibe los conductos colectores de cientos de lobulillos. La porción más superficial o externa de cada pirámide (1/3) recibe el nombre de médula externa; la más profunda (2/3) es la médula interna y en ella se incluye la región papilar.
Índice del artículo
Los componentes más importantes de las papilas son los conductos papilares de Bellini que le dan los toques finales al líquido tubular que reciben. Al finalizar su trayecto por los conductos papilares este líquido, convertido ya en orina, se vierte en un cáliz menor y no sufre más modificaciones.
Los conductos papilares, relativamente gruesos, son las porciones terminales del sistema tubular renal y se forman por la unión sucesiva de unos siete conductos colectores, de los que al dejar la corteza y adentrarse en las pirámides, han pasado de corticales a medulares.
Los agujeros de desembocadura de los varios conductos de Bellini de una papila le brindan a su recubrimiento mucoso un aspecto de lámina perforada, por lo que se le conoce con el nombre de lámina cribosa. A través de esa lámina cribosa se vierte la orina al cáliz.
Además de los conductos de Bellini, también se encuentran en las papilas los extremos de las asas de Henle largas, integrantes de aquellas nefronas cuyos glomérulos se ubican en la corteza que limita inmediatamente con la médula. Nefronas llamadas por eso yuxtamedulares.
Otro componente adicional de las papilas son los llamados vasos rectos, que se originan en las arteriolas eferentes de las nefronas yuxtamedulares y descienden rectamente hacia el extremo de las papilas, para luego subir de nuevo rectamente hasta la corteza.
Tanto las asas de Henle largas, como los vasos rectos, son conductos cuyos segmentos iniciales descienden hasta las papilas, y allí se curvan para volver a la corteza siguiendo un trayecto ascendente paralelo al descendente. El flujo por ambos segmentos se dice que es en contracorriente.
Aparte de los elementos citados, se describe también la presencia en las papilas de un conjunto de células sin una organización histológica precisa y a las que se da el nombre de células intersticiales, de función desconocida, pero que pudieran ser precursoras en procesos de regeneración tisular.
Una de las características más resaltantes de la médula renal y que alcanza su máxima expresión en las papilas, es la existencia de un gradiente hiperosmolar en el líquido intersticial que baña a los elementos estructurales descritos.
Es de hacer notar que los líquidos corporales se encuentran por lo general en equilibrio osmolar, y es ese equilibrio el que determina la distribución del agua en los distintos compartimentos. La osmolaridad intersticial, por ejemplo, es la misma en toda la corteza renal e igual a la del plasma.
En el intersticio de la médula renal, curiosamente, tratándose de un mismo compartimiento, la osmolaridad no es homogénea, sino que va aumentando progresivamente desde unos 300 mosmol/l cerca de la corteza, hasta un valor, en la papila humana, de alrededor de unos 1200 mosmol/l.
La producción y la conservación de este gradiente hiperosmolar es, en gran parte, el resultado de la organización en contracorriente ya descrita para las asas y los vasos rectos. Las asas contribuyen a conformar un mecanismo multiplicador en contracorriente que crea el gradiente.
Si la organización vascular fuese como la de cualquier otro tejido, este gradiente se disiparía porque la corriente sanguínea se llevaría los solutos. Los vasos rectos aportan un mecanismo intercambiador en contracorriente que previene ese lavado y ayuda a conservar el gradiente.
La existencia del gradiente hiperosmolar es una característica fundamental que, como se verá más adelante, se añade a otros aspectos que permiten la producción de orinas con osmolaridades y volúmenes variables ajustados a las necesidades fisiológicas impuestas por las circunstancias.
Una de las funciones de las papilas consiste en contribuir a la formación del gradiente hiperosmolar y determinar la osmolaridad máxima que se puede alcanzar en su intersticio. Muy ligada a esta función está también la de contribuir a determinar el volumen urinario y la osmolaridad del mismo.
Ambas funciones están asociadas al grado de permeabilidad que los conductos papilares ofrezcan a la urea y al agua; permeabilidad que está asociada a la presencia y a los niveles plasmáticos de la hormona antidiurética (ADH) o vasopresina.
A nivel del intersticio papilar, la mitad de la concentración osmolar es de ClNa (600 mosmol/l) y la otra mitad corresponde a la urea (600 mosmol/l). La concentración de urea en este sitio depende de la cantidad de esta sustancia que logre atravesar la pared del conducto papilar hacia el intersticio.
Esto se logra porque la concentración de urea incrementa en los conductos colectores a medida que el agua se reabsorbe, de manera que cuando el líquido llega a los conductos papilares su concentración es tan alta que si la pared lo permite difunde por gradiente químico al intersticio.
Si no hay ADH, la pared es impermeable a la urea. En este caso, su concentración intersticial es baja y la hiperosmolaridad también lo es. La ADH promueve la inserción de transportadores de urea que facilitan la salida de esta y su incremento en el intersticio. La hiperosmolaridad es entonces más alta.
La hiperosmolaridad intersticial es muy importante, porque ella representa la fuerza osmótica que permitirá la reabsorción del agua que está circulando por los conductos colectores y papilares. El agua que no se reabsorba en estos segmentos finales será excretada finalmente en forma de orina.
Pero para que el agua pueda atravesar la pared de los conductos y reabsorberse hacia el intersticio se requiere la presencia de aquaporinas que se producen en las células del epitelio tubular y se insertan en su membrana por acción de la hormona antidiurética.
Los conductos papilares, pues, trabajando en conjunción con La ADH, contribuyen a la hiperosmolaridad de la médula y a la producción de orinas de volúmenes y osmolaridades variables. Con ADH máxima, el volumen de orina es bajo y su osmolaridad alta. Sin ADH, el volumen es alto y la osmolaridad baja.
- Ganong WF: Renal Function and Micturition, in Review of Medical Physiology, 25th ed. New York, McGraw-Hill Education, 2016.
- Guyton AC, Hall JE: The Urinary System, in Textbook of Medical Physiology, 13th ed, AC Guyton, JE Hall (eds). Philadelphia, Elsevier Inc., 2016.
- Koeppen BM and Stanton BA: Renal Transport Mechanisms: NaCl and Water reabsorption along the nephron, In: Renal Physiology 5th ed. Philadelphia, Elsevier Mosby, 2013.
- Lang F, Kurtz A: Niere, in Physiologie des Menschen mit Pathophysiologie, 31 th ed, RF Schmidt et al (eds). Heidelberg, Springer Medizin Verlag, 2010.
- Silbernagl S: Die function der nieren, in Physiologie, 6th ed; R Klinke et al (eds). Stuttgart, Georg Thieme Verlag, 2010.
