Timolftaleina: características, preparación y aplicaciones
La timolftaleína es un indicador de pH cuyo nombre científico es: 3,3-bis [4-hidroxi-2-metil-5-(1-metil) fenil]-1(3H)-isobenzofuranona y su fórmula química es C28H30O4. Se sintetiza a partir del anhídrido ftálico y del timol.
Este indicador de pH tiene propiedades muy peculiares, pues a pH extremadamente bajo es rojo intenso (pH 0). Posteriormente hay un amplio rango de pH en donde es completamente incoloro (pH 1 – 9,2), con un rango de viraje entre 9,3 a 10,5 donde puede cambiar a azul, mientras que por encima de 10,5 es azul intenso.
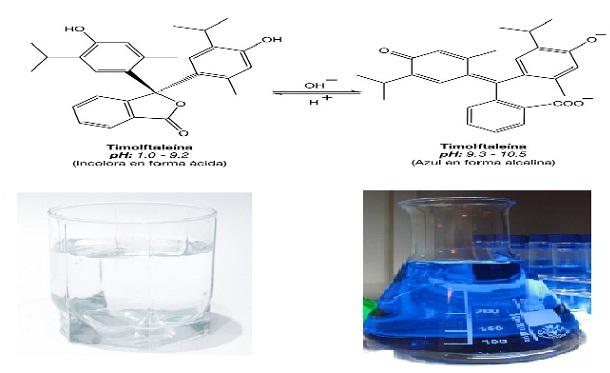
Entre sus aplicaciones está servir como indicador ácido – base en ciertas reacciones químicas. También es utilizado como cromógeno en algunas reacciones colorimétricas donde se evalúa la actividad enzimática. Por ejemplo, en la determinación de la fosfatasa alcalina.
En cuanto a la toxicidad, es menos nocivo que otros indicadores de pH, siendo clasificado por la Asociación Nacional de Protección contra el fuego (NFPA) como nivel 1 en relación a su afectación a la salud; lo cual quiere decir que no es carcinógeno ni mutagénico.
Tampoco posee una toxicidad específica contra ningún órgano diana; es decir, representa un bajo riesgo de agresión para la salud. Sin embargo, al contacto directo con piel y mucosas puede producir una leve irritación.
Por otra parte, en cuanto a inflamabilidad está clasificado como 1 y en cuanto a reactividad como cero.
Índice del artículo
El indicador de pH timolftaleína en su forma sólida es un polvo de color blanco, en su estado líquido es rojo intenso a pH menor a cero, incoloro a pH 1-9,2 y azul por encima de 10,5. Su masa molar es de 430,54 g/mol, con un punto de fusión de (258°C), en tanto que el punto de ebullición oscila entre 248-252°C. La densidad es de 0.92 g/mL a 25 °C
Es insoluble en agua fría y soluble en etanol. No es una sustancia explosiva.
A medida de precaución, durante su transporte, almacenamiento y manipulación debe mantenerse alejado de oxidantes fuertes.
Por lo general se usa el indicador de pH timolftaleína a una concentración de 0,1% para los análisis volumétricos. Para ello se debe proceder de la siguiente manera:
– Pesar 100 mg de timolftaleína y disolver en 100 ml de alcohol etílico de 95%.
También se puede preparar de la siguiente manera:
– Pesar 100 mg de timolftaleína y disolver en 60 ml de alcohol absoluto, y adicionar 40 ml de agua destilada.
– Almacenar a temperatura ambiente (15 – 25°C). Es importante que el lugar de almacenamiento esté fresco, ventilado y libre de humedad.
En la determinación de esta prueba existe una técnica que se fundamenta en la acción hidrolítica que tiene la fosfatasa alcalina sobre la timolftaleína monofosfato. Si la fosfatasa alcalina está presente, hidrolizará la timolftaleína monofosfato, liberándose la timoltaleína.
Esto produce una coloración azul en pH alcalino. La actividad enzimática de la fosfatasa alcalina es directamente proporcional a la intensidad del color formado. La absorbancia se lee a 590 nm.
En este sentido, Shao F y colaboradores en el 2018 desarrollaron una técnica colorimétrica en la que utilizan nanopartículas de sílice mesoporosas que atrapan a las moléculas de timolftaleína, las cuales se unen fuertemente por la presencia de feniltrimetiloxisilano.
A su vez, estas nanopartículas han sido recubiertas con polietilenimina (PEI), favoreciendo la unión del anticuerpo anti-PSA secundario.
Por otra parte, la muestra del paciente se ha inmovilizado en una placa; y al ponerse en contacto con las nanopartículas el PSA presente, este se unirá a los anticuerpos. Las nanopartículas que no se unan serán eliminadas.
Posteriormente, la timolftaleína se liberará fácilmente al adicionar una solución alcalina, lo cual genera una coloración azul. El grado de color es directamente proporcional a la concentración de PSA.
Usando el indicador de pH timolftaleína se puede determinar la actividad enzimática de la arginina quinasa. La prueba se fundamenta en lo siguiente:
La enzima arginina quinasa es una fosfotransferasa que participa en la formación de la fosfoarginina.¡, tal como se revela en la siguiente reacción química:
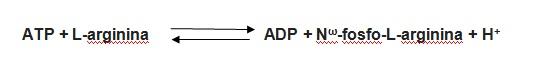
Si esta reacción se lleva a cabo frente al indicador de pH timolftaleína, es posible medir la actividad enzimática. Esto es posible de acuerdo a la siguiente explicación: la reacción ocurre en un pH alcalino, donde la timolftaleína mostrará su color azul.
La actividad enzimática se mide por el desvanecimiento del color reflejada por la disminución de la absorbancia a 575 nm, pues a medida que la enzima actúa se van liberando protones (H+), lo que acidifica el medio.
Esto hace que la timolftaleína pierda color una vez que se acerca a la zona de viraje. Si el pH llega a valores por debajo de 9,2, se vuelve completamente incolora.
Por tanto, la intensidad del color azul es inversamente proporcional a la actividad enzimática.
Este compuesto es menos tóxico que la mayoría de los indicadores de pH, ya que no se le atribuyen hasta los momentos efectos cancerígenos, ni mutagénicos. Sin embargo, no es totalmente inofensivo: al contacto con la piel y mucosas puede producir enrojecimiento de las zonas mencionadas.
También puede producir reacciones indeseables si es ingerido o inhalado de forma accidental.
En caso de que haya contacto directo con piel y mucosas, se debe lavar la zona afectada con abundante agua por lo menos durante 15 minutos. Y si observan signos de irritación, se debe acudir al centro asistencial más cercano.
Es por ello que se recomienda el uso de implementos de seguridad como bata, guantes y lentes de seguridad cuando se esté manipulando.
A pesar de tener un bajo riesgo de inflamabilidad, se recomienda que por prudencia se mantenga alejado de los mecheros.
A pesar de ser menos tóxico para la salud humana, sí es tóxico en los ambientes acuáticos, afectando a los organismos que allí se encuentran. Además, tiene un alto poder de bioacumulación, y a largo plazo es posible que se puedan formar productos de degradación dañinos para el ambiente.
Por tanto, debe evitarse que este producto llegue a aguas superficiales o subterráneas, ya que afectaría al agua potable.
En este sentido, los laboratorios que utilicen este indicador deben eliminar sus desechos cumpliendo con las regulaciones vigentes en cada país.
- Pizzani P, Godoy S, León M, Rueda E, Castañeda M, Arias A. Efecto de concentraciones crecientes de Fósforo Fítico sobre la actividad de las enzimas fitasa y fosfatasa alcalina en el epitelio intestinal de ovinos jóvenes. Rev. Cient. (Maracaibo). 2008,18 (1): 59-64. Disponible en:scielo.org.
- “Timolftaleína.” Wikipedia, La enciclopedia libre. 22 feb 2019, 04:40 UTC. 19 may 2019, 22:20, es.wikipedia.org.
- Shao F, Zhang L, Jiao L, Wang X, Miao L, Li H, Zhou F. Enzyme-Free Immunosorbent Assay of Prostate Specific Antigen Amplified by Releasing pH Indicator Molecules Entrapped in Mesoporous Silica Nanoparticles. Anal Chem. 2018; 17; 90 (14):8673-8679.
- Yu Z, Pan J, Zhou HM. A direct continuous pH-spectrophotometric assay for arginine kinase activity. Protein Pept Lett. 2002; 9(6):545-52.
- Scharlau. Ficha de seguridad de la timolftaleína. 2013. Disponible en: javeriana.edu.co
- Hoja de seguridad timolftaleína. MSDS. Universidad Nacional de Heredia, Costa Rica. Disponible en: Timolftaleína%20(3).
- “Arginina quinasa.” Wikipedia, La enciclopedia libre. 10 jul 2018, 13:49 UTC. 20 may 2019, 03:58 es.wikipedia.org.
