Alquenos: qué son, estructura, propiedades, reactividad, usos
¿Qué son los alquenos?
Los alquenos u olefinas son hidrocarburos insaturados que tienen al menos un doble enlace en su estructura. Se les denominaba olefinas por la capacidad que tiene el eteno o etileno de reaccionar con halógenos para producir aceite u óleo. Actualmente, el término de olefinas ha quedado en desuso y a estos compuestos se les denomina ahora alquenos.
Las propiedades físicas de los alquenos están influenciadas por el peso molecular de los mismos, así como también de su esqueleto carbonado. Por ejemplo, los alquenos con 2 a 4 carbonos (eteno a buteno) son gases. Con 5 a 18 átomos de carbono en la cadena larga son líquidos. Mientras que los alquenos con más de 18 átomos de carbono son sólidos.
La presencia del doble enlace les proporciona una gran reactividad, experimentando así muchas reacciones químicas, tales como adición, eliminación, hidrogenación, hidratación y polimerización, que le permiten generar numerosos usos y aplicaciones.
Los alquenos se producen industrialmente por el craqueo térmico de alcanos de alto peso molecular (ceras de parafinas); deshidrogenación catalítica y cloración-dehidrocloración.
Estructura química de los alquenos
Los alquenos se caracterizan por poseer uno o más dobles enlaces en su estructura. Este se representa como C=C, teniendo ambos átomos de carbono una hibridación sp2.
Por lo tanto, la región de la cadena donde está el doble enlace, o la insaturación, es plana. También es meritorio señalar que los dos carbonos pueden enlazarse a otros dos sustituyentes (o grupos).
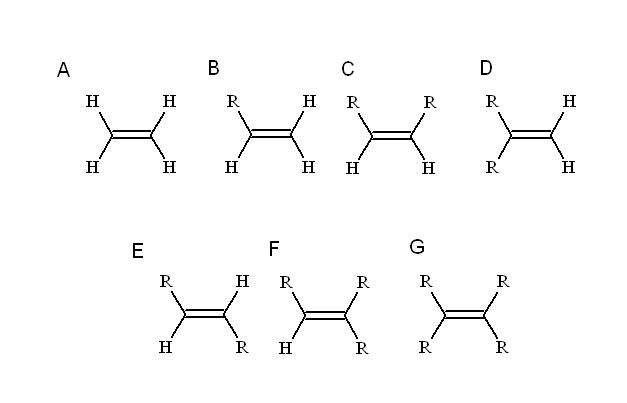
¿Cuáles sustituyentes? Cualquiera que reemplace a uno de los hidrógenos del alqueno más simple de todos: el etileno (o eteno). Partiendo de él (A, imagen superior) R, el cual es un sustituyente alquílico, ocupa el lugar de uno de los cuatro hidrógenos para originar un alqueno mono-sustituido (B).
Hasta el momento, sin importar cuál hidrógeno se sustituye, no se altera la identidad de B. Esto significa que carece de estereoisómeros, compuestos con iguales fórmulas químicas pero con una disposición espacial diferente de sus átomos.
Estereoisómeros
Cuando se sustituye un segundo hidrógeno por otro R, como ocurre en C, ahora sí surgen los estereoisómeros C, D y E. Esto se debe a que las orientaciones espaciales respecto a ambos R pueden variar, y para discernir unas de otras se recurre a las asignaciones cis-trans o E-Z.
En C, alqueno di-sustituido, los dos R pueden ser cadenas de cualquier longitud o algún heteroátomo. Uno se encuentra en posición frontal en relación con el otro. Si los dos R consisten en un mismo sustituyente, F, por ejemplo, entonces C es el estereoisómero-cis.
En D, ambos grupos R están aún más cerca, ya que están enlazados al mismo átomo de carbono. Este es el estereoisómero geminal, aunque más que un estereoisómero, es en realidad un doble enlace terminal, es decir, que está al final o principio de una cadena (por esa razón posee dos hidrógenos el otro carbono).
Y en E, el más estable de los estereoisómeros (o isómeros geométricos), los dos grupos R están separados por una distancia mayor, la cual cruza la diagonal del doble enlace. ¿Por qué es el más estable? Se debe a que como la separación espacial entre ellos es mayor, entonces no existe tensión estérica entre ambos.
Por otro lado, F y G son alquenos tri- y tetra- sustituidos respectivamente. Nuevamente, ellos no son capaces de generar ningún estereoisómero.
Propiedades físicas y químicas de los alquenos
Solubilidad
Son inmiscibles con el agua debido a su baja polaridad. Pero se disuelven en solventes orgánicos.
Puntos de fusión en ºC
Eteno -169, propeno -185, 1-penteno -165, 1-hepteno -119, 3-octeno
-101,9, 3-noneno -81,4 y 5-deceno -66,3.
Punto de ebullición en º C
Eteno -104, propeno -47, trans2buteno 0,9, cis2buteno 3,7, 1-penteno 30, 1-hepteno 115, 3-octeno 122, 3-noneno 147 y 5-deceno 170.
El punto de ebullición se incrementa en relación directa con el número de carbonos del alqueno. Por otro lado, mientras más ramificada sea su estructura, más débiles son sus interacciones intermoleculares, lo cual se refleja en el descenso del punto de ebullición o de fusión.
Densidad
Eteno 0,6128 mg/ml, propeno 0,6142 mg/ml y 1-buteno 0,6356 mg/ml, 1-penteno 0,64 mg/ml y 1-hexeno 0,673.
En los alquenos la densidad máxima es 0,80 mg/ml. Es decir, son menos densos que el agua.
Polaridad
Depende de la estructura química, sustituciones y presencia de otros grupos funcionales. Los alquenos tienen un bajo momento dipolar, así el isómero cis del 2-buteno tiene un momento dipolar de 0,33, mientras que su isómero trans tiene un momento dipolar de cero.
Reactividad de los alquenos
Los alquenos presentan gran capacidad para reaccionar debido a los dobles enlaces que poseen. Entre las reacciones en las que intervienen están: adición, eliminación, sustitución, hidrogenación, hidratación y polimerización.
Reacción de adición
H2C=CH2 + Cl2 => ClCH2-CClH2 (dicloruro de etileno)
Reacción de hidrogenación
Ocurre a temperaturas elevadas y en presencia de catalizadores adecuados (Pt, Pd, Ni finamente divididos)
CH2=CH2 + H2 => CH3-CH3 (etano)
Reacción de hidratación
Reacción que es la fuente de generación de alcoholes a partir de derivados del petróleo:
H2C=CH2 + H2O => H3C-CH2OH (alcohol etílico)
Reacciones de polimerización
El etileno en presencia de catalizadores como trialquil aluminio y tetracloruro de titanio polimeriza en polietileno, que contiene alrededor de 800 átomos de carbono. Este tipo de polímeros recibe el nombre de polímero de adición.
Usos y aplicaciones de los alquenos
Polímeros
- El polietileno de baja densidad se utiliza en la fabricación de bolsas, plásticos de invernaderos, envases, platos, vasos, etc. Mientras que el de alta densidad es más rígido y mecánicamente resistente, utilizándose en la fabricación de cajas, muebles, protectores como cascos y rodilleras, juguetes y paletas.
- El polipropileno, polímero del propileno, se usa en la elaboración de recipientes, láminas, equipos de laboratorio, juguetes, películas para empaque, filamentos para sogas, tapicería y alfombras.
- El cloruro de polivinilo (PVC) es un polímero del cloruro de vinilo que se usa en la fabricación de tubos, losetas para los pisos, canales, marcos de puertas y ventanas, etc.
- Polibutadieno, polímero del 1,3-butadieno, se destina para la fabricación de bandas de rodamiento, mangueras y cinturones de vehículos, así como para el recubrimiento de latas metálicas.
- Los copolímeros de etileno y propileno se usan en la fabricación de mangueras, carrocería y partes del chasis para autos, recubrimiento de textiles, etc.
Alquenos
- Se usan en la obtención de solventes como etilenglicol y dioxano. El etilenglicol se usa como anticongelante en los radiadores de los automóviles.
- El etileno es una hormona de las plantas que controla su crecimiento, la germinación de las semillas y el desarrollo de los frutos. Por lo tanto, se usa para inducir la maduración de los plátanos cuando estos llegan a su destino.
- Son utilizados como materia prima para la manufactura de muchos compuestos como haluros de alquilo, óxido de etileno y sobre todo el etanol. También tienen uso en la industria, en el cuidado personal y en la medicina.
- Se utilizan en la obtención y en la fabricación de lacas, detergentes, aldehídos y combustibles. 1,3-butadieno es usado como materia prima en la fabricación de cauchos sintéticos.
Referencias
- Chemistry Assignment. Physical Properties of Alkenes. Tomado de: chemistry-assignment.com
- Wikipedia. (2018). Alkene. Tomado de: en.wikipedia.org
- Chemistry LibreTexts. Physical Properties of Alkenes. Tomado de: chem.libretexts.org
- Whitten, Davis, Peck & Stanley. Química. (8va ed.). CENGAGE Learning.
- Francis A. Carey. Química Orgánica. (Sexta edición., pág 194). Mc Graw Hill.
- Houghton Mifflin Harcourt. (2016). Alkenes: Molecular and Structural Formulas. Tomado de: cliffsnotes.com
- Chipera, Angie. (25 de abril de 2017). What Is an Olefin in Chemistry? Sciencing. Tomado de: sciencing.com
