Ácido succínico: estructura, propiedades, obtención, usos
El ácido succínico es un compuesto orgánico sólido cuya fórmula química es C4H6O4. Es un ácido dicarboxílico, es decir, posee dos grupos carboxilo –COOH, uno en cada extremo de la molécula cuyo esqueleto posee 4 átomos de carbono. Se le conoce también como ácido butanodioico. Se dice que es un ácido alfa, omega-dicarboxílico o un ácido C4-dicarboxílico.
Está ampliamente distribuido en plantas, hongos y animales. Su anión succinato es un componente esencial dentro del ciclo de Krebs, el cual consta de una serie de reacciones químicas que ocurren durante la respiración celular.
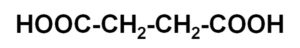
El ácido succínico es uno de los ácidos naturales que se encuentran en los alimentos, frutas como las uvas y los albaricoques, vegetales como el brócoli y la remolacha, quesos y carnes, entre muchos otros.
Se encuentra también en el ámbar amarillo o succino, de donde proviene su nombre. Puede obtenerse por destilación de esta u otras resinas. Industrialmente se obtiene mediante la hidrogenación del ácido maleico.
El ácido succínico se genera también durante la fermentación del vino. Además, es un saborizante natural muy apreciado para diversos alimentos. También se emplea como materia prima en la obtención de varios compuestos químicos que poseen aplicaciones en diversas áreas industriales, medicina y cosmética, entre muchas otras.
Índice del artículo
El ácido succínico posee 4 átomos de carbono unidos de forma lineal pero en zig-zag. Es como una molécula de butano en la cual los grupos metilo –CH3 se encuentran oxidados formando grupos carboxílicos –COOH.
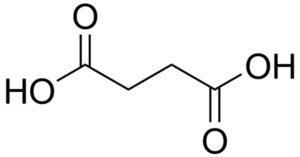
– Ácido succínico
– Ácido butanodioico
– Ácido 1,4-butanodioico
– Ácido 1,2-etanodicarboxílico
– Ácido del ámbar
– Espíritu del ámbar
Sólido cristalino incoloro a blanco, cristales triclínicos o prismas monoclínicos
118,09 g/mol
188,0 ºC
235 ºC
160 ºC (método de copa abierta).
1,572 a 25 ºC/4 ºC
1,450
En agua: 83,2 g/L a 25 ºC.
Soluble en etanol CH3CH2OH, éter etílico (CH3CH2)2O, acetona CH3COCH3 y metanol CH3OH. Insoluble en tolueno y benceno.
Una solución acuosa 0,1 molar (0,1 mol/L) tiene un pH de 2,7.
K1 = 6,4 x 10-5
K2 = 0,23 x 10-5
Los ácidos dicarboxílicos en general presentan el mismo comportamiento químico que los monocarboxílicos. Sin embargo, el carácter ácido de un ácido dicarboxílico es mayor que el de un monocarboxílico
En cuanto a la ionización de sus hidrógenos, la ionización del segundo grupo carboxílico sucede con menos facilidad que la del primero como se puede observar en las constantes de disociación del ácido succínico, donde K1 es mayor que K2.
Se disuelve en NaOH acuoso y en NaHCO3 acuoso.
El ácido succínico no es higroscópico.
Cuando se calienta desprende muy fácilmente una molécula de agua y forma el anhídrido succínico.
Por reacción de reducción (lo contrario de oxidación) el ácido succínico se convierte en 1,4-butanodiol.
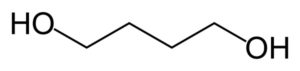
Mediante deshidrogenación del 1,4-butanodiol (eliminación de hidrógeno) se obtiene γ-butirolactona.
Cuando se realiza la ciclización del 1,4-butanodiol (formación de una molécula cíclica) se obtiene el tetrahidrofurano.
Por aminación del ácido succínico (adición de una amina) se obtienen pirrolidonas.
Su polimerización con dioles permite obtener poliésteres y con diaminas se obtienen poliamidas. Ambos son polímeros de amplio uso.
La cantidad presente en las fuentes naturales es muy pequeña por lo que industrialmente se obtiene por síntesis a partir de otros compuestos generalmente derivados del petróleo.
Se puede producir mediante la hidrogenación catalítica del ácido maleico o del anhídrido maleico.
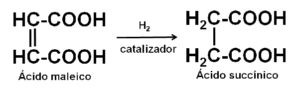
También a partir del ácido fumárico o partiendo del acetileno y del formaldehido.
Sin embargo, todos estos son procesos petroquímicos contaminantes del ambiente y dependientes del precio del petróleo. Por estas razones, desde hace tiempo se han estado desarrollando otros métodos de obtención basados en fermentación anaeróbica, los cuales son más económicos y menos contaminantes.
Estos procesos emplean CO2, lo que es beneficioso para la disminución de este gas y del efecto invernadero que genera.
Su producción puede ser fermentativa por ejemplo con Anaerobiospirillum succiniproducens y Actinobacillus succinogenes, que lo producen en altas concentraciones a partir de fuentes de carbono, como glucosa, lactosa, xilosa, arabinosa, celobiosa y otros azúcares. También utilizan el CO2 como fuente de carbono.
Hay investigadores que promueven el desarrollo del concepto de biorrefinerías, que permitiría explotar el potencial total de los recursos renovables. Tal es el caso de la utilización de efluentes de la fabricación del papel, tallos de maíz, biomasa de algas, bagazo de caña de azúcar, melaza de caña, desechos de tallos de cosechas y pulpa de remolacha para obtener ácido succínico, entre otros productos valiosos.

Por ejemplo, el empleo de la pulpa de remolacha involucra la extracción de pectina y de la parte rica en antioxidantes fenólicos, seguida de hidrólisis de la celulosa y hemicelulosa para obtener azúcares fermentables. Estos últimos son la base para obtener el ácido succínico por su fermentación anaeróbica en biorreactores.
El ácido succínico le imparte sabor de forma natural a los alimentos. Tiene efecto mejorador del sabor, por lo que en alimentos procesados es empleado como aditivo.
Se ha sugerido que tiene efectos sobre los sabores que no pueden ser duplicados por otros ácidos en los alimentos, como por ejemplo el denominado sabor umami en algunos quesos (umami es una palabra proveniente del japonés que significa “sabroso”).

Se usa incluso en alimentos para animales para su estimulación.
El ácido succínico se produce naturalmente durante la fermentación alcohólica del vino. De los ácidos no-volátiles que se generan en dicho proceso, el ácido succínico corresponde al 90% del total.

El vino contiene aproximadamente de 0,5 a 1,5 g/L de ácido succínico, pudiendo llegar a 3 g/L.
El ácido succínico es la materia prima para la obtención de productos de alto valor industrial como son el tetrahidrofurano, el 1,4-butanodiol, la gamma-butirolactona, el ácido adípico, ésteres alifáticos lineales, la N-metilpirrolidona y polímeros biodegradables.
Estos compuestos y materiales tienen numerosas aplicaciones en la industria del plástico (fibras elásticas, películas elásticas), adhesivos, disolventes industriales (remoción de pinturas y lacas), limpiadores en microelectrónica, medicina (anestésicos, vehículos de fármacos), agricultura, textiles y cosméticos.
El ácido succínico es ingrediente de algunas preparaciones farmacéuticas. Las succinimidas, derivados del ácido succínico, se emplean en medicina como anticonvulsivos.
Forma parte de fórmulas de inhibidores de corrosión, sirve como plastificante para polímeros y se utiliza en perfumería. Es además un intermediario en la síntesis de tensoactivos y detergentes.
El ácido succínico puede ser usado como monómero para la producción de polímeros y plásticos biodegradables.
Se emplea en fórmulas agrícolas para el crecimiento de plantaciones.
Las sales del ácido succínico tienen uso en los refrigerantes para vehículos y para favorecer el deshielo, siendo menos contaminantes que otros compuestos.
Los ésteres de succinato se emplean como aditivos en combustibles.
- U.S. National Library of Medicine. (2019). Succinic acid. Recuperado de: pubchem.ncbi.nlm.nih.gov
- Comuzzo, P. and Battistutta, F. (2019). Acidification and pH Control in Red Wines. In Red Wine Technology. Recuperado de sciencedirect.com.
- Alexandri, M. et al. (2019). Restructuring the conventional sugar beet industry into a novel biorefinery: Fractionation and bioconversion of sugar beet pulp into succinic acid and value-added co-products. ACS Sustainable Chemistry & Engineering. February 2019. Recuperado de pubs.acs.org.
- Methven, L. (2012). Natural food and beverage flavor enhancer. In Natural Food Additives, Ingredients and Flavourings. Recuperado de sciencedirect.com.
- Featherstone, S. (2015). Ingredients used in the preparation of canned foods. In A Complete Course in Canning and Related Processes (Fourteenth Edition). Recuperado de sciencedirect.com.
- Qureshi, N. (2009). Beneficial biofilms: wastewater and other industrial applications. In Biofilms in the Food and Beverage Industries. Recuperado de sciencedirect.com.
