Enlace Éster: Características y Tipos
Un enlace éster se define como el enlace entre un grupo alcohol (-OH) y un grupo ácido carboxílico (-COOH), formado por la eliminación de una molécula de agua (H2O) (Futura-Sciences,, S.F.).
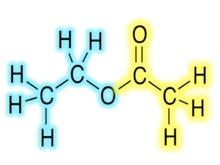
En la figura 1 se muestra la estructura del acetato de etilo. El enlace éster es aquel enlace simple que se forma entre el oxígeno del ácido carboxílico y el carbono del etanol.
R-COOH + R’-OH → R-COO-R’ + H2O
En la figura, la parte azul corresponde a la parte del compuesto que proviene del etanol y la parte amarilla la del ácido acético. Se señala el enlace éster en el círculo rojo.
Hidrólisis del enlace éster
Para entender un poco mejor la naturaleza de los enlaces éster, se explica el mecanismo de reacción de la hidrólisis de estos compuestos. El enlace éster es relativamente débil. En medio ácido o básico se hidroliza para formar respectivamente alcohol y ácido carboxílico. El mecanismo de reacción de la hidrólisis de los esteres está bien estudiado.
En medio básico, primero los hidróxidos nucleófilos atacan en el C electrofílico del éster C = O, rompiendo el enlace π y creando el intermedio tetraédrico.
Luego, el intermedio colapsa, reformando el C = O, dando como resultado la pérdida del grupo saliente, el alcóxido, RO-, que conduce al ácido carboxílico.
Por último, una reacción ácido / base es un equilibrio muy rápido donde el alcóxido, RO- funciona como una base que desprotona el ácido carboxílico, RCO2H, (un tratamiento ácido permitiría que el ácido carboxílico se obtuviera de la reacción).

El mecanismo de la hidrólisis del enlace éster en medio ácido es un poco más complicado. Primero ocurre una reacción ácido / base, dado que solo se tiene un nucleófilo débil y un electrófilo deficiente se necesita activar el éster.
La protonación del éster carbonílico lo hace más electrofílico. En el segundo paso, el óxigeno del agua funciona como el nucleófilo atacando el C electrofílico en el C = O, con los electrones moviéndose hacia el ion hidrónio, creando el intermedio tetraédrico.
En el tercer paso ocurre una reacción ácido / base desprotonandose el oxígeno que provenía de la molécula de agua para neutralizar la carga.
En el cuarto paso ocurre otra reacción ácido / base. Se necesita hacer salir el -OCH3, pero se necesita convertirlo en un buen grupo saliente por protonación.
En el quinto paso su usan los electrones de un oxígeno adyacente para ayudar a “expulsar” el grupo saliente, produciendo una molécula neutra de alcohol.
En el último paso ocurre una reacción ácido / base. La desprotonación del ion hidronio revela el carbonilo C = O en el producto de ácido carboxílico y regenera el catalizador ácido (Dr. Ian Hunt, S.F.).
Tipos de éster
Éster carbónico
Los esteres carbónicos son los más comunes de este tipo de compuestos. El primer éster carbónico fue el acetato de etilo o también llamado etanoato de etilo. Antiguamente se le conocía a este compuesto como éter de vinagre, cuyo nombre en alemán es Essig-Äther cuya contracción se derivó el nombre de este tipo de compuestos.
Los ésteres se encuentran en la naturaleza y son ampliamente utilizados en la industria. Muchos ésteres tienen olores característicos de frutas, y muchos están presentes naturalmente en los aceites esenciales de las plantas. Esto también ha llevado a su uso común en aromas artificiales y fragancias cuando los olores tratan de ser imitado.
Varios miles de millones de kilogramos de poliésteres se producen de forma industrial anualmente, productos importantes como lo son; tereftalato de polietileno, ésteres de acrilato y acetato de celulosa.
El enlace éster de los esteres carboxílicos es el responsable de la formación de triglicéridos en los organismos vivos.
Los triglicéridos se encuentran en todas las células, pero principalmente en el tejido adiposo, son la principal reserva de energía que tiene el organismo. Los triacilglicéridos (TAG) constituyen moléculas de glicerol unido a tres ácidos grasos por medio de un enlace éster. Los ácidos grasos presentes en los TAG están predominantemente saturados (Wilkosz, 2013).

Los triacilglicéridos (triglicéridos) se sintetizan prácticamente en todas las células. Los tejidos principales para la síntesis de TAG son el intestino delgado, el hígado y los adipocitos. Excepto para el intestino y los adipocitos, la síntesis TAG comienza con glicerol.
El glicerol se fosforila en primer lugar con glicerol-quinasa y después los ácidos grasos activados (acilo graso-CoAs) sirven como sustratos para la adición de ácidos grasos que generan ácido fosfatídico. El grupo fosfato se separa y se añade el último ácido graso.
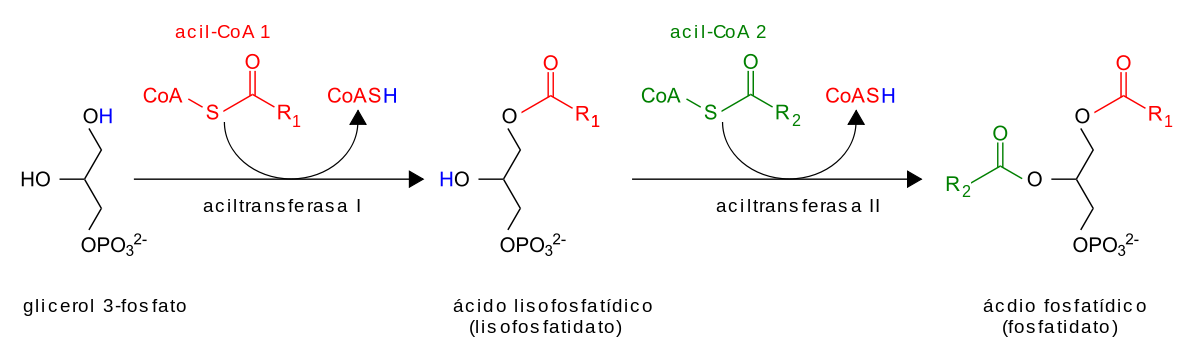
En el intestino delgado, los TAGs dietéticos se hidrolizan para liberar ácidos grasos y monoacilglicéridos (MAG) antes de la captación por los enterocitos. Los MAG de enterocitos sirven como sustratos para la acilación en un proceso de dos etapas que produce un TAG.
Dentro del tejido adiposo no hay expresión de glicerol quinasa por lo que el bloque de construcción para TAG en este tejido es el intermedio glicolítico, dihidroxiacetona fosfato, DHAP.
El DHAP se reduce a glicerol-3-fosfato por glicerol-3-fosfato deshidrogenasa citosólica y la reacción restante de síntesis de TAG es la misma que para todos los demás tejidos.
Éster fosfórico
Los ésteres fosfóricos se producen por la formación de un enlace éster entre un alcohol y el ácido fosfórico. Dada la estructura del ácido, estos ésteres pueden ser mono, di y trisustituidos.
Este tipo de enlaces éster se encuentran en compuestos como los fosfolípidos, el ATP, el ADN y ARN.
Los fosfolípidos se sintetizan por la formación de un enlace éster entre un alcohol y el fosfato de ácido fosfatídico (1,2-diacilglicerol 3-fosfato). La mayoría de los fosfolípidos tienen un ácido graso saturado sobre C-1 y un ácido graso insaturado sobre C-2 del esqueleto de glicerol.
Los alcoholes más comúnmente añadidos (serina, etanolamina y colina) también contienen nitrógeno que puede cargarse positivamente, mientras que el glicerol y el inositol no (King, 2017).

El adenosin trifosfato (ATP) es una molécula que se utiliza como moneda de la energía en la célula. Esta molécula está compuesta por una molécula de adenina unida a la molécula de ribosa con a tres grupos fosfatos (figura 8).
Los tres grupos fosfatos de la molécula se denominan gamma (γ), beta (β) y Alfa (α), este último esterifica al grupo hidroxilo C-5 de la ribosa.
El enlace entre la ribosa y el grupo α-fosforilo es un enlace fosfoéster porque incluye un átomo de carbono y un átomo de fósforo, mientras que los grupos β- y γ-fosforilo en ATP están conectados por enlaces fosfoanhídrido que no implican átomos de carbono.
Todos los fosfoanhidro tienen considerable energía potencial química, y el ATP no es una excepción. Esta energía potencial puede ser utilizada directamente en reacciones bioquímicas (ATP, 2011).
Un enlace fosfodiéster es un enlace covalente en el que un grupo fosfato se une a carbonos adyacentes a través de enlaces éster. El enlace es el resultado de una reacción de condensación entre un grupo hidroxilo de dos grupos de azúcar y un grupo de fosfato.
El enlace de diéster entre el ácido fosfórico y dos moléculas de azúcar en el ADN y el ARN esqueleto enlaza dos nucleótidos juntos para formar polímeros de oligonucleótidos. El enlace fosfodiéster enlaza un carbono 3 ‘con un carbono 5’ en el ADN y el ARN.
(base1) – (ribosa) -OH + HO-P (O) 2-O- (ribosa) – (base 2)
(base1) – (ribosa) – O – P (O) 2 – O- (ribosa) – (base 2) + H2O
Durante la reacción de dos de los grupos hidroxilo en ácido fosfórico con un grupo hidroxilo en otras dos moléculas se forman dos enlaces éster en un grupo fosfodiéster. Una reacción de condensación en la que se pierde una molécula de agua genera cada enlace éster.
Durante la polimerización de nucleótidos para formar ácidos nucleicos, el grupo hidroxilo del grupo fosfato se une al carbono 3′ de un azúcar de un nucleótido para formar un enlace éster al fosfato de otro nucleótido.
La reacción forma un enlace fosfodiéster y elimina una molécula de agua (phosphodiesther bond formation, S.F.).
Éster sulfúrico
Los ésteres sulfúricos o tioésteres son compuestos con el grupo funcional R-S-CO-R’. Son el producto de la esterificación entre un ácido carboxílico y un tiol o con el ácido sulfúrico (Block, 2016).
En bioquímica, los tioésteres más conocidos son derivados de la coenzima A, por ejemplo, acetil-CoA.
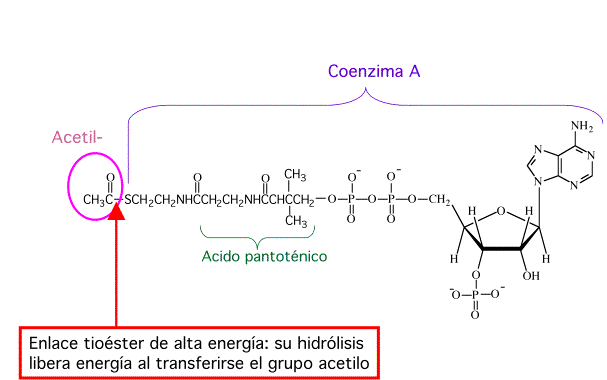
La acetil coenzima A o acetil-CoA (figura 8) es una molécula que participa en muchas reacciones bioquímicas. Es una molécula central en el metabolismo de lípidos, proteínas y carbohidratos.
Su función principal es entregar el grupo acetilo al ciclo del ácido cítrico (ciclo de Krebs) que se va a oxidar para la producción de energía. También es la molécula precursora de la síntesis de ácidos grasos y es producto de la degradación de algunos aminoácidos.
Los ácidos grasos activados con CoA mencionados anteriormente son otros ejemplos de tioesteres que se originan dentro de la célula muscular. La oxidación de los tioésteres de ácido graso-CoA ocurre realmente en cuerpos vesiculares discretos llamados mitocondrias (Thompson, 2015).
Referencias
- Organosulfur compound. Recuperado de britannica.com.
- Hydrolysis of Esters. Recuperado de chem.ucalgary.ca.
- Ester bond. Recuperado de futura-sciences.us.
