Tensión interfacial: definición, ecuación, unidades y medición
La tensión interfacial (γ) es la fuerza neta por unidad de longitud que se ejerce en la superficie de contacto entre una fase (sólida o líquida) y otra (sólida, líquida o gaseosa). La fuerza neta es vertical a la superficie de contacto y está dirigida hacia el interior de las fases.
Cuando una de las fases es un gas se le suele llamar tensión superficial. Las fases en contacto son inmiscibles, es decir, no se pueden disolver entre sí para formar una solución. La región de contacto entre las fases es una superficie geométrica de separación llamada interfase. La tensión interfacial se debe a las fuerzas intermoleculares presentes en la interfase.

La tensión interfacial juega un importante papel en muchos fenómenos y procesos interfaciales como por ejemplo en la elaboración de emulsiones y en la producción de petróleo.
Índice del artículo
- 1 Definición
- 2 Ecuación y unidades de tensión interfacial
- 3 Dependencia de la temperatura
- 4 Medición de la tensión interfacial
- 5 Referencias
Las propiedades de la interfase no son iguales a las propiedades en el interior de las fases en contacto, debido a que se manifiestan diferentes interacciones moleculares porque en esa región hay moléculas que pertenecen tanto a una fase como a la otra.
Las moléculas en el interior de una fase interactúan con moléculas vecinas, las cuales tienen propiedades similares. En consecuencia, la fuerza neta interior es nula porque las interacciones atractivas y repulsivas son iguales en todas las direcciones posibles.
Las moléculas que están en la superficie entre las dos fases están rodeadas de moléculas de una misma fase pero también de moléculas vecinas de la otra fase.
En este caso, la fuerza neta no es nula, y está dirigida hacia el interior de la fase en la cual hay mayor interacción. El resultado es que el estado de energía de las moléculas en la superficie es mayor que el estado de energía en el seno de la fase.
La fuerza neta que actúa hacia el interior por unidad de longitud a lo largo de la interfase es la tensión interfacial. Debido a esta fuerza las moléculas de forma espontánea tienden a minimizar la energía minimizando el área superficial por cada unidad de volumen.
Para atraer una molécula desde el interior hacia la superficie es necesario que las fuerzas que actúan sobre la molécula superen la fuerza neta. En otras palabras, se requiere realizar trabajo para aumentar la superficie interfacial.

Mientras mayor es la fuerza neta intermolecular mayor es el trabajo a realizar y mayor es la entrada de energía. Por esta razón la tensión interfacial también se define en función del trabajo o en función de la energía, como se menciona a continuación:
La tensión interfacial es el trabajo necesario para crear una unidad de área en la interfase. Así mismo, la tensión interfacial se define como la energía libre requerida por unidad de área creada.
La ecuación de la tensión interfacial en función de la fuerza neta intermolecular es:
γ = F/2l [1]
F = Fuerza neta
l = longitud de la interface
El número 2 que aparece en la ecuación [1] significa que hay dos superficies, una por cada cara de la interface.
La tensión interfacial en función del trabajo requerido para generar una unidad de área superficial se expresa mediante la siguiente ecuación:
γ = W/ΔA [2]
W = Trabajo
ΔA = Incremento del área superficial
La creación del área interfacial va acompañada de un incremento en la energía libre de formación.
γ = ΔE/ΔA [3]
ΔE = Energía de formación de la interface
Las unidades de tensión interfacial en el sistema internacional son N/m o Joules/m2. También suele utilizarse Dinas/cm o mN/m.
Uno de los principales factores que afectan la tensión interfacial es la temperatura. A medida que aumenta la temperatura las fuerzas de interacción disminuyen, como consecuencia de esto, la fuerza neta que contrae la superficie también disminuye causando un decrecimiento de la tensión interfacial.
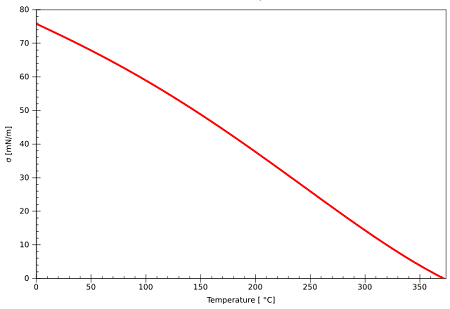
Si se sigue aumentando la temperatura, llegará un momento en que la tensión interfacial se anulará y ya no existirá ninguna superficie de separación entre las fases. La temperatura en la cual la tensión interfacial se anula se llama temperatura crítica (tc).
La razón por la cual disminuye la tensión interfacial es que al aumentar la temperatura aumenta la energía cinética por el aumento en el movimiento térmico de las moléculas.
Existen diferentes métodos de medición experimental de la tensión interfacial, entre los cuales se puede escoger el que más convenga de acuerdo a las propiedades características de las fases en contacto y de las condiciones experimentales.
Entre estos métodos se mencionan el método de la placa Wilhelmy, el método del anillo de Du Nouy, el método de la gota pendiente, y el método de la gota giratoria.
Consiste en medir la fuerza hacia abajo que ejerce la superficie de una fase líquida sobre una placa de aluminio o de vidrio. La fuerza neta ejercida sobre la placa es igual al peso más la fuerza de tensión. El peso de la placa se obtiene mediante una microbalanza sensible a la torsión unida a la placa mediante un dispositivo.
En este método se mide la fuerza para separar la superficie de un anillo metálico de una superficie líquida asegurándose que antes de medir, el anillo esté completamente sumergido en el líquido. La fuerza de separación es igual a la tensión interfacial y se mide utilizando una balanza de alta precisión.
Este método se fundamenta en medir la deformación de una gota colgando de un capilar. La gota se mantiene en equilibrio mientras está colgando debido a que la fuerza de tensión iguala el peso de la gota.
El alargamiento de la gota es proporcional al peso de la gota. El método se fundamenta en determinar la longitud de alargamiento de la gota debido a su peso.

El método de la gota giratoria es muy útil para medir tensiones interfaciales muy bajas que se aplican al proceso de producción de emulsiones y microemulsiones.
Consiste en colocar una gota de un líquido menos denso dentro de un tubo capilar lleno de otro líquido. La gota se somete a una fuerza centrifuga debida a un movimiento de rotación, con gran velocidad, que alarga la gota en el eje y se opone a la fuerza de tensión.
La tensión interfacial se obtiene a partir de las dimensiones de la forma geométrica de la gota, estando deformada, y de la velocidad de rotación.
- Tadros, T F. Applied Surfactants. Berkshire, UK : Wiley-VCH Verlag Gmbh & Co, 2005.
- van Oss, C J. Interfacial Forces in Aqueous Media. Florida , US : Taylor & Francis Group, 2006.
- Figura, L y Teixeira, A A. Food Physics: Physical Properties – Measurement and Applications. Germany : Springer, 2007.
- Anton de Salager, R E. Tensión Interfacial. Mérida : FIRP – Universidad de los Andes, 2005.
- Speight, J G. Handbook of Petroleum Product Analysis. New Jersey, US : Jhon Wiley & sons, 2015.
- Adamson, A W y Gast, A P. Physical Chemistry of Surfaces . US : John Wiley & Sons, Inc. , 1997.
- Blunt, M J. Multiphase Flow in Permeable Media: A Pore-Scale Perspective. Cambridge, UK : Cambridge University Press, 2017.
