Prueba de oxidasa: fundamento, procedimiento y usos
La prueba de oxidasa es un método diagnóstico que evidencia la presencia del complejo enzimático denominado citocromo oxidasa c. Este sistema induce la transformación del citocromo reducido a oxidado, ya que capta el oxígeno y este a su vez actúa como último aceptor de electrones (H+) en la cadena respiratoria.
El termino oxidasa es una forma resumida de hacer referencia a la enzima citocromo oxidasa, también conocida como indofenol oxidasa. En la antigüedad se creyó que las enzimas citocromo oxidasa y la indofenol oxidasa eran dos enzimas diferentes, pero hoy se sabe que son la misma.
Por su parte, los citocromos son hemoproteínas que contienen hierro y completan el sistema citocromo oxidasa. Los citocromos pueden variar de una especie a otra.
Existen distintas variedades de citocromos (citocromos a1, a2, a3 y 0). Algunas bacterias pueden producir una sola, pero otras hasta dos o tres a la vez. En este sentido, la presencia del citocromo a y a3 se conoce como citocromo – oxidasa c. Este es el tipo de citocromo que detecta la prueba de oxidasa.
Los géneros Neisseria y Pseudomonas contienen citocromo oxidasa c. Estos géneros dan la prueba de oxidasa positiva, ayudando a diferenciarlos de los géneros Acinetobacter y Stenotrophomonas respectivamente.
También existen otros géneros que son oxidasa positivos.
Índice del artículo
El sistema citocromo oxidasa c actúa de la siguiente manera: los microorganismos oxidasa positivos utilizan el oxígeno para generar energía a través de la respiración aeróbica. Este sistema funciona gracias al transporte de electrones a partir de sustancias donadoras como el NADH+ hacia sustancias receptoras, en este caso el oxígeno.
Esto da como resultado que se produzca energía (ATP) y agua o peróxido de hidrógeno, dependiendo del sistema de citocromo oxidasa que posea el microorganismo.
Es por ello que la mayoría de las bacterias oxidasa positivos también son catalasa positivas, condición necesaria para eliminar el peróxido de hidrógeno producido, ya que esta sustancia es tóxica para las bacterias.
El sistema citocromo oxidasa c está presente en algunas bacterias aerobias, ciertas anaerobias facultativas, escasas microaerofílicas y ninguna anaerobia estricta. Esto último es comprensible, ya que los anaerobios estrictos no pueden vivir en presencia del oxígeno, por tanto carecen del sistema citocromo oxidasa.
En esta prueba utiliza sustancias que actúan como aceptores artificiales de electrones, sustituyendo los naturales dentro de la cadena de transporte de electrones.
Principalmente se utilizan colorantes como el parafenilendiamina y el indofenol, que actúan como sustratos receptores y donadores de electrones artificiales.
El parafenilendiamina es oxidado por el sistema del citocromo oxidasa c. El colorante en su forma reducida es incolora, pero en su forma oxidada es coloreado.
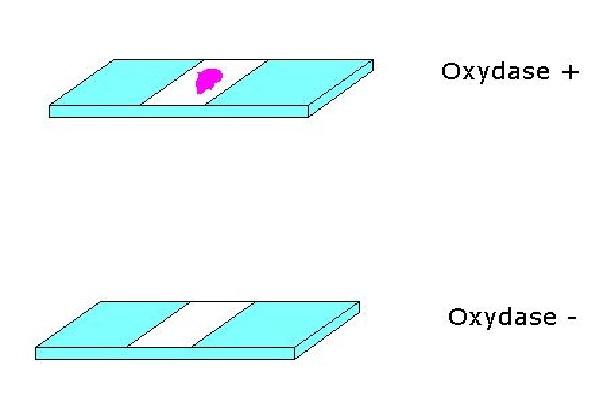
Es así como se pone en evidencia la presencia del sistema citocromo oxidasa c; pues una reacción positiva generará una coloración lavanda o azul –púrpura dependiendo del reactivo utilizado.
En cambio, si la última sustancia aceptora de electrones en la cadena respiratoria es diferente al oxígeno, la prueba de oxidasa dará negativa (no hay producción de color); este es el caso de los microorganismos anaerobios.
Así mismo, si el citocromo utilizado por el microorganismo es diferente al citocromo oxidasa c, también dará la prueba negativa.
Para la prueba de la oxidasa existen diversos reactivos y protocolos, todos con el mismo fin.
Reactivo de Kovacs, reactivo de Gordon y McLeod, reactivo de Nadi, reactivo de Carpenter, Suhrland y Morrison, y uso de discos de oxidasa.
-Reactivo de oxidasa de Kovacs
Está formado por diclorhidrato de tetrametil-p-fenilendiamina al 1%.
El reactivo de Kovacs se prepara disolviendo 1 gr de la sustancia antes mencionada en 50 ml de agua destilada. Se calienta sutilmente hasta su disolución total. Trasvasar a un frasco color ámbar de capacidad suficiente y completar el volumen a 100 ml con agua destilada. Esperar al menos 15 minutos antes de usar. Guardar en nevera protegido de la luz.
Se rotula como reactivo de oxidasa de Kovacs, para diferenciarlo del reactivo de Kovacs utilizado para revelar la prueba del indol. Este reactivo es el más sensible, menos tóxico pero más costoso que el resto de los reactivos.
Una reacción positiva se evidenciará con este reactivo con el cambio de color de la colonia a lavanda, que vira rápidamente a púrpura casi negro. Una reacción negativa se evidencia porque no hay cambio de color de la colonia o esta toma una ligera coloración rosada. El medio puede igualmente oscurecer, pero eso no significa reacción positiva.
Con este reactivo el tiempo de reacción es crucial, se considera una reacción positiva aquel cambio de color que ocurre entre 5 a 15 seg.
-Reactivo de Gordon y McLeod
Está compuesto por diclorhidrato de dimetil-p-fenilendiamina, también conocido como N-dimetil-p-fenilendiamina o monoclorhidrato de p-aminodimetilanilina. Se prepara como fue descrito para el reactivo de oxidasa de Kovacs, sustituyendo por la sustancia involucrada.
Este reactivo es ligeramente más estable que el reactivo de oxidasa de Kovacs, aunque todos los reactivos que contienen p-fenilendiamina son inestables.
Esta reacción es más tardía, se interpreta como positiva con la aparición de un color azul –púrpura dentro de 10 a 30 minutos.
-Reactivo de Nadi
Está compuesto por α-naftol al 1% en alcohol etílico (etanol al 95%) y 1% de aminodimetilanilina. La mezcla se prepara a partes iguales y utilizando alcohol etílico absoluto como diluente, hasta completar la cantidad suficiente para 100 ml.
-Reactivo de Carpenter, Suhrland y Morrison
Está compuesto por oxalato de p-aminodimetilalanina al 1%. Preparar de igual manera a la descrita para reactivo de oxidasa de Kovacs, cambiando por la sustancia correspondiente.
Con la solución lista, se preparan tiras reactivas de la siguiente manera: se impregnan tiras de papel de filtro Whatman N°1 de 6-8 cm con el reactivo de oxalato de dimetil-p-fenilendiamina al 1%.
Se dejan secar sin que tenga contacto con metal, guardar en frascos tapa de rosca con desecante y conservar en nevera. Estas tiras son estables hasta por 6 meses.
Es el reactivo más estable de todos los mencionados, pudiendo durar en solución hasta 6 meses. Otro punto a favor es que no colorea el medio alrededor de la colonia, si se usa directo sobre la placa.
La aparición de un color rojo se interpreta como una prueba positiva.
-Discos de oxidasa
Son discos comerciales que vienen impregnados con reactivo para la prueba de oxidasa. Existen diversas marcas comerciales en el mercado.
Su uso es bastante práctico, ya que no hay que preparar reactivos frescos, lo que facilita el trabajo. Los resultados obtenidos son confiables siempre y cuando los discos se conserven adecuadamente.
Método en placa directa, método indirecto sobre papel y uso de discos impregnados con reactivos de oxidasa.
-Método de la placa directa
Se adicionan 2 o 3 gotas de cualquiera de los reactivos antes mencionados para este fin directamente sobre la o las colonia (s) contenidas en una placa de medio de cultivo que no contenga glucosa.
Se interpreta el cambio o no de color de las colonias, no del medio. El tiempo de reacción válido depende del reactivo utilizado.
-Método indirecto sobre papel
Cortar un trozo de papel de filtro (Whatman N°1) a un tamaño de 6 cm2 y se coloca dentro de una placa de Petri vacía.
Adicionar 2 o 3 gotas del reactivo de oxidasa de Kovacs en el papel, tomar parte de la colonia que se quiere estudiar con un asa de platino o palillo de madera y extenderla en línea recta sobre el papel impregnado de reactivo. Interpretar en un lapso de 5 a 10 segundos.
Con las tiras preparadas con el reactivo Carpenter, Suhrland y Morrison se extiende una colonia sobre la tira seca. Una misma tira sirve para probar varias cepas. Interpretar en 10 seg.
-Discos (método directo)
Humedecer sutilmente los discos comerciales con agua destilada estéril y sobreponer sobre la colonia a estudiar. Se recomienda usar las placas a 35°C, si se usan placas a temperatura ambiente o placas refrigeradas la reacción es un poco más lenta. Interpretar el cambio de color entre 10 a 20 seg.
Se pueden usar colonias contenidas en agar sangre o chocolate.
-Discos (método indirecto)
Humedecer el disco como se describió anteriormente. Colocarlo en una placa de Petri vacía. Tomar cantidad suficiente de la colonia a estudiar con un asa de platino o palillo de madera y colocar sobre el disco. Interpretar el cambio de color entre 10 a 20 seg.
El género Neisseria y Acinetobacter en ocasiones se parecen mucho morfológicamente porque a pesar de que el género Acinetobacter es un bacilo Gram negativo, a veces puede adoptar una forma cocoide y distribuirse en pares, simulando el género Neisseria.
En este caso la prueba de oxidasa es realmente útil. El género Neisseria es positiva y Acinetobacter negativa.
Sin embargo, el género Moraxella es muy similar al género Neisseria y ambas dan reacción positiva; es por ello que siempre hay que realizar pruebas de fermentación de carbohidratos para la identificación definitiva.
Por otra parte, la prueba de oxidasa es útil para diferenciar una bacteria perteneciente a la familia Enterobacteriaceae (todos oxidasa negativa) de otros fermentadores, tales como el género Pasteurella, Aeromonas, Plesiomonas (oxidasa positivos).
El género Vibrio y Helicobacter también son oxidasa positivos.
Usar cepas conocidas de Escherichia coli como control negativo y cepas de Pseudomonas aeruginosa como control positivo.
-Los reactivos deben usarse recién preparados, su vida útil en solución a temperatura ambiente es corta por ser muy inestables. Refrigerados pueden durar entre 5 días a 2 semanas.
-Los reactivos son incoloros, si cambian de color deben ser desechados. Los discos dañados se evidencian porque se oscurecen con el tiempo.
-Una reacción positiva con el reactivo oxidasa de Kovacs entre 15 -60 seg se considera una reacción retardada y después de pasar 60 segundos se debe considerar como negativa.
-El Haemophylus influenzae da una reacción oxidasa negativa si se utiliza cualquier reactivo con dimetil-p-fenilendiamina, pero positiva si se usa el reactivo de oxidasa de Kovacs (tetrametil-p-fenilendiamina).
-Medios que contengan glucosa interfieren en la prueba, dando falsamente negativos.
-Las cepas de Bordetella pertussis pueden dar reacción falsamente positivo si provienen de placas de agar sangre muy concentradas.
-El uso de asas de metal (hierro) dan reacción falsamente positiva.
-Debido a que los reactivos son muy inestables y tienden a auto-oxidarse se recomienda congelar alícuotas de 1 a 2 ml e ir sacando conforme se va necesitando.
-Otra forma de retardar la auto-oxidacion del reactivo es adicionar ácido ascórbico al 0,1% al momento de preparar los reactivos.
-Como los reactivos son inestables se recomienda realizar un control de calidad semanalmente.
-Los reactivos que no pasen la prueba de control de calidad, no deben ser usados.
- Koneman E, Allen S, Janda W, Schreckenberger P, Winn W. (2004). Diagnóstico Microbiológico. 5ta ed. Editorial Panamericana S.A. Argentina.
- Forbes B, Sahm D, Weissfeld A. (2009). Diagnóstico Microbiológico de Bailey & Scott. 12 ed. Editorial Panamericana S.A. Argentina.
- “Prueba de la Oxidasa.” Wikipedia, La enciclopedia libre. 15 ene 2018, 10:32 UTC. 3 abr 2019, 14:03
- Organización Mundial de la Salud. Manual de Laboratorio para la Identificación y Prueba de Susceptibilidad a los Antimicrobianos de Patógenos Bacterianos de Importancia para la Salud Pública en el Mundo en Desarrollo.2004. Disponible en: who.int/drugresistance/infosharing
- Tiras reactivas para el diagnóstico de actividad oxidasa en las bacterias. Rev Cubana Med Trop [Internet]. 2000; 52( 2 ): 150-151.
