Quinonas: qué son, propiedades, clasificación, obtención, reacciones, usos
¿Qué son las quinonas?
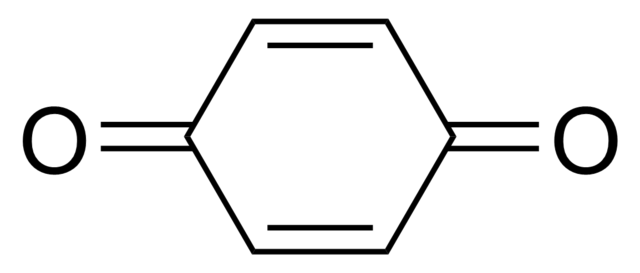
Las quinonas son compuestos orgánicos con una base aromática como el benceno, el naftaleno, el antraceno y el fenantreno. Sin embargo, se consideran moléculas cíclicas diacetónicas conjugadas. Derivan de la oxidación de los fenoles, y, por lo tanto, los grupos C–OH se oxidan a C=O.
Por lo general, son compuestos coloreados que cumplen funciones de tintes y colorantes. Sirven de base para la elaboración de numerosos medicamentos.
Uno de los derivados de la 1,4-benzoquinona (imagen superior) es constituyente de la ubiquinona o coenzima Q, presente en todos los seres vivos, de allí su nombre de “ubicuo”.
Esta coenzima interviene en el funcionamiento de la cadena de transporte electrónico. El proceso ocurre en la membrana interna mitocondrial, y está acoplada a la fosforilación oxidativa, en la cual se produce ATP, principal fuente energética para los seres vivos.
Las quinonas se encuentran en la naturaleza en forma de pigmentos, en plantas y animales. Asimismo, están presentes en muchas hierbas que se usan tradicionalmente en China, como el ruibarbo, cassia, sen, consuelda, nudillo gigante, poligonum y aloe vera.
Las quinonas que emplean los grupos fenólicos como auxocromos (las hidroxi quinonas), presentan una variedad de colores como el amarillo, el naranja, el marrón rojizo, el púrpura, etc.
Propiedades físicas y químicas de las quinonas
A continuación se describen las propiedades físicas y químicas de la 1,4-benzoquinona. Sin embargo, dada la semejanza estructural que existe entre todas las quinonas, se pueden extrapolar estas propiedades a otras conociendo sus diferencias estructurales.
Aspecto físico
Sólido cristalino de color amarillento.
Olor
Picante irritante.
Punto de ebullición
293 °C.
Punto de fusión
115.7 °C (240.3 °F). Por lo tanto, las quinonas con mayores masas moleculares son sólidos con puntos de fusión más altos que 115.7 °C.
Sublimación
Puede sublimar aún a temperatura ambiente.
Solubilidad
Mayor que el 10% en éter y en etanol.
Solubilidad en agua
11.1 mg/mL a 18 °C. Las quinonas en general son muy solubles en agua y solventes polares por su capacidad de aceptar puentes de hidrógeno (pese al componente hidrofóbico de sus anillos).
Densidad
3.7 (con relación al aire tomado como 1).
Presión de vapor
0.1 mm Hg a 77 °C (25 °C).
Autoignición
1040 °F (560 °C).
Calor de combustión
656.6 kcal/g. mol.
Olor (umbral)
0.4 m/m3.
Clasificación de las quinonas
Hay tres grupos principales de quinonas: las benzoquinonas (1,4-benzoquinona y la 1,2-benzoquinona), las naftoquinonas y las antraquinonas.
Benzoquinonas
Todas ellas tienen en común un anillo bencénico con grupos C=O. Ejemplos de benzoquinonas son: embelina, rapanona y primina.
Naftoquinonas
La base estructural de las naftoquinonas, como su nombre lo indica, es el anillo nafténico, es decir, derivan del naftaleno. Ejemplos de naftoquinonas son: plumbagina, lawsona, juglona y lapachol.
Antraquinonas
Las antraquinonas se caracterizan por tener como base estructural el anillo antracénico, es decir, un conjunto de tres anillos bencénicos enlazados por sus laterales. Ejemplos de antraquinonas son: barbaloina, alizarina y crisofanol.
Obtención
Benzoquinona
– La benzoquinona se puede obtener mediante la oxidación de 1,4-dihidrobenceno con clorato de sodio, en presencia de pentóxido de divanadio como catalizador, y ácido sulfúrico como disolvente.
– También se obtiene por la oxidación de la anilina con dióxido de manganeso o cromato, como oxidantes en una disolución ácida.
– Se produce benzoquinona por los procesos de oxidación de la hidroquinona, por ejemplo, en la reacción de la benzoquinona con peróxido de hidrógeno.
Naftoquinona
– La naftoquinona se sintetiza mediante la oxidación del naftaleno por el óxido crómico en presencia de alcohol.
Antraquinona
– Se sintetiza la antraquinona por la condensación del benceno con anhídrido ftálico en presencia de AlCl3 (acilación de Friedel-Crafts), generando el ácido O-benzoil benzoico, el cual experimenta un proceso de acilación formando la antraquinona.
– Se produce la antraquinona por la oxidación del antraceno con ácido crómico en ácido sulfúrico al 48%, o por oxidación con aire en fase de vapor.
Reacciones de las quinonas
– Los agentes reductores, como ácido sulfúrico, cloruro estañoso o ácido yodhídrico, actúan sobre la benzoquinona reduciéndola a hidroquinona.
– También una solución de yoduro de potasio reduce una solución de benzoquinona a hidroquinona, que puede ser oxidada de nuevo con nitrato de plata.
– El cloro y los agentes clorantes, como el clorato de potasio, en presencia de ácido clorhídrico, forman derivados clorados de la benzoquinona.
– La 1,2-benzoquinona se condensa con la O-fenildiamina para formar las quinoxalinas.
– La benzoquinona se usa como un agente oxidante en las reacciones de química orgánica.
– En la síntesis de Baily-Scholl (1905), la antraquinona se condensa con el glicerol para formar bezantreno. En el primer paso, la quinona se reduce por el cobre con ácido sulfúrico como medio. Un grupo carbonilo se convierte en un grupo metileno, y después se adiciona el glicerol.
Funciones y usos de las quinonas
Vitamina K1
La vitamina K1 (filoquinona), formada por la unión de un derivado de la naftoquinona con una cadena lateral de un hidrocarburo alifático, cumple una función central en el proceso de coagulación, ya que interviene en la síntesis de la protrombina, un factor de la coagulación.
Ubiquinona
– La ubiquinona, o citocromo Q, se forma por un derivado de la pbenzoquinona unida a una cadena lateral de un hidrocarburo alifático.
– Interviene en la cadena de transporte electrónico en condiciones aeróbicas, acoplada a la síntesis de ATP en las mitocondrias.
Benzoquinonas
– La embelina es un colorante que se usa para teñir de amarillo la lana. Además, la alizarina (antraquinona) es empleada en la tinción.
– Una solución alcalina de 1,4-bencenodiol (hidroquinona) y sulfato de sodio, se usa como un sistema revelador que actúa sobre las partículas de bromuro de plata activadas, reduciéndolas a plata metálica, que constituye un negativo de las fotos.
Plastoquinona
La plastoquinona forma parte de una cadena de transporte de electrones entre los fotosistemas I y II, que intervienen en la fotosíntesis de los vegetales.
Naftoquinonas
– Los protozoarios de los géneros Leishmania, Tripanosoma y Toxoplasma muestran susceptibilidad a una naftoquinona presente en la drosera (D. lycoides).
– La plumbagina es una naftoquinona que se ha usado para calmar el dolor reumático y presenta, además, acciones antiespasmódicas, antibacterianas y antifúngicas.
– Se ha reportado en una naftoquinona, llamada lapachol, una actividad antitumoral, antimalárica y antifúngica.
– La 2,3-dicloro-1,4-naftoquinona presenta una actividad antifúngica. Había sido utilizada previamente en la agricultura, en el control de la plaga y en la industria textil.
– Se ha sintetizado el antibiótico fumaquinona que presenta actividad selectiva contra las bacterias grampositivas, especialmente con Streptomyces fumanus.
– Hay naftoquinonas que ejercen una acción inhibitoria sobre el Plasmodium sp. Se han sintetizado derivados de la naftoquinona que presentan una eficiencia antimalárica cuatro veces superior a la quinina.
– La lawsona es un pigmento aislado de las hojas y tallo de la henna. Presenta una coloración anaranjada y se usa para teñir el cabello.
– La juglona, obtenida de las hojas y cáscaras del nogal, se emplea en la tinción de la madera.
Referencias
- Carey F. Química Orgánica. Mc Graw Hill.
- John D. Robert y Marjorie C. Caserio. Quinones. Recuperado de chem.libretexts.org
