Lacasas: características, estructura, funciones
Las lacasas, p-difenol:dioxigeno oxidorreductasas o benzenediol-oxígeno oxidorreductasas, son enzimas que pertenecen al grupo de las enzimas oxidasas llamadas “oxidasas azules de cobre”.
Existen en las plantas superiores, en algunos insectos, en bacterias y en prácticamente todos los hongos que han sido estudiados; su color azul característico es producto de cuatro átomos de cobre unidos a la molécula en su sitio catalítico.
Estas enzimas fueron descritas por Yoshida y colaboradores en el año 1883, al estudiar la resina del árbol Rhus vernicifera o “árbol de la laca” japonés, donde se determinó que su función principal era la de catalizar reacciones de polimerización y despolimerización de compuestos.
Mucho después se descubrió que, en los hongos, estas proteínas con actividad enzimática tienen funciones específicas en los mecanismos de remoción de fenoles tóxicos del medio donde crecen, mientras que en las plantas están implicadas en procesos sintéticos como la lignificación.
Los avances científicos respecto al estudio de estas enzimas permitieron su empleo a nivel industrial, donde se ha aprovechado su capacidad catalítica, especialmente en los contextos de la biorremediación, de textilería, en la remoción de tintes aplicados a textiles, en la industria papelera, entre otras.
Las principales razones por las cuales las lacasas son tan interesantes desde el punto de vista industrial tienen que ver con el hecho de que sus reacciones de oxidación implica, simplemente, la reducción del oxígeno molecular y la producción de agua como elemento secundario.
Índice del artículo
Las enzimas lacasas pueden ser secretadas o encontrarse en la región intracelular, pero ello depende del organismo que se estudie. A pesar de esto, la mayor parte de las enzimas analizadas (con excepción de algunas proteínas de ciertos hongos e insectos) son proteínas extracelulares.
Estas enzimas, como se comentó anteriormente, se encuentran predominantemente en hongos, en plantas superiores, en bacterias y en algunas especies de insectos.
Entre las plantas donde se ha demostrado su existencia están manzanos, espárragos, papas, peras, mangos, duraznos, pinos, ciruelos, entre otros. Los insectos que expresan lacasas pertenecen principalmente a los géneros Bombyx, Calliphora, Diploptera, Drosophila, Musca, Papilio, Rhodnius, y otros.
Los hongos son los organismos de los cuales se han aislado y estudiado la mayor cantidad y variedad de lacasas, y estas enzimas están presentes tanto en ascomicetes como en deuteromicetes y basidiomicetes.
La reacción que catalizan las lacasas consiste en la oxidación monoelectrónica de una molécula de sustrato, que puede pertenecer al grupo de fenoles, compuestos aromáticos o aminas alifáticas, a su radical reactivo correspondiente.
El resultado de la reacción catalítica es la reducción de una molécula de oxígeno a dos moléculas de agua y la oxidación, al mismo tiempo, de cuatro moléculas de sustrato para producir cuatro radicales libres reactivos.
Los radicales libres intermediarios pueden unirse y formar dímeros, oligómeros o polímeros, por ello se dice que las lacasas catalizan reacciones de polimerización y “despolimerización”.
Las lacasas son glicoproteínas, es decir, son proteínas que poseen residuos oligosacáridos unidos covalentemente a la cadena polipeptídica, y estos representan entre el 10 y el 50% del peso total de la molécula (en las enzimas vegetales el porcentaje puede ser un poco mayor).
La porción carbohidratada de este tipo de proteínas contiene monosacáridos como glucosa, manosa, galactosa, fucosa, arabinosa y algunas hexosaminas, y se piensa que la glicosilación tiene importantes funciones en la secreción, la susceptibilidad proteolítica, en la actividad, la retención de cobre y la estabilidad térmica de la proteína.
Generalmente estas enzimas se encuentran en la naturaleza como monómeros u homodímeros y el peso molecular de cada monómero puede variar entre los 60 y los 100 kDa.
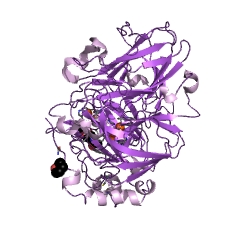
El centro catalítico de las lacasas está conformado por cuatro átomos de cobre (Cu), que le otorgan a la molécula en general un color azul debido a la absorción electrónica que tiene lugar en los enlaces cobre-cobre (Cu-Cu).
Las lacasas vegetales tienen puntos isoeléctricos con valores cercanos a 9 (bastante básicos), mientras que las enzimas fúngicas están entre puntos isoeléctricos de 3 y 7 (por lo que son enzimas que trabajan en condiciones ácidas).
Muchos hongos que producen lacasas también poseen isoformas de estas, que están codificadas por el mismo gen o por genes diferentes. Estas isoenzimas difieren unas de otras principalmente en cuanto a su estabilidad, a su pH y temperatura óptimos para catalizar y en cuanto a la afinidad por diferentes tipos de sustrato.
En determinadas condiciones, estas isoenzimas pueden tener funciones fisiológicas diferentes, pero ello depende de la especie o de la condición en la que esta habita.
Algunos investigadores han demostrado que las lacasas están implicadas en la “esclerotización” de la cutícula en los insectos y del ensamblaje de esporas resistentes a luz ultravioleta en microorganismos del género Bacillus.
En los organismos vegetales, los lacasas participan en la formación de la pared celular, en los procesos de lignificación y “deslignificación” (pérdida o desintegración de la lignina); y además, se han relacionado con la desintoxicación de los tejidos mediante la oxidación de fenoles antifúngicos o la desactivación de fitoalexinas.
Significativamente abundantes en este grupo de organismos, las lacasas participan en variedad de procesos celulares y fisiológicos. Entre ellos se puede mencionar la protección de los hongos patogénicos de los taninos y las “fitoalexinas” vegetales; por lo que se puede decir que, para los hongos, estas enzimas son factores de virulencia.
Las lacasas también tienen funciones en la morfogénesis y diferenciación de las estructuras de resistencia y esporas de los basidiomicetes, así como en la biodegradación de lignina en los hongos que degradan tejidos de especies vegetales leñosas.
Al mismo tiempo, las lacasas participan en la formación de pigmentos de los micelios y los cuerpos fructíferos de muchos hongos y contribuyen en los procesos de adhesión célula-célula, en la formación del “pegamento” polifenólico que une a las hifas y en la evasión del sistema inmune de los hospedadores infectados con hongos patógenos.
Estas particulares enzimas son empleadas industrialmente con varios propósitos, pero los más resaltantes corresponden a las industrias textiles y papeleras y a los procesos de biorremediación y descontaminación de aguas residuales producto de otros procesos industriales.
Puntualmente, estas enzimas son empleadas con frecuencia para la oxidación de fenoles y sus derivados presentes en aguas contaminadas con desechos industriales, cuyos productos de catálisis son insolubles (polimerizados) y precipitan, lo que los hace fácilmente separables.
En la industria alimenticia también tienen cierta importancia puesto que la remoción de compuestos fenólicos es necesaria para la estabilización de bebidas como el vino, la cerveza y los jugos naturales.
Son empleadas en la industria de cosméticos, en la síntesis química de muchos compuestos, en la biorremediación de suelos y en la nanobiotecnología.
Las más empleadas son las lacasas provenientes de hongos, pero recientemente se ha determinado que las lacasas bacterianas poseen características más destacadas desde el punto de vista industrial; son capaces de trabajar con mayor variedad de sustratos y a rangos de temperatura y pH mucho más amplios, además de que son mucho más estables frente agentes inhibitorios.
- Claus, H. (2004). Laccases: structure, reactions, distribution. Micron, 35, 93–96.
- Couto, S. R., Luis, J., & Herrera, T. (2006). Industrial and biotechnological applications of laccases: A review. Biotechnology Advances, 24, 500–513.
- Madhavi, V., & Lele, S. S. (2009). Laccase: properties and applications. Bioresources, 4(4), 1694–1717.
- Riva, S., Molecolare, R., & Bianco, V. M. (2006). Laccases: blue enzymes for green chemistry. Trends in Biotechnology, 24(5), 219–226.
- Singh, P., Bindi, C., & Arunika, G. (2017). Bacterial laccase: recent update on production, properties and industrial applications. Biotech, 7(323), 1–20.
