Glucólisis anaerobia: reacciones y vías fermentativas
La glucólisis anaerobia o anaeróbica es una ruta catabólica empleada por muchos tipos de células para la degradación de la glucosa en ausencia de oxígeno. Es decir, la glucosa no es oxidada completamente a dióxido de carbono y agua, como es el caso de la glucólisis aeróbica, sino que se generan productos fermentativos.
Se denomina glucólisis anaerobia puesto que tiene lugar sin la presencia del oxígeno, que en otros casos funciona como aceptor final de electrones en la cadena transportadora de la mitocondria, donde se producen grandes cantidades de energía a partir del procesamiento de los productos glucolíticos.
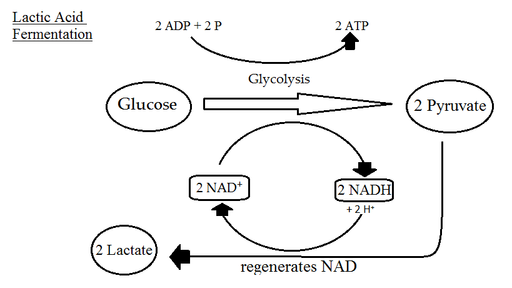
Dependiendo del organismo, una condición de anaerobiosis o ausencia de oxígeno va a resultar en la producción de ácido láctico (células musculares, por ejemplo) o de etanol (levaduras), a partir del piruvato generado por el catabolismo de la glucosa.
Como resultado, el rendimiento energético cae drásticamente, ya que sólo se producen dos moles de ATP por cada mol de glucosa que es procesado, en comparación con los 8 moles que pueden obtenerse durante la glucólisis aeróbica (únicamente en la fase glucolítica).
La diferencia en el número de moléculas de ATP tiene que ver con la reoxidación del NADH, que no genera ATP adicional, contrario a lo que sucede en la glucólisis aeróbica, que por cada NADH se obtienen 3 moléculas de ATP.
Índice del artículo
La glucólisis anaeróbica no dista en absoluto de la glucólisis aeróbica, puesto que el término “anaeróbico” hace referencia más bien a lo que ocurre posterior a la ruta glucolítica, es decir, al destino de los productos e intermediarios de reacción.
Así pues, en las reacciones de la glucólisis anaeróbica participan diez enzimas diferentes, a saber:
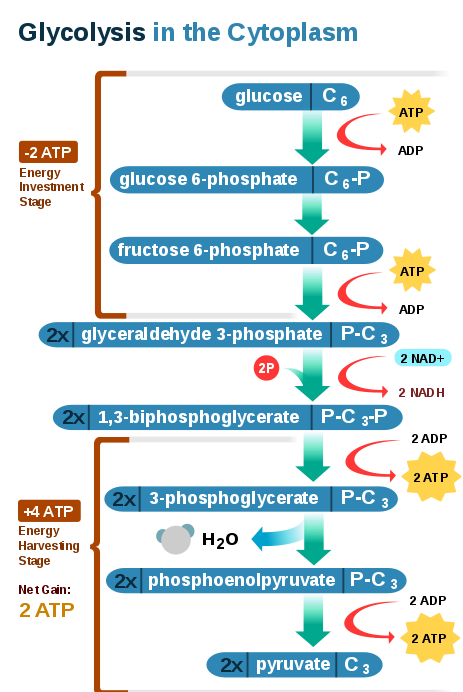
1-Hexoquinasa (HK): utiliza una molécula de ATP por cada molécula de glucosa. Produce glucosa 6-fosfato (G6P) y ADP. La reacción es irreversible y amerita iones magnesio.
2-Fosfoglucosa isomerasa (PGI): isomeriza la G6P a fructosa 6-fosfato (F6P).
3-Fosfofructoquinasa (PFK): fosforila la F6P a fructosa 1,6-bifosfato (F1,6-BP) empleando una molécula de ATP por cada F6P, esta reacción también es irreversible.
4-Aldolasa: escinde la molécula de F1,6-BP y produce gliceraldehído 3-fosfato (GAP) y dihidroxiacetona fosfato (DHAP).
5-Triosa-fosfato isomerasa (TIM): participa en la interconversión de DHAP y GAP.
6-Gliceraldehído 3-fosfato deshidrogenasa (GAPDH): emplea dos moléculas de NAD+ y 2 moléculas de fosfato inorgánico (Pi) para fosforilar el GAP, rinde 1,3-bifosfoglicerato (1,3-BPG) y 2 NADH.
7-Fosfoglicerato quinasa (PGK): produce dos moléculas de ATP por fosforilación a nivel de sustrato de dos moléculas de ADP. Emplea como donador de grupo fosfato cada molécula de 1,3-BPG. Produce 2 moléculas de 3-fosfoglicerato (3PG).
8-Fosfoglicerato mutasa (PGM): reorganiza la molécula de 3PG para originar un intermediario con mayor energía, el 2PG.
9-Enolasa: a partir del 2PG produce fosfoenolpiruvato (PEP) por deshidratación del primero.
10-Piruvato quinasa (PYK): el fosfoenolpiruvato es empleado por esta enzima para formar piruvato. La reacción implica la transferencia del grupo fosfato en la posición 2 del fosfoenolpiruvato a una molécula de ADP. Se producen 2 piruvatos y 2 ATP por cada glucosa.
La fermentación es el término que se emplea para indicar que la glucosa u otros nutrientes son degradados en ausencia de oxígeno, con el fin de obtener energía.
En ausencia de oxígeno la cadena transportadora de electrones no posee un aceptor final y por ende no ocurre la fosforilación oxidativa que rinde grandes cantidades de energía en forma de ATP. El NADH no es reoxidado por vía mitocondrial sino por vías alternas, que no producen ATP.
Sin suficiente NAD+ la vía glucolítica se detiene, puesto que la transferencia del fosfato al GAP requiere de la reducción concomitante de este cofactor.
Algunas células poseen mecanismos alternativos para sobrellevar períodos de anaerobiosis, y generalmente estos mecanismos implican algún tipo de fermentación. Otras células, por el contrario, dependen casi exclusivamente de los procesos fermentativos para su subsistencia.
Los productos de las vías fermentativas de muchos organismos son económicamente relevantes para el hombre; ejemplos son la producción de etanol por parte de algunas levaduras en anaerobiosis y la formación de ácido láctico por las lacto-bacterias empleadas para la producción de yogurt.
Muchos tipos de células en ausencia de oxígeno producen ácido láctico gracias a la reacción catalizada por el complejo lactato deshidrogenasa, que utiliza los carbonos del piruvato y los NADH producidos en la reacción de la GAPDH.
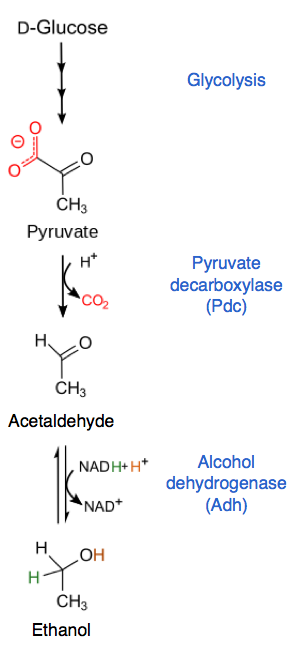
El piruvato es convertido en acetaldehído y CO2 por la piruvato descarboxilasa. El acetaldehído luego es empleado por la alcohol deshidrogenasa, que lo reduce produciendo etanol y regenerando una molécula de NAD+ por cada molécula de piruvato que ingresa por esta vía.
La glucólisis anaeróbica tiene como característica principal el hecho de que los productos finales no corresponden a CO2 y agua, como en el caso de la glucólisis aeróbica. En su lugar se generan productos típicos de reacciones de fermentación.
Algunos autores han descrito un proceso de “fermentación aeróbica” o glucólisis aeróbica de la glucosa para ciertos organismos, entre los que destacan algunos parásitos de la familia Trypanosomatidae y muchas células tumorales cancerosas.
En estos organismos se ha demostrado que aún en presencia de oxígeno, los productos de la vía glucolítica corresponden a productos de rutas fermentativas, por lo que se piensa que ocurre una oxidación “parcial” de la glucosa, puesto que no se extrae toda la energía posible de sus carbonos.
Aunque la “fermentación aeróbica” de la glucosa no implica la ausencia total de actividad respiratoria, ya que no es un proceso de todo o nada. No obstante, la bibliografía señala la excreción de productos como piruvato, lactato, succinato, malato y otros ácidos orgánicos.
Muchas células cancerígenas muestran un aumento en la toma de glucosa y del flujo glucolítico.
Los tumores en los pacientes con cáncer crecen rápidamente, por lo que los vasos sanguíneos se encuentran en hipoxia. Así, el suplemento energético de estas células depende principalmente de la glucólisis anaeróbica.
Ahora bien, este fenómeno está ayudado por un factor de transcripción inducible por hipoxia (HIF), que incrementa la expresión de las enzimas glucolíticas y transportadores de glucosa en la membrana a través de complejos mecanismos.
- Akram, M. (2013). Mini-review on Glycolysis and Cancer. J. Canc. Educ., 28, 454–457.
- Bustamante, E., & Pedersen, P. (1977). High aerobic glycolysis of rat hepatoma cells in culture: Role of mitochondrial hexokinase. Proc. Natl. Acad. Sci., 74(9), 3735–3739.
- Cazzulo, J. J. (1992). Aerobic fermentation of glucose by trypanosomatids. The FASEB Journal, 6, 3153–3161.
- Jones, W., & Bianchi, K. (2015). Aerobic glycolysis: beyond proliferation. Frontiers in Immunology, 6, 1–5.
- Li, X., Gu, J., & Zhou, Q. (2015). Review of aerobic glycolysis and its key enzymes – new targets for lung cancer therapy. Thoracic Cancer, 6, 17–24.
- Maris, A. J. A. Van, Abbott, Æ. D. A., Bellissimi, Æ. E., Brink, J. Van Den, Kuyper, Æ. M., Luttik, Æ. M. A. H., Pronk, J. T. (2006). Alcoholic fermentation of carbon sources in biomass hydrolysates by Saccharomyces cerevisiae: current status. Antonie van Leeuwenhoek, 90, 391–418.
- Nelson, D. L., & Cox, M. M. (2009). Lehninger Principios de Bioquímica. Ediciones Omega (5th ed.).
