Grupo hidroxilo: qué es, estructura, características, ejemplos
¿Qué es un grupo hidroxilo?
Un grupo hidroxilo es un grupo funcional o una parte de otros grupos funcionales presentes en muchos compuestos orgánicos e inorgánicos. Está formado por un átomo de hidrógeno y uno de oxígeno (de allí su nombre).
Los grupos hidroxilo suelen estar enlazados a un átomo de carbono o a otro elemento no metálico como el azufre o el fósforo, entre otros, y son uno de los grupos funcionales más importantes en química orgánica.
Este grupo de átomos está presente en grupos funcionales orgánicos como los alcoholes, los fenoles y los ácidos carboxílicos, y es el que le da a cada uno de estos grupos funcionales sus propiedades químicas características. En las distintas estructuras se puede representar como –OH o HO–
Características de los grupos hidroxilo
- Consiste en un átomo de oxígeno y uno de hidrógeno enlazados entre sí y enlazados a otro átomo en una molécula a través de enlaces covalentes.
- El enlace entre el átomo de hidrógeno y oxígeno es un enlace polar en el que el oxígeno posee carga parcial negativa y el hidrógeno carga parcial positiva, lo que hace que el grupo hidroxilo sea un grupo funcional polar.
- Posee una estructura similar a la del agua. Por esta razón, muchos de los compuestos que lo contienen suelen ser solubles en dicho solvente.
- Posee un hidrógeno directamente enlazado al átomo oxígeno, por lo que el grupo hidroxilo puede formar un enlace de hidrógeno en el que participa como grupo donante de hidrógeno.
- Al poseer dos pares de electrones libres sobre el átomo de oxígeno, el grupo hidroxilo puede formar dos enlaces de hidrógeno adicionales actuando como aceptor de átomos de hidrógeno.
- Puede actuar como ácido cediendo un protón a una base. Dependiendo del grupo funcional del cual forme parte y del átomo al cual esté directamente enlazado, el grupo hidroxilo puede mostrar diferentes niveles de acidez. Por ejemplo, en los alcoholes, posee un pKa de 15 o más (ácido más débil que el agua), en los fenoles varía entre 7 y 10 mientras que en los ácidos carboxílicos suele estar entre 4 y 5.
- También puede actuar como base de Lewis, donando uno de sus pares de electrones para enlazarse a otro protón o a algún otro ácido de Lewis.
Estructura del grupo hidroxilo
Como se mencionó entre las características, los átomos de oxígeno e hidrógeno en el grupo hidroxilo forman un enlace covalente polar.
Además, el átomo de oxígeno forma un segundo enlace covalente con otro átomo que forma parte de una molécula como un alcohol, fenol a algún otro compuesto. La estructura de Lewis de este grupo se presenta a continuación:
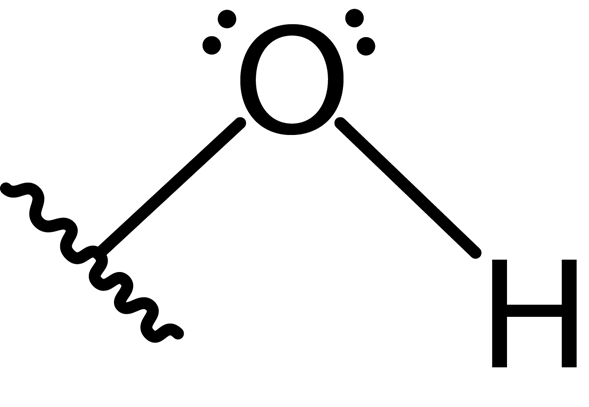
Debido a la presencia de los dos pares de electrones libres sobre el átomo de oxígeno y los dos enlaces covalentes, el grupo hidroxilo posee geometría angular con un ángulo de aproximadamente 104°, ligeramente menor que el ángulo tetraédrico. La longitud del enlace oxígeno-hidrógeno es de alrededor de 0.97 angstroms.
Grupo hidroxilo, radical hidroxilo y anión hidróxido
Es muy común confundir al grupo hidroxilo con el radical hidroxilo y el anión hidróxido, ya que todos están formados por los mismos dos átomos, sin embargo, estos términos no se refieren a lo mismo.
Por un lado, el radical hidroxilo se diferencia del grupo hidroxilo en que es un radical libre con un número impar de electrones de valencia, y además no está enlazado a ningún otro átomo o grupo de átomos (por eso se le dice libre).
A pesar de estas diferencias, muchas personas utilizan erróneamente el término radical hidroxilo para referirse al grupo hidroxilo cuando está presente en una molécula.
El anión hidróxido, por otro lado, es un ion con carga negativa formado por hidrógeno y oxígeno, mientras que el grupo hidroxilo es un grupo neutro.
Además, mientras que el grupo hidroxilo siempre está enlazado a una molécula por medio de un enlace covalente, los compuestos que contienen iones hidróxido presentan enlace iónico entre este y algún metal como el sodio, el litio o el potasio.
Ejemplos de grupo hidroxilo
Alcoholes
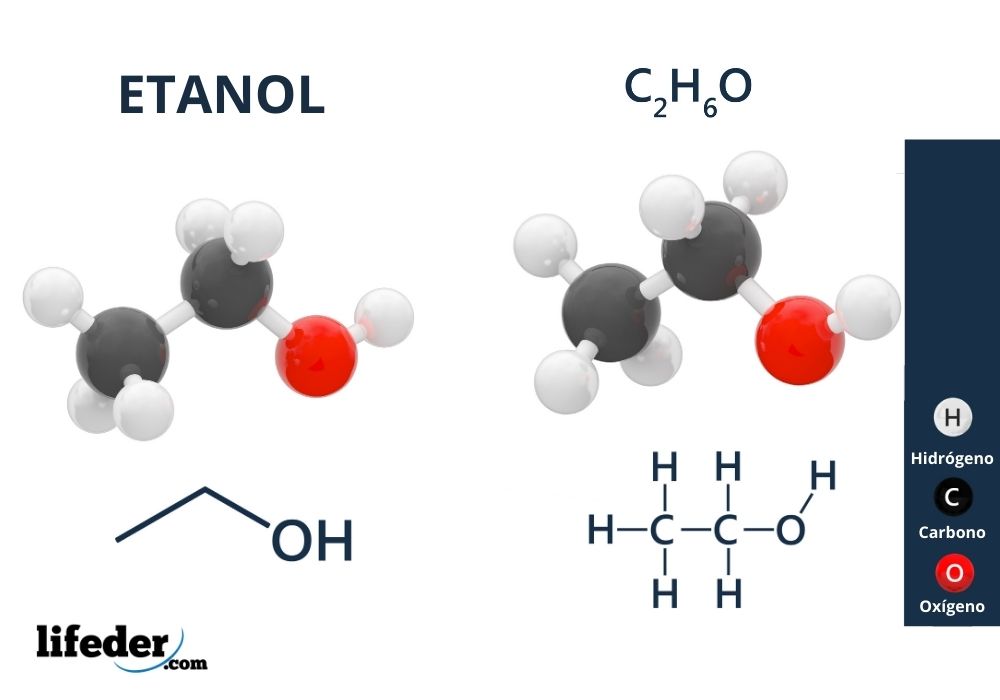
Los alcoholes poseen grupos hidroxilo enlazados a un carbono alifático. Ejemplos de alcoholes son:
- Alcohol metílico.
- Etanol.
- Alcohol isopropílico.
Fenoles
Los fenoles se caracterizan por poseer un grupo hidroxilo directamente enlazado a un anillo aromático. Algunos ejemplos de fenoles comunes son:
- Fenol.
- Alfa y Beta-naftol.
- Orto, meta y para cresol.
Carbohidratos
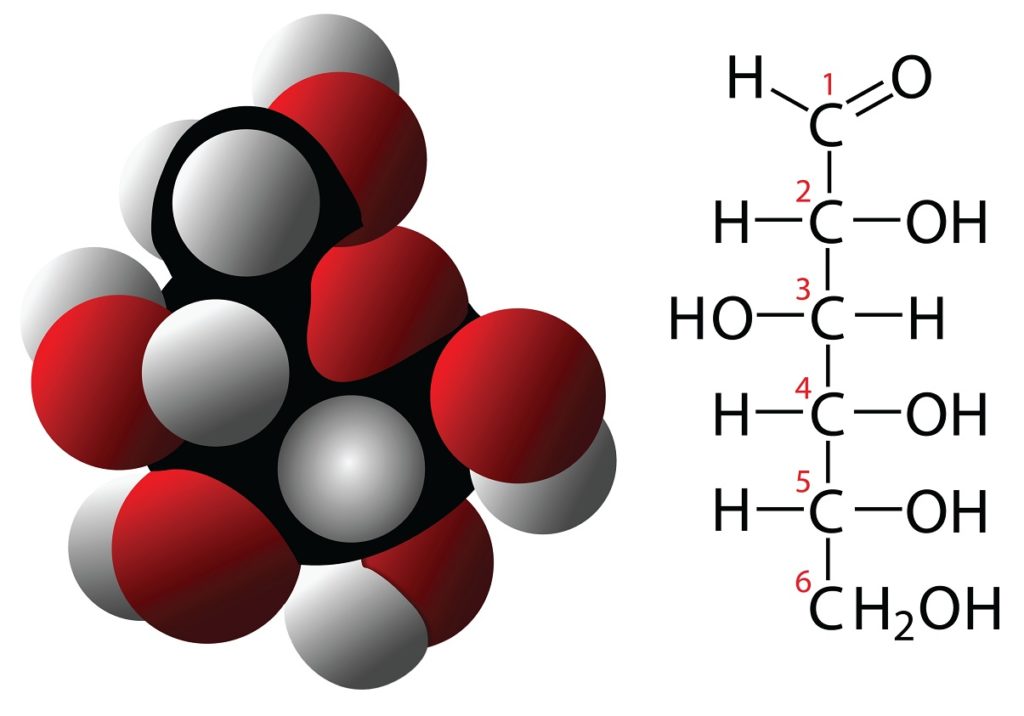
Los carbohidratos son compuestos con 3 o más átomos de carbono que se caracterizan por poseer una fórmula empírica formada por carbonos y moléculas de agua. Estos compuestos suelen poseer múltiples grupos hidroxilos lo que los hace muy solubles en agua. Algunos ejemplos de carbohidratos son:
- Glucosa.
- Fructosa.
- Sacarosa.
Ácidos carboxílicos
El grupo funcional carboxilo presente en los ácidos carboxílicos corresponde a uno de los grupos funcionales más ácidos que puede tener una molécula orgánica. Estos compuestos suelen ser ácidos débiles al compararlos con algunos ácidos minerales, pero pueden llegar a ser considerablemente ácidos dependiendo de su estructura.
La acidez del grupo carboxilo se debe a la presencia de un grupo hidroxilo enlazado a un grupo carbonilo, el cual estabiliza la carga negativa del anión que se forma cuando el hidroxilo cede su protón. Algunos ejemplos de ácidos carboxílicos son:
- Ácido acético.
- Ácido benzóico.
- El ácido trifluoroacético.
Ácidos sulfónicos
Los ácidos sulfónicos son compuestos orgánicos que se forman por la reacción entre algunos compuestos orgánicos y el ácido sulfúrico o el dióxido de azufre. Este tipo de compuestos posee un grupo hidroxilo y, en general, son ácidos bastante fuertes, comparables con el ácido sulfúrico.
Algunos ejemplos de ácidos sulfónicos son:
- El ácido pentanosulfónico.
- Los isómeros orto, meta y para del ácido toluensulfónico.
- El ácido bencenosulfónico.
Ácidos inorgánicos
Los grupos hidroxilo no solo aparecen en los compuestos orgánicos. Muchos compuestos inorgánicos también los poseen, en particular los ácidos oxácidos. En estos casos, el grupo hidroxilo está enlazado directamente a algún no metal, generalmente distinto del carbono.
Algunos ejemplos de ácidos inorgánicos que poseen grupos hidroxilo junto con el no metal al cual este está enlazado son:
- Ácido hipocloroso, en el que el grupo hidroxilo está enlazado a un átomo de cloro.
- El ácido sulfúrico, el cual posee dos grupos hidroxilo enlazados a un átomo de azufre.
- Ácido fosfórico, en el que los tres grupos hidroxilo se enlazan a un átomo de fósforo.
