Monómeros: qué son, características, estructura, tipos, ejemplos
¿Qué son los monómeros?
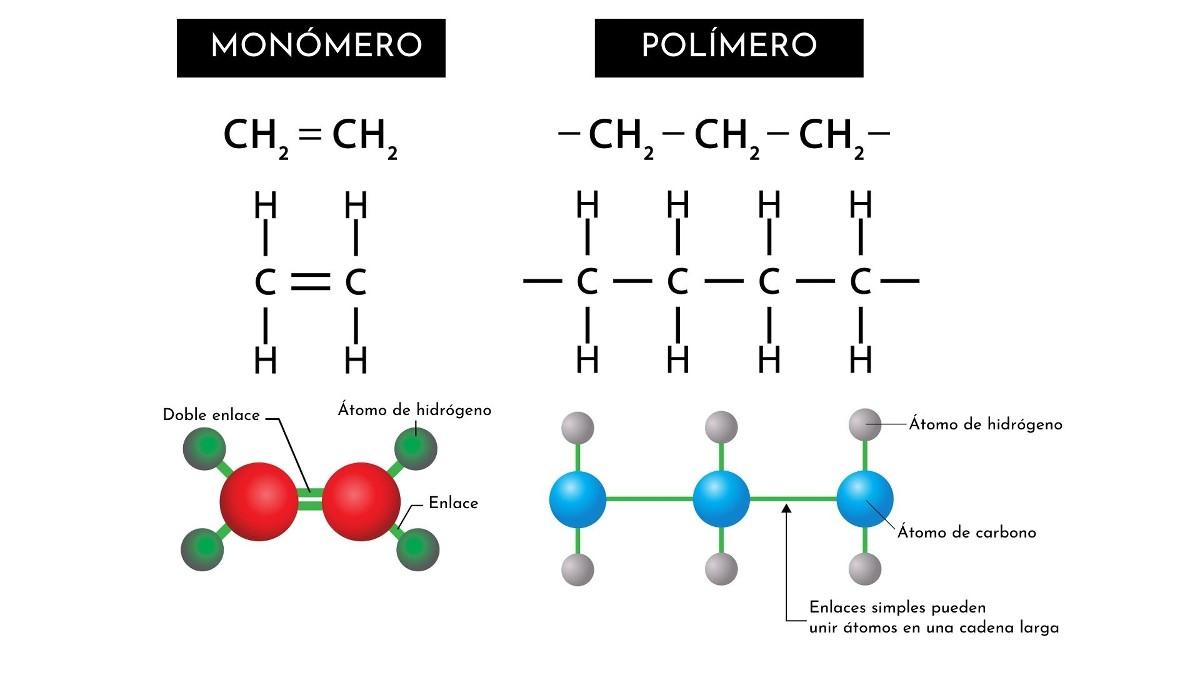
Los monómeros son moléculas pequeñas o simples que constituyen la unidad estructural básica o esencial de moléculas más grandes o complejas denominadas polímeros. Monómero es una palabra de origen griego que significa mono, uno, y mero, parte.
A medida que un monómero se une con otro, se forma un dímero. Al unirse este a su vez con otro monómero, forma un trímero, y así sucesivamente, hasta formar cadenas cortas llamadas oligómeros, o cadenas más largas, que son los denominados polímeros.
Los monómeros se unen o polimerizan mediante la formación de enlaces químicos al compartir pares de electrones; es decir, se unen por enlaces de tipo covalente.
A esta unión de monómeros se le conoce como polimerización. Se pueden unir monómeros de un mismo tipo o diferentes, y el número de enlaces covalentes que pueden establecer con otra molécula va a determinar la estructura del polímero que formen (cadenas lineales, inclinadas o estructuras tridimensionales).
Existe una gran variedad de monómeros, entre los cuales se encuentran los de origen natural. Estos pertenecen y diseñan las moléculas orgánicas denominadas biomoléculas, presentes en la estructura de los seres vivos.
Por ejemplo, los aminoácidos que forman las proteínas; las unidades de monosacáridos de los carbohidratos y los mononucleótidos que forman los ácidos nucléicos. También existen monómeros sintéticos, los cuales permiten elaborar una innumerable variedad de productos poliméricos inertes, como pinturas o plásticos.
Características de los monómeros
Los monómeros se unen mediante enlaces covalentes
Los átomos que participan en la formación de un monómero se mantienen unidos por enlaces fuertes y estables como el enlace covalente. Asimismo, los monómeros polimerizan o se unen con otras moléculas monoméricas mediante estos enlaces, dándole fuerza y estabilidad a los polímeros.
Estos enlaces covalentes entre los monómeros pueden formarse por reacciones químicas que dependerán de los átomos que conforman el monómero, de la presencia de dobles enlaces y de otras características que presenten la estructura del monómero.
El proceso de polimerización puede darse por una de las tres reacciones siguientes: por condensación, adición o por radicales libres. Cada una de ellas conlleva sus propios mecanismos y modo de crecimiento.
Funcionalidad de los monómeros y estructura del polímero
Un monómero se puede unir con al menos otras dos moléculas monoméricas. Esta propiedad o característica es lo que se conoce como funcionalidad de los monómeros, y es lo que les permite ser las unidades estructurales de las macromoléculas.
Los monómeros pueden ser bifuncionales o polifuncionales, dependiendo de los sitios activos o reactivos del monómero; es decir, de los átomos de la molécula que pueden participar en la formación de enlaces covalentes con los átomos de otras moléculas o monómeros.
También esta característica es importante, ya que está estrechamente ligada con la estructura de los polímeros que conformen, tal y como se detalla a continuación.
Bifuncionalidad: polímero lineal
Los monómeros son bifuncionales cuando presentan solo dos sitios de unión con otros monómeros; es decir, el monómero solo puede formar dos enlaces covalentes con otros monómeros y forma únicamente polímeros lineales.
Entre los polímeros lineales se pueden mencionar como ejemplo el etilen glicol y los aminoácidos.
Monómeros polifuncionales – polímeros tridimensionales
Existen monómeros que se pueden unir con más de dos monómeros y constituyen las unidades estructurales de mayor funcionalidad.
Se denominan polifuncionales y son los que producen las macromoléculas poliméricas ramificadas, de red o tridimensionales; como el polietileno, por ejemplo.
Esqueleto o estructura central
Con doble enlace entre carbono y carbono
Existen monómeros que presentan en su estructura un esqueleto central conformado por al menos dos átomos de carbono unidos por un enlace doble (C=C).
A su vez, esta cadena o estructura central presenta átomos unidos lateralmente que pueden cambiar conformando un monómero diferente (R2C=CR2).
Si se modifica o sustituye cualquiera de las cadenas R, se obtiene un monómero diferente. Asimismo, cuando estos nuevos monómeros se unan formarán un polímero distinto.
Se puede mencionar como ejemplo de este grupo de monómeros el propileno (H2C=CH3H), el tetrafluoroetileno (F2C=CF2) y el cloruro de vinilo (H2C=CClH).
Dos grupos funcionales en la estructura
Aunque existen monómeros que poseen un solo grupo funcional, se encuentra un amplio grupo de monómeros que poseen dos grupos funcionales en su estructura.
Los aminoácidos son un buen ejemplo de ello. Poseen un grupo funcional amino (-NH2) y el grupo funcional del ácido carboxílico (-COOH) unidos a un átomo de carbono central.
Esta característica de ser un monómero difuncional, también le da la capacidad de formar largas cadenas de polímeros, como la presencia de los dobles enlaces.
Grupos funcionales
En general las propiedades que presentan los polímeros son dadas por los átomos que forman las cadenas laterales de los monómeros. Estas cadenas conforman los grupos funcionales de los compuestos orgánicos.
Existen familias de compuestos orgánicos cuyas características son dadas por los grupos funcionales o cadenas laterales. Como ejemplo se encuentra el grupo funcional ácido carboxílico R–COOH, el grupo amino R–NH2, el alcohol R–OH, entre muchos otros que participan en las reacciones de polimerización.
Unión de monómeros iguales o de diferente tipo
Unión de monómeros iguales
Los monómeros pueden formar diferentes clases de polímeros. Se pueden unir monómeros iguales o de un mismo tipo y generar los denominados homopolímeros.
Como ejemplo se puede mencionar el estireno, monómero que forma el poliestireno. El almidón y la celulosa también son ejemplos de homopolímeros formados por largas cadenas ramificadas del monómero glucosa.
Unión de monómeros diferentes
La unión de monómeros diferentes forman los copolímeros. Las unidades se repiten en diferente número, orden o secuencia a lo largo de la estructura de las cadenas poliméricas (A-B-B-B-A-A-B-A-A-…).
Como ejemplo de copolímeros se puede mencionar el nailon, polímero formado por unidades repetitivas de dos monómeros diferentes. Estos son el ácido dicarboxílico y una molécula de diamina, los cuales se unen vía condensación en proporciones equimolares (iguales).
También se pueden unir monómeros diferentes en desigual proporción, como el caso de formación de un polietileno especializado que tiene como estructura básica el monómero 1-octeno más el monómero etileno.
Tipos de monómeros
Existen muchas características que permiten establecer varios tipos de monómeros, entre las que destacan su origen, funcionalidad, estructura, el tipo de polímero que forman, cómo se polimerizan y sus enlaces covalentes.
Monómeros naturales
- Existen monómeros de origen natural como el isopreno, que se obtiene de la savia o látex de las plantas, y que además es la estructura monomérica del caucho natural.
- Algunos aminoácidos producidos por insectos forman la fibroína, o proteína de la seda. Asimismo, se encuentran aminoácidos que forman el polímero queratina, la cual es la proteína de la lana producida por animales como las ovejas.
- Entre los monómeros naturales se encuentran también las unidades estructurales básicas de las biomoléculas. El monosacárido glucosa, por ejemplo, se une con otras moléculas de glucosa para formar diferentes tipos de carbohidratos como almidón, glucógeno, celulosa, entre otros.
- Los aminoácidos, por otra parte, pueden formar una amplia gama de polímeros conocidos como proteínas. Esto se debe a que son veinte tipos de aminoácidos, los cuales pueden enlazarse en cualquier orden arbitrario; y por lo tanto, terminan formando una u otra proteína con sus propias características estructurales.
- Los mononucleótidos, los cuales forman las macromoléculas denominadas ácidos nucleicos ADN y ARN respectivamente, también son monómeros muy importantes dentro de esta categoría.
Monómeros sintéticos
- Entre los monómeros artificiales o sintéticos (que son numerosos), se puede mencionar algunos con los que se elaboran diferentes variedades de plásticos, como el cloruro de vinilo, el cual forma el polivinil cloruro o PVC; y el gas etileno (H2C=CH2), y su polímero polietileno. Es bien conocido que con estos materiales se puede construir una gran variedad de envases, botellas, objetos para el hogar, juguetes, materiales de construcción, entre otros.
- El monómero tetrafluoroetileno (F2C=CF2) se encuentra formando el polímero denominado y conocido comercialmente como teflón.
- La molécula de caprolactama derivado del tolueno es esencial para la síntesis del nailon, entre muchos otros.
- Existen varios grupos de monómeros acrílicos que se clasifican según la composición y función. Entre estos se encuentran la acrilamida y metacrilamida, el acrilato, los acrílicos con flúor, entre otros.
Monómeros apolares y polares
Esta clasificación se realiza de acuerdo a la diferencia de electronegatividad de los átomos que forman el monómero. Cuando existe una notoria diferencia, se forman monómeros polares; por ejemplo, aminoácidos polares como la treonina y la asparagina.
Cuando la diferencia de electronegatividad es nula, los monómeros son apolares. Existen aminoácidos no polares como el triptófano, alanina, valina, entre otros; y también monómeros apolares como el acetato de vinilo.
Monómeros cíclicos o lineales
Conforme a la forma u organización de los átomos dentro de la estructura de los monómeros, estos pueden clasificarse como monómeros cíclicos, como la prolina o el óxido de etileno; y lineales o alifáticos, como el aminoácido valina o el etilenglicol, entre muchos otros.
Ejemplos de monómeros
Además de los ya mencionados, se tienen los siguientes ejemplos adicionales de monómeros:
- Formaldehído
- Furfural
- Cardanol
- Galactosa
- Estireno
- Alcohol polivinílico
- Isopreno
- Los ácidos grasos
- Epóxidos
- Y aunque no se mencionaron, existen monómeros cuyas estructuras no son carbonadas, sino sulfuradas, fosforadas, o tienen átomos de silicio.
Referencias
- Carey F. (2006). Química Orgánica. (6ta. ed.). México: Mc Graw Hill.
- The Editors of Encyclopedia Britannica (2015). Monomer: Chemical Compound. Tomado de: britannica.com
- Mathews, Holde y Ahern (2002). Bioquímica (3a. ed.). Madrid: PEARSON
- Polymers y Monomers. Recuperado de: materialsworldmodules.org
- Wikipedia (2018). Monomer. Tomado de: en.wikipedia.org
