Bioelementos: clasificación (primarios y secundarios)
“Bioelemento” es un término utilizado para referirse a los principales elementos químicos que componen a los seres vivos. En algunas clasificaciones, estos son divididos en elementos primarios y en elementos secundarios.
De los 87 elementos químicos que se conocen, solo 34 componen a la materia orgánica, y se sabe que 17 de estos 34 son verdaderamente indispensables para la vida. Además, de estos 17 elementos indispensables, cinco constituyen más del 90% de la materia que compone a los organismos vivos.
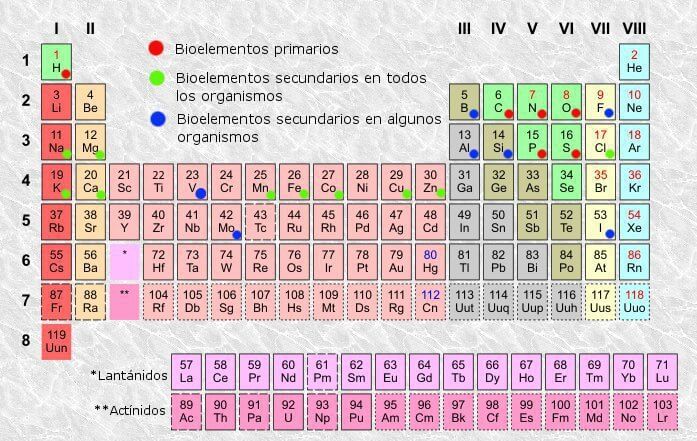
Los seis elementos principales en la materia orgánica son el hidrógeno (H, 59%), el oxígeno (O, 24 %), el carbono (C, 11%), el nitrógeno (N, 4%), el fósforo (P, 1%) y el azufre (S, del 0,1 al 1%).
Estos porcentajes reflejan la cantidad de átomos de cada elemento respecto a la cantidad total de átomos que constituye a las células vivas y estos son los que se conocen como “bioelementos primarios”.
Los bioelementos secundarios se encuentran en mucha menor proporción y son el potasio (K), el magnesio (Mg), el hierro (Fe), el calcio (Ca), el molibdeno (Mo), el flúor (F), el Cloro (Cl), el sodio (Na), el yodo (I), el cobre (Cu) y el Zinc (Zn).
Los elementos secundarios usualmente son cofactores en reacciones catalíticas y participan en numerosos de los procesos bioquímicos y fisiológicos inherentes a las células de los organismos.
Índice del artículo
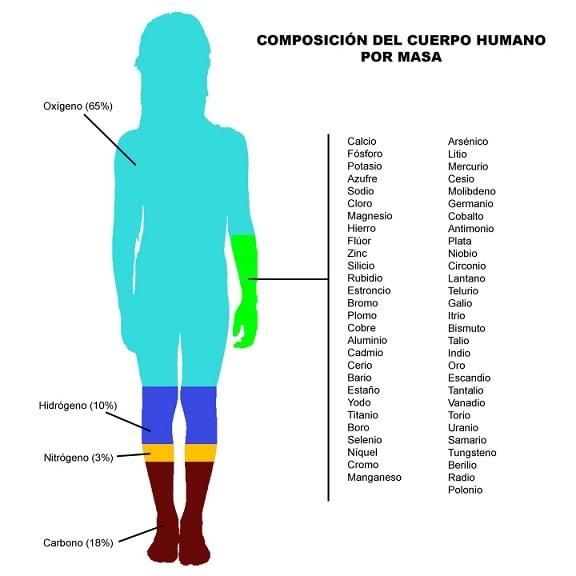
Los átomos de carbono, hidrógeno y oxígeno son la base estructural de las moléculas que componen la materia orgánica, entretanto el nitrógeno, el fósforo y el azufre interactúan con las diferentes biomoléculas para provocar reacciones químicas.
El hidrógeno es un elemento químico que existe en forma gaseosa a temperatura ambiente (25 º C), solo puede existir en estado sólido o líquido a temperatura ambiente cuando se encuentra enlazado a otras moléculas.
Se piensa que los átomos de hidrógeno estuvieron entre los primeros átomos que formaron el universo primitivo. Las teorías que se manejan proponen que los protones contenidos en el núcleo de los átomos de hidrógeno comenzaron a asociarse con los electrones de otros elementos para formar moléculas más complejas.
El hidrógeno puede combinarse químicamente con casi cualquier otro elemento para formar moléculas, entre las cuales destacan el agua, los carbohidratos, los hidrocarburos, etc.
Este elemento es responsable de la formación de los enlaces conocidos como “puentes de hidrógeno”, una de las interacciones débiles más importantes para las biomoléculas y la principal fuerza responsable del mantenimiento de las estructuras tridimensionales de las proteínas y los ácidos nucleicos.
El carbono forma el núcleo de muchas biomoléculas. Sus átomos pueden combinarse covalentemente con otros cuatro átomos de elementos químicos diferentes y también consigo mismos para formar la estructura de moléculas de gran complejidad.
El carbono, junto al hidrógeno, es uno de los elementos químicos que puede formar mayor cantidad de compuestos químicos distintos. Tanto es así que todas las sustancias y compuestos catalogados como “orgánicos” contienen átomos de carbono en su estructura principal.
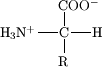
Entre las principales moléculas carbonadas de los seres vivos se encuentran los carbohidratos (azúcares o sacáridos), las proteínas y sus aminoácidos, los ácidos nucléicos (ADN y ARN), los lípidos y los ácidos grasos, entre otras.
El oxígeno es un elemento gaseoso y es el más abundante en toda la corteza terrestre. Está presente en muchos componentes orgánicos e inorgánicos y forma compuestos con casi todos los elementos químicos.
Es responsable de la oxidación de los compuestos químicos y de la combustión, que son también diferentes formas de oxidación. El oxígeno es un elemento muy electronegativo, forma parte de la molécula de agua y participa en el proceso de respiración de gran parte de los seres vivos.
Las especies reactivas de oxígeno son responsables del estrés oxidativo en el interior de las células. Es muy común observar el daño causado por los compuestos oxidantes a las macromoléculas en el interior celular, ya que estos desequilibran el interior reductor de las células.
El nitrógeno también se encuentra predominantemente en forma gaseosa, conformando cerca del 78% de la atmósfera terrestre. Es un elemento importante en la nutrición de las plantas y los animales.
En los animales, el nitrógeno es parte fundamental de los aminoácidos que, a su vez, son los bloques de construcción para las proteínas. Las proteínas estructuran los tejidos y muchas de ellas tienen la actividad enzimática necesaria para acelerar muchas de las reacciones vitales para las células.
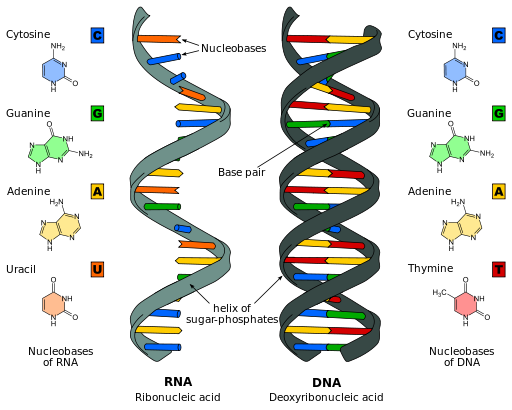
El nitrógeno está presente en las bases nitrogenadas del ADN y el ARN, moléculas esenciales para la transferencia de información genética desde los progenitores hacia la descendencia y para el funcionamiento adecuado de los organismos vivos como sistemas celulares.
La forma más abundante de este elemento en la naturaleza es como fosfatos sólidos en los suelos fértiles, ríos y lagos. Es un elemento importante para el funcionamiento de los animales y de los vegetales, pero también de las bacterias, los hongos, protozoarios y de todos los seres vivos.
En los animales, el fósforo se encuentra en abundancia en todos los huesos en forma de fosfato de calcio.
El fósforo es esencial para la vida, ya que también es un elemento que forma parte del ADN, el ARN, el ATP y los fosfolípidos (componentes fundamentales de las membranas celulares).
Este bioelemento siempre está comprometido en reacciones de transferencia de energía, ya que forma compuestos con enlaces muy energéticos, cuya hidrólisis se emplea para mover diferentes sistemas celulares.
El azufre se encuentra comúnmente en forma de sulfuros y sulfatos. Es especialmente abundante en zonas volcánicas y está presente en los residuos de los aminoácidos cisteína y metionina.
En las proteínas, los átomos de azufre de la cisteína forman una interacción intra o intermolecular muy fuerte conocida como “puente disulfuro”, que es esencial para la conformación de la estructura secundaria, terciaria y cuaternaria de las proteínas celulares.
La coenzima A, un intermediario metabólico con gran variedad de funciones, tiene en su estructura un átomo de azufre.
Dicho elemento también es fundamental en la estructura de muchos cofactores enzimáticos que participan en diferentes rutas metabólicas importantes.
Como se mencionó anteriormente, los bioelementos secundarios son aquellos que se encuentran en menor proporción que los primarios y los más importantes son el potasio, el magnesio, el hierro, el calcio, el sodio y el zinc.
Los bioelementos secundarios u oligoelementos están involucrados en muchos de los procesos fisiológicos de las plantas, en la fotosíntesis, en la respiración, en el equilibrio iónico celular de la vacuola y los cloroplastos, en el transporte de carbohidratos al floema, etc.
Esto también es cierto para los animales y otros organismos, donde estos elementos, más o menos dispensables y menos abundantes, forman parte de muchos cofactores necesarios para el funcionamiento de toda la maquinaria celular.
El hierro es uno de los bioelementos secundarios más importantes en vista de que ejerce funciones en múltiples fenómenos energéticos. Es muy importante en las reacciones naturales de óxido reducción.
En los mamíferos, por ejemplo, el hierro es parte esencial de la hemoglobina, la proteína que se encarga del transporte del oxígeno en la sangre dentro de los eritrocitos o glóbulos rojos.
En las células vegetales este elemento también forma parte de algunos pigmentos como la clorofila, fundamental para los procesos fotosintéticos. Es parte de las moléculas de citocromo, esenciales también para la respiración.
Los científicos piensan que el zinc fue uno de los elementos clave en la aparición de los organismos eucariotas hace millones de años, ya que muchas de las proteínas de unión a ADN para la replicación que componían a los “eucariotas primitivos” utilizaban el zinc como motivo de unión.
Un ejemplo de este tipo de proteínas son los dedos de zinc, que participan en la transcripción genética, la traducción de proteínas, el metabolismo y el ensamblaje de proteínas, etc.
El calcio es uno de los minerales más abundantes en el planeta tierra; en la mayoría de los animales compone dientes y huesos en la forma hidroxifosfato de calcio. Este elemento es esencial para la contracción muscular, la transmisión de impulsos nerviosos y la coagulación de la sangre.
La mayor proporción de magnesio en la naturaleza se encuentra en forma sólida combinado con otros elementos, no se encuentra solo en estado libre. El magnesio es cofactor de más 300 sistemas enzimáticos diferentes en los mamíferos.
Las reacciones en las que participa van desde la síntesis de proteínas, la movilidad muscular y la función nerviosa, hasta la regulación de los niveles de glucosa en sangre y la presión arterial. El magnesio es necesario para la producción de energía en los organismos vivos, para la fosforilación oxidativa y la glucolisis.
También contribuye al desarrollo de los huesos y es necesario para la síntesis de ADN, ARN, glutatión, entre otros.
Son dos iones muy abundantes en el interior celular y las variaciones en sus concentraciones internas y externas, así como su transporte, son determinantes para muchos procesos fisiológicos.
El potasio es el catión intracelular más abundante, mantiene el volumen líquido en el interior celular y los gradientes electroquímicos transmembranales.
Tanto el sodio como el potasio participan activamente en la transmisión de impulsos nerviosos, ya que son transportados por la bomba sodio-potasio. El sodio también participa de la contracción muscular y en la absorción de nutrientes a través de la membrana celular.
El resto de los bioelementos secundarios: el molibdeno (Mo), el flúor (F), el Cloro (Cl) el yodo (I) y el cobre (Cu) cumplen funciones importantes en muchas reacciones fisiológicas. Sin embargo, se necesitan es mucha menor proporción que los seis elementos explicados anteriormente.
- Egami, F. (1974). Minor elements and evolution. Journal of molecular evolution, 4(2), 113-120.
- Hackh, I. W. (1919). Bioelements; The Chemical Elements of the Living Matter. The Journal of general physiology, 1(4), 429
- Kaim, W., & Rall, J. (1996). Copper—a “modern” bioelement. Angewandte Chemie International Edition in English, 35(1), 43-60.
- National Institutes of Health. (2016). Magnesium: fact sheet for health professionals. Version current, 27.
- Peñuelas, J., Fernández‐Martínez, M., Ciais, P., Jou, D., Piao, S., Obersteiner, M., … & Sardans, J. (2019). The bioelements, the elementome, and the biogeochemical niche. Ecology, 100(5), e02652
- Skalny, A. V. (2014). Bioelements and Bioelementology in Pharmacology and Nutrition: Fundamental and Practical Aspects. In Pharmacology and Nutritional Intervention in the Treatment of Disease. IntechOpen.
- Solioz, M. (2018). Copper—A Modern Bioelement. In Copper and Bacteria (pp. 1-9). Springer, Cham.
- World Health Organization. (2015). Fact Sheet: Salt.
