Definición de enlace peptídico
 El término enlace tiene varios usos: en este caso nos interesa aludir a su acepción como una unión o un vínculo entre distintos elementos. Peptídico, por su parte, es aquello relacionado con los péptidos: las moléculas que se forman mediante una unión covalente de aminoácidos (sustancias orgánicas cuya composición molecular presenta un grupo carboxilo y un grupo amino).
El término enlace tiene varios usos: en este caso nos interesa aludir a su acepción como una unión o un vínculo entre distintos elementos. Peptídico, por su parte, es aquello relacionado con los péptidos: las moléculas que se forman mediante una unión covalente de aminoácidos (sustancias orgánicas cuya composición molecular presenta un grupo carboxilo y un grupo amino).
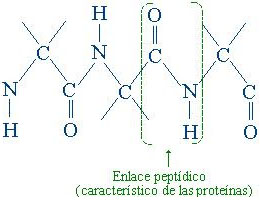
Se llama enlace peptídico al enlace químico que se establece entre el grupo carboxilo de un aminoácido y el grupo amino de otro aminoácido. Esta clase de enlace, donde se pierde una molécula de agua, permite la formación de los mencionados péptidos y de las proteínas.
Al unirse un grupo amino (-NH2) y un grupo carboxilo (-COOH) con pérdida de una molécula de agua, se establece un enlace CO-NH. El desarrollo de este enlace siempre necesita el aporte de energía; a su vez, cuando el enlace peptídico se rompe, se produce la liberación de energía.
La rotura de un enlace peptídico puede producirse a través de la hidrólisis: así se denomina al desdoblamiento que registra una molécula por intermedio del agua. La hidrólisis, en el ámbito natural, se produce de una manera muy lenta, aunque es posible acelerar el proceso haciendo uso de diversas técnicas.
En presencia del agua, un enlace peptídico se puede romper con una cantidad de energía libre que ronda los 8-16 kilojulios/mol (lo que es equivalente a 2-4 kcal/mol). La unidad kilojulio por mol, que puede simbolizarse como kJ/mol, está reconocida por el Sistema Internacional de Unidades (SI) y corresponde a la relación entre la energía y la cantidad de materia: la energía se expresa en kilojulios y la materia se mide en moles.
Los kilojulios no son más que miles de julios, otra unidad de medida reconocida por el Sistema Internacional, cuyo nombre original es joule y se usa para la medición de calor, trabajo y energía. En términos técnicos, su definición es «la cantidad de trabajo que lleva a cabo un newton con una fuerza constante a lo largo de un metro en la dirección de dicha fuerza». La unidad mol, por otro lado, se usa para medir la cantidad de una sustancia dada, y forma parte de las siete magnitudes físicas fundamentales del SI.
Para acelerar la hidrólisis de un enlace péptido, que en la naturaleza puede llegar a tardar más de un milenio, los científicos pueden escoger uno de los siguientes métodos:
* hidrólisis ácida: se consigue dejando la proteína en una ebullición durante mucho tiempo con soluciones de tipo ácido fuerte (H2SO4 y HCI). Este camino consigue la destrucción completa del triptófano y parte de la treonina y la serina;
 * hidrólisis básica: por lo general se lleva a cabo haciendo uso de BaOH o NaOH, y no destruye los aminoácidos mencionados en el método anterior;
* hidrólisis básica: por lo general se lleva a cabo haciendo uso de BaOH o NaOH, y no destruye los aminoácidos mencionados en el método anterior;
* hidrólisis enzimática: en los seres vivos, esta forma de degradar los enlaces peptídicos es la más normal. En este caso entran en acción unas enzimas proteolíticas que actúan lentamente y muchas veces no completan su trabajo, aunque tampoco se produce la destrucción de los aminoácidos ni la racemización (cuando un compuesto ópticamente activo se vuelve racémico). Este tipo de hidrólisis es muy específico;
* hidrólisis por temperatura: si las condiciones son normales, los enlaces peptídicos no se destruyen, pero la proteína sí puede desnaturalizarse (es decir que se rompan sus estructuras secundaria, terciaria y cuaternaria). Por otro lado, si se aplica una temperatura superior a los 110° durante 48 horas, sí es posible destruir los enlaces.
Cabe destacar que, por lo general, el enlace peptídico es representado como un enlace sencillo. De todas maneras, cuenta con diversas características que lo acercan a un doble enlace. Por eso los especialistas suelen mencionar que un enlace peptídico presenta propiedades que lo ubican a mitad de camino entre un enlace sencillo y un enlace doble.
