Alcanos: concepto, propiedades, tipos, nomenclatura, ejemplos
¿Qué son los alcanos?
Los alcanos son los compuestos orgánicos más simples que existen. Son hidrocarburos alifáticos saturados, formados exclusivamente por carbono e hidrógeno, en los que los carbonos están unidos únicamente por medio de enlaces covalentes simples.
Pueden ser de cadena abierta, en cuyo caso poseen la fórmula general CnH2n+2. También pueden formar uno o más ciclos, en cuyo caso la fórmula general pierde dos hidrógenos por cada ciclo que se forme (CnH2n si tienen un solo ciclo, CnH2n-2 si tienen 2, etc.).
Muchos compuestos orgánicos comunes que utilizamos todos los días son alcanos. Por ejemplo, el gas de cocina y el gas natural está formado por uno o más alcanos gaseosos. El combustible para automóviles (gasolina, bencina o carburante, dependiendo del país) está compuesto por mezclas complejas de alcanos líquidos, entre los cuales los más importantes son los isómeros del octano.
Propiedades de los alcanos
Son muy poco reactivos
La principal característica o propiedad química de los alcanos es que son moléculas bastante estables que no participan en reacciones químicas, a menos que sea en condiciones muy energéticas tales como muy altas temperaturas o en presencia de luz ultravioleta o de radicales libres.
Son compuestos apolares
Los enlaces simples C-C y C-H son enlaces covalentes apolares, por lo que las moléculas de alcanos no pueden tener un momento dipolar neto. Debido a esto, son moléculas apolares.
Tienen puntos de ebullición y de fusión bajos
Por el mismo hecho de ser apolares, las únicas fuerzas de atracción intermoleculares que presentan los alcanos son fuerzas de dispersión como las fuerzas de Van der Waals. Como estas fuerzas son muy débiles, son fáciles de romper para convertir a los sólidos a líquidos y estos a gases a baja temperatura.
Son menos densos que el agua
Los alcanos son los menos densos de los compuestos orgánicos, y siempre son menos densos que el agua. Por esta razón, siempre flotan en la superficie del agua cuando se mezclan los dos.
En general son incoloros
Los alcanos gaseosos y líquidos son incoloros y translúcidos. Sin embargo, cuando solidifican, en general forman sólidos amorfos opacos de color blanco, como en el caso de algunas parafinas y de algunos plásticos.
No son solubles en agua
La regla de oro para la solubilidad es que semejantes disuelven a semejantes. El agua es un solvente polar mientras que todos los alcanos son completamente apolares, por lo que no son solubles en agua.
Son solubles en solventes orgánicos apolares
Utilizando el mismo argumento anterior, los alcanos sí son solubles en solventes apolares tales como benceno o ciclohexano. De hecho, los alcanos líquidos forman parte de los solventes orgánicos apolares.
No pueden sufrir reacciones de adición
Al ser hidrocarburos saturados, los alcanos no pueden sufrir reacciones de adición. La única excepción es el ciclopropano que posee un anillo de solo tres miembros que está muy tensionado y se puede romper fácilmente.
Son combustibles
Una de las pocas reacciones químicas en las que participan los alcanos es en la combustión, y es justamente ese el principal uso que se les da.
Tipos de alcanos
Dependiendo de la conectividad entre los átomos de carbono, los alcanos pueden ser:
- Lineales
- Ramificados
- Cíclicos (cicloalcanos)
- Alcanos bicíclicos o policíclicos
- Espiranos
Alcanos lineales
Son los más simples de los alcanos y, por lo tanto, de todos los compuestos orgánicos. Todos tienen fórmula molecular CnH2n+2 y se caracterizan por poseer una única cadena de átomos de carbono enlazados uno después de otro.
Alcanos ramificados
También tienen fórmula general CnH2n+2 pero a diferencia de los alcanos lineales, la cadena de átomos de carbono se ramifica por lo menos en un punto. Los alcanos ramificados son isómeros de cadena de los alcanos lineales, ya que solo se diferencian en el orden en el que se encuentran enlazados los átomos de carbono.
Cicloalcanos
En los cicloalcanos, los extremos de la cadena de los alcanos lineales se unen entre sí para formar una cadena cíclica. Para formar este enlace C-C adicional es necesario eliminar un hidrógeno de cada carbono terminal, por lo que la fórmula general de estos compuestos es CnH2n. El cicloalcano más pequeño posible es el de tres átomos de carbono denominado ciclopropano (C3H6).
Al igual que los alcanos de cadena abierta que pueden tener ramificaciones, los cicloalcanos también pueden presentar grupos sustituyentes en forma de cadenas abiertas.
Alcanos bicíclicos y policíclicos
Existen muchos alcanos cíclicos en los que dos o más ciclos comparten dos o más átomos de carbono. Estos compuestos se denominan policiclos. La fórmula molecular de los policiclos depende de cuántos ciclos presente la estructura.
En el caso más sencillo, los biciclos, la fórmula es CnH2n-2 ya que se debe perder un par de hidrógenos para cerrar cada ciclo. Para los policiclos con más de dos ciclos fusionados, la fórmula será igual a la de los alcanos menos un par de hidrógenos por cada ciclo formado.
Espiranos
Los espiranos son una clase especial de biciclos en los cuales los dos ciclos comparten solo un átomo de carbono. En estos casos, los dos ciclos están en planos perpendiculares entre sí, por lo que la estructura se ve como si uno de los ciclos estuviera girado con respecto al otro.
Nomenclatura de los alcanos
Nomenclatura de los alcanos lineales
La nomenclatura de los alcanos y, de hecho, la de todos los compuestos orgánicos, se basa en la nomenclatura de los alcanos lineales. Estos se nombran simplemente según el número de átomos de carbono en la cadena.
Los primeros cuatro reciben nombres comunes que son metano, etano, propano y butano, mientras que el resto se nombran de forma sistemática anteponiendo un prefijo que indica el número de carbonos (penta, hexa, hepta, etc.) a la terminación _ano de alcano.
Número de carbonos | Fórmula molecular | Fórmula semidesarrollada | Nombre |
1 | CH4 | CH4 | Metano |
2 | C2H6 | CH3CH3 | Etano |
3 | C3H8 | CH3CH2CH3 | Propano |
4 | C4H10 | CH3(CH2)2CH3 | Butano |
5 | C5H12 | CH3(CH2)3CH3 | Pentano |
6 | C6H14 | CH3(CH2)4CH3 | Hexano |
7 | C7H16 | CH3(CH2)5CH3 | Heptano |
8 | C8H18 | CH3(CH2)6CH3 | Octano |
9 | C9H20 | CH3(CH2)7CH3 | Nonano |
10 | C10H22 | CH3(CH2)8CH3 | Decano |
Nomenclatura de los alcanos ramificados
Los alcanos ramificados se nombran en base al nombre de los alcanos lineales. El proceso involucra seleccionar una de las posibles cadenas de carbonos como la cadena principal y el resto de las ramificaciones quedan como grupos sustituyentes.
El proceso consiste en los siguientes pasos:
Paso 1: Identificar la cadena principal.
La selección se hace de acuerdo a los siguientes criterios en orden de prioridad:
- Se selecciona la cadena más larga.
- Si hay más de una, se selecciona entre ellas la que tenga más ramificaciones.
- En caso de haber más de una que tenga la misma longitud y el mismo número de ramificaciones, se selecciona la que, al numerarla, dé la combinación de localizadores más pequeña posible.
- Si dos o más cadenas tienen la misma longitud, el mismo número de ramificaciones y todas tienen los mismos localizadores, se selecciona la que le asigne los menores localizadores a las ramificaciones que aparezcan primero por orden alfabético.
- En caso de que todo lo anterior sea igual, entonces se puede elegir cualquiera.
La cadena principal le da el nombre principal al alcano, como si fuera un alcano lineal.
Paso 2: Numerar la cadena principal.
Se deben enumerar los átomos de carbono de la cadena principal en secuencia de un extremo a otro, siguiendo estas reglas:
- Se selecciona la numeración que asigne la menor combinación de localizadores a las ramificaciones.
- Si las dos numeraciones dan la misma combinación de localizadores, se selecciona la que asigne los menores localizadores a las ramificaciones que aparezcan primero en el orden alfabético.
- En caso de que ambas sean iguales, entonces da lo mismo cuál se elija.
Paso 3: Nombrar las ramificaciones y ordenarlas alfabéticamente.
Las ramificaciones se nombran como radicales alquilo, sustituyendo la terminación _ano del alcano lineal correspondiente por la terminación _ilo.
Número de carbonos | Radical alquilo | Nombre |
1 | –CH3 | Radical metilo |
2 | –CH2CH3 | " etilo |
3 | –CH2CH2CH3 | " propilo |
4 | –CH2(CH2)2CH3 | " butilo |
5 | –CH2(CH2)3CH3 | " pentilo |
6 | –CH2(CH2)4CH3 | " hexilo |
7 | –CH2(CH2)5CH3 | " heptilo |
8 | –CH2(CH2)6CH3 | " octilo |
9 | –CH2(CH2)7CH3 | " nonilo |
10 | –CH2(CH2)8CH3 | " decilo |
Paso 4: Se construye el nombre del compuesto.
El nombre se construye nombrando en orden alfabético todas las ramificaciones (suprimiéndole la letra “o” final del alquilo), precedidas por su localizador, seguidas del nombre de la cadena principal.
Si alguna ramificación se repite, se colocan los localizadores de cada una, separados por comas, y se antepone al nombre de la ramificación un prefijo que indica cuantas veces se repite (di para 2, tri para 3, y así sucesivamente).
Ejemplo:
Nombrar el siguiente alcano ramificado:

PASO 1: Selección de la cadena principal.
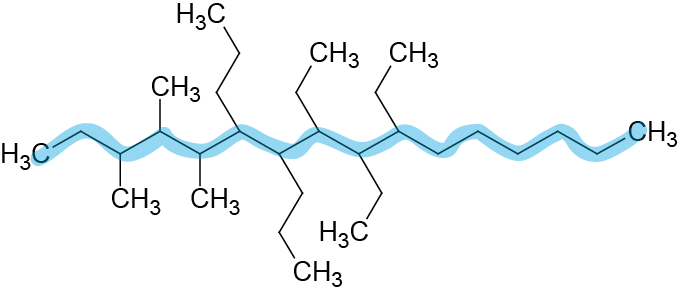
Esta cadena tiene 16 carbonos, por lo que la cadena prinicipal se llamará hexadecano.
PASO 2: Numerar cadena principal.

Se numera de izquierda a derecha porque dan los menores localizadores.
PASO 3: Nombrar todas las ramificaciones.
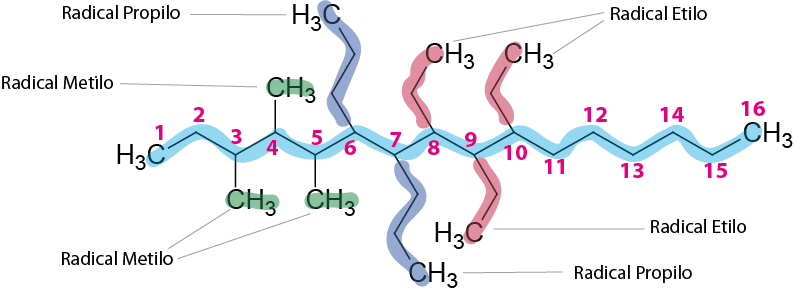
Hay tres radicales etilo, tres radicales metilo y dos radicales propilo.
PASO 4: Construir el nombre
El nombre del compuesto será:
8,9,10-trietil-3,4,5-trimetil-6,7-dipropilhexadecano
Ejemplos de alcanos
En la siguiente tabla se presentan algunos ejemplos adicionales de alcanos.
Nombre | Fórmula molecular o estructura | Radical | Número de carbonos |
Metano | CH4 | Metilo | 1 |
Etano | C2H6 | Etilo | 2 |
Propano | C3H8 | n-propilo | 3 |
n-Butano | C4H10 | n-butilo | 4 |
Isobutano | C4H10 | Isobutilo | 4 |
n-Pentano | C5H12 | n-pentilo | 5 |
Isopentano | C5H12 | Isopentilo | 5 |
Neopentano | C5H12 | Neopentilo | 5 |
n-Hexano | C6H14 | n-hexilo | 6 |
Polietileno | CH3(CH2)nCH3 | ---- | >100 |
Ciclopentano | C5H10 | Ciclopentilo | 5 |
Ciclohexano | C6H12 | ciclohexilo | 5 |
