Aminoglucósidos: clasificación, efectos, indicaciones, contraindicaciones
Los aminoglucósidos son un conjunto de antibióticos que comparten las mismas características químicas y farmacológicas. Tienen efecto bactericida contra las bacterias aeróbicas Gram negativas (bacterias que se tiñen rosado pálido y no de azul oscuro o violeta con la tinción de Gram).
El primer aminoglucósido descubierto fue la estreptomicina, en 1943. Más tarde aparecieron la tobramicina y la gentamicina como antibióticos eficaces contra Gram negativos. En la década de los setenta (1970) se desarrollaron los aminoglucósidos semisintéticos como la amikacina, la netilmicina y la dibekacina.

La mayor parte de los miembros de esta familia tiene en su estructura un aminociclitol (un alcohol cíclico con un grupo amino R-NH2) unido por un enlace glucosídico a uno o varios aminoazúcares, por lo que en realidad son aminoglucósidos-aminociclitoles.
Estos antibióticos no se absorben por vía oral, por lo que se administran por vía parenteral (intravenosa, intramuscular o subcutánea) o se usan tópicamente. Se eliminan por filtración glomerular sin ser metabolizados previamente.
Todos los miembros de esta familia muestran algún grado de nefrotoxicidad (tóxicos renales) y/o ototoxicidad (tóxicos tanto para el oído como para el sistema vestibular, pueden producir trastornos de la audición y del equilibrio).
Generalmente se usan en combinación con algún betalactámico (otra familia de antibióticos) y su uso se restringe usualmente a infecciones severas.
Estos antibióticos están contraindicados en pacientes que han desarrollado reacciones alérgicas a dichos medicamentos. Aunque pasan a la leche materna, como no se absorben por vía intestinal (oral) se consideran aptos para administrarle a la madre, de ser necesario, durante la lactancia.
Su uso durante el embarazo se permite solamente en los casos en que los beneficios clínicos superen los riesgos (categoría D de riesgo).
Índice del artículo
- 1 Mecanismo de acción
- 2 Clasificación
- 3 Efectos adversos
- 4 Resistencia a los aminoglucósidos
- 5 Indicaciones
- 6 Contraindicaciones
- 7 Referencias
Todos los aminoglucósidos inhiben la síntesis proteica de las bacterias susceptibles. Estos se adhieren a la unidad 30S de los ribosomas bacterianos e inhiben su función. A diferencia de la mayor parte de los agentes antimicrobianos que inhiben la síntesis proteica que son bacteriostáticos, estos son bactericidas.
“Bacteriostático” deriva del prefijo “bacter” que significa bacteria y “stasis” terminación griega que significa estático, sin cambio. En medicina, los agentes bacteriostáticos se utilizan para reducir el metabolismo de las bacterias y disminuir su crecimiento y reproducción.
Si el agente bacteriostático se elimina por disolución las bacterias previamente inhibidas se seguirán desarrollando. Un agente bactericida es aquel que es capaz de matar a las bacterias. Los aminoglucósidos son bactericidas.
El efecto bactericida de los aminoglucósidos es dependiente de la concentración. Los aminoglucósidos penetran al interior del espacio periplasmático de las bacterias aeróbicas Gram negativas a través de unos canales de agua llamados acuaporinas.
El transporte a través de la membrana citoplasmática depende del transporte de electrones y puede ser inhibido o bloqueado por anaerobiosis (ausencia de oxígeno), calcio, magnesio, pH ácido o hiperosmolaridad.
Una vez dentro de la célula, los aminoglucósidos se unen a los polisomas (varios ribosomas traduciendo el mismo ARNm) en la subunidad 30S. Interfieren con la síntesis proteica generando una falla de lectura y una terminación temprana del proceso de traducción del ARNm.
Esto genera unas proteínas defectuosas que al insertarse en la membrana celular alteran su permeabilidad, lo que facilitará luego la entrada subsiguiente de estos antibióticos. Posteriormente se observan fugas de iones, seguidos de moléculas más grandes hasta que, previo a la muerte de la bacteria, se pierden las proteínas.
Los aminoglucósidos se clasifican en dos grandes grupos según tengan un aminociclitol con o sin componente aminoglucósido: aminoglucósidos con aminociclitol y aminociclitol sin aminoglucósido.
En el primer grupo, que son los que contienen aminociclitol con componente aminoglucósido, existen dos subgrupos. Estos subgrupos se forman por los diferentes componentes de aminociclitol: la estreptidina y la desoxiestreptamina
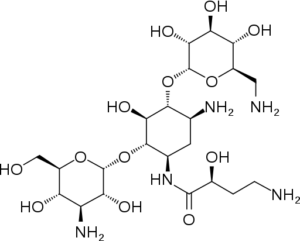
Así pues, existe un subgrupo con el aminociclitol estreptidina y otro con el aminociclitol desoxiestreptamina. A continuación, se muestran los aminoglucósidos más importantes de cada grupo.
Aminociclitol estreptidina: Estreptomicina
Aminociclitol desoxiestreptamina: dentro de este grupo están las familias Kanamicina, Gentamicina y otras.
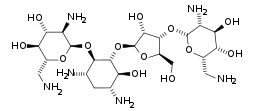
Familia Kanamicina:
– Kanamicina
– Amikacina
– Tobramicina
– Dibekacina
Familia Gentamicina:
– Gentamicina
– Sisomicina
– Netilmicina
– Isepamicina
Otros:
– Neomicina
– Paromomicina
Todos los aminoglucósidos son potencialmente tóxicos para el sistema renal, el aparato auditivo y el sistema vestibular. Estos efectos tóxicos pueden ser reversibles o irreversibles. Dichas consecuencias secundarias adversas dificultan la administración y el uso de estos antibióticos.
Cuando se necesita suministrar un aminoglucósido por tiempos prolongados y a dosis altas es necesario monitorear la función auditiva, vestibular y renal, ya que en etapas iniciales estos daños son reversibles.
Al administrarse aminoglucósidos puede ocurrir disfunción tanto del aparato auditivo como del sistema vestibular. Estas drogas se acumulan y concentran en la perilinfa y en la endolinfa del oído interno, sobre todo cuando se utilizan dosis altas.
La difusión desde estos líquidos del oído otra vez hacia el plasma es muy lenta, y la vida media de los aminoglucósidos en el oído es de 5 a 6 veces mayor que en el plasma sanguíneo. La ototoxicidad es más frecuente en aquellos pacientes que tienen concentraciones plasmáticas persistentemente altas.
Con dosis bajas se observan daños en las células sensoriales del órgano vestibular y de la cóclea, afectándose los extremos (estereocilios) de las células ciliadas. Con dosis más altas se observan daños basales en dichas células, hasta generar destrucción de las células sensoriales.
Cuando se destruyen las células sensoriales el efecto es irreversible y consecuentemente ocurren pérdidas auditivas permanentes. Como se pierden células sensoriales cocleares con la edad, los pacientes ancianos son más susceptibles a la ototoxicidad con el uso estos antibióticos.
Drogas como la furosemida o el ácidoetacrínico potencian el efecto ototóxico de los aminoglucósidos. Ambas drogas son diuréticos de asa (aumentan la emisión de orina) usados para el tratamiento de la hipertensión arterial y el edema.
A pesar de que todos los aminoglucósidos pueden afectar tanto la función coclear como la vestibular, existe una toxicidad preferencial evidente.
Así pues, la estreptomicina y la gentamicina afectan preferentemente al sistema vestibular, en cambio, la amikacina, kanamicina y la neomicina afectan primariamente la función auditiva y la tobramicina afecta ambas funciones por igual.
Síntomas de la ototoxicidad coclear
Como primer síntoma de ototoxicidad suelen presentarse tinitus (silbido o zumbido no asociado a algún sonido proveniente del exterior) de alta frecuencia. Si no se suspende el tratamiento, en pocos días el daño será permanente.
El tinitus puede perdurar hasta por dos semanas, y como lo que primero se pierde es la percepción de sonidos de alta frecuencia, el paciente no se percata inicialmente de su pérdida auditiva. Si bajo estas condiciones sigue el tratamiento, la pérdida auditiva progresa hasta desarrollar problemas para conversar.
Síntomas de la ototoxicidad vestibular
Inicialmente aparece dolor de cabeza de moderada intensidad. Luego aparecen vómitos, náuseas y problemas de equilibrio postural que pueden persistir por una a dos semanas. Los síntomas más prominentes son el vértigo en posición erecta, con dificultad para sentarse o pararse sin señales visuales.
Los síntomas agudos ceden bruscamente y son reemplazados por manifestaciones de laberintitis crónica por un periodo de aproximadamente dos meses. Progresivamente ocurre una compensación y luego solo aparecen los síntomas al cerrar los ojos. La recuperación de esta fase requiere de 12 a 18 meses.
La mayoría de estos pacientes quedan con algún grado de daño residual permanente. Como no existe un tratamiento específico para el daño vestibular, la suspensión del aminoglucósido ante las primeras manifestaciones clínicas es la única medida eficiente para evitar las lesiones permanentes.
Aproximadamente del 8 al 25% de los pacientes que reciben tratamiento con algún aminoglucósido por varios días desarrollan alguna alteración renal reversible. Esta toxicidad es el resultado de la acumulación, concentración y retención de los aminoglucósidos en las células del túbulo proximal renal.
Consecuentemente, se altera la estructura y función del túbulo proximal. Inicialmente aparece proteinuria moderada y cilindros hialinos en la orina. Luego de varios días aparece una reducción del volumen de filtración glomerular con un ligero incremento en los valores plasmáticos de creatinina.
Las alteraciones renales son muchas veces reversibles, ya que el túbulo proximal tiene capacidad de regeneración. La toxicidad renal depende de la cantidad total suministrada y depende del aminoglucósido utilizado.
La neomicina es uno de los aminoglucósidos que exhibe mayor toxicidad renal, ya que se concentra en la corteza renal en cantidades mucho mayores que los demás aminoglucósidos.
Se han descrito otros efectos tóxicos menos frecuentes, entre ellos está el bloqueo neuromuscular que puede causar problemas respiratorios y/o parálisis en algunos músculos. Alteraciones de la función del nervio óptico con aparición de escotomas, que son zonas de ceguera transitorias, y neuritis periféricas.
La resistencia de los microorganismos a los aminoglucósidos puede deberse a alguna de las siguientes causas: 1) Las membranas de la bacteria son impermeables a estos antibióticos 2) los ribosomas de estas bacterias tienen una baja afinidad por el antibiótico 3) las bacterias sintetizan enzimas que inactivan al aminoglucósido.
Las dos primeras causas explican las resistencias naturales a los aminoglucósidos. En cambio, la inactivación enzimática permite explicar la resistencia adquirida que se ha descrito clínicamente con el uso de aminoglucósidos.
Los genes para la síntesis de estas enzimas se transmiten a través de plásmidos. Los plásmidos son estructuras circulares de ADN extracromosómico. Estos plásmidos están ampliamente distribuidos en la naturaleza, pero sobretodo en las bacterias alrededor de los ambientes hospitalarios.
Los plásmidos codifican para muchas enzimas y estas inactivan a los aminoglucósidos. Como las enzimas que inactivan a cada aminoglucósido son diferentes, la resistencia para uno no necesariamente ocasiona resistencia para otro.
Sin embargo, si bien esto es cierto para la estreptomicina y la gentamicina, en el caso de la resistencia a la gentamicina (como la enzima que la causa es bifuncional) se presentará concomitantemente resistencia a la tobramicina, amikacina, kanamicina y netilmicina.
Aunque se han desarrollado antibióticos menos tóxicos, el uso de los aminoglucósidos sigue siendo una herramienta importante para combatir infecciones severas causadas por enterococos o estreptococos.
La gentamicina, la amikacina, la tobramicina y netilmicina tienen un espectro amplio contra bacterias aeróbicas Gram negativas. La kanamicina y la estreptomicina tienen un espectro más reducido y no deben usarse para Pseudomonas aeruginosa o Serratia spp.
La gentamicina se usa junto con penicilina o con vancomicina para estreptococos y enterococos. La tobramicina se utiliza para Pseudomonas aeruginosa y algunas especies de Proteus. Para las infecciones nosocomiales (infecciones hospitalarias) se usa amikacina y netilmicina.
Si bien lo expuesto anteriormente representa las indicaciones más frecuentes de los aminoglucósidos, el uso racional de estos antibióticos debe hacerse en función del cultivo y antibiograma del agente agresor.
Los aminoglucósidos están contraindicados en pacientes con reacciones alérgicas a estos antibióticos. No deben usarse en los casos de enfermedades causadas por gérmenes que son resistentes. No deben usarse durante el embarazo si existen alternativas menos tóxicas.
Existen contraindicaciones relativas en pacientes con enfermedades renales y/o problemas auditivos.
- Boussekey, N., & Alfandari, S. (2007). Aminoglucósidos. EMC-Tratado de Medicina, 11(1), 1-4.
- Durante-Mangoni, E., Grammatikos, A., Utili, R., & Falagas, M. E. (2009). Do we still need the aminoglycosides? International journal of antimicrobial agents, 33(3), 201-205.
- Goodman and Gilman, A. (2001). The pharmacological basis of therapeutics. Tenth edition. McGraw-Hill
- Kotra, L. P., Haddad, J., & Mobashery, S. (2000). Aminoglycosides: perspectives on mechanisms of action and resistance and strategies to counter resistance. Antimicrobial agents and chemotherapy, 44(12), 3249-3256.
- Meyers, F. H., Jawetz, E., Goldfien, A., & Schaubert, L. V. (1978). Review of medical pharmacology. Lange Medical Publications.
- Palomino, J., and Pachon, J. (2003) Aminoglycosides, Enfermedades infecciosas y microbiología clínica 21(2),105-115.
- Rodríguez-Julbe, M. C., Ramírez-Ronda, C. H., Arroyo, E., Maldonado, G., Saavedra, S., Meléndez, B., … & Figueroa, J. (2004). Antibiotics in older adults. Puerto Rico health sciences journal, 23(1).
