Exonucleasa: características, estructura y funciones
Las exonucleasas son un tipo de nucleasas que digieren a los ácidos nucleicos por uno de sus extremos libres – ya sea el 3’ o el 5’. El resultado es una digestión progresiva del material genético, liberando uno a uno los nucleótidos. La contraparte a estas enzimas son las endonucleasas, que hidrolizan a los ácidos nucleicos en secciones internas de la cadena.
Estas enzimas actúan mediante la hidrólisis de los enlaces fosfodiéster de la cadena de nucleótidos. Participan en el mantenimiento de la estabilidad del genoma y en varios aspectos del metabolismo celular.
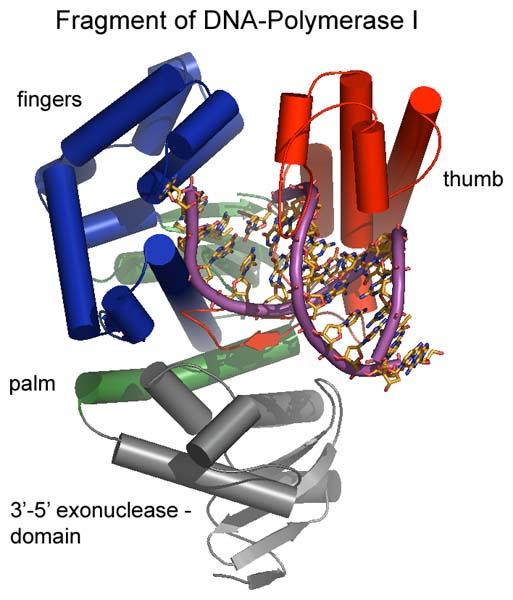
Específicamente, tanto en los linajes procariotas como en los eucariotas encontramos distintos tipos de exonucleasas que participan en la replicación y reparación del ADN y en la maduración y degradación del ARN.
Índice del artículo
Las exonucleasas son un tipo de nucleasas que hidrolizan los enlaces fosfodiéster de las cadenas de ácidos nucleicos de manera progresiva por alguno de sus extremos, ya sea el 3’ o el 5’.
Un enlace fosfodiéster se encuentra formado por la unión covalente entre un grupo hidroxilo ubicado en el carbono 3’ y un grupo fosfato localizado en el carbono 5’. La unión entre ambos grupos químicos se traduce en un doble enlace del tipo éster. La función de las exonucleasas – y de las nucleasas en general – es romper estos enlaces químicos.
Existe una gran variedad de exonucleasas. Estas enzimas pueden usar como sustrato al ADN o al ARN, dependiendo del tipo de nucleasa. Del mismo modo, la molécula puede estar en simple o en doble banda.
Uno de los aspectos críticos para mantener en condiciones óptimas la vida de un organismo es la estabilidad del genoma. Afortunadamente, el material genético cuenta con una serie de mecanismos muy efectivos que permiten su reparación, en caso de verse afectado.
Estos mecanismos requieren de la ruptura controlada de los enlaces fosfodiéster, y, como mencionamos, las nucleasas son las enzimas que cumplen esta función vital.
Las polimerasas son enzimas presentes tanto en eucariotas como en procariotas que participan en la síntesis de los ácidos nucleicos. En bacterias, se han caracterizado tres tipos y en eucariotas cinco. En estas enzimas la actividad de las exonucleasas es necesaria para cumplir sus funciones. A continuación veremos cómo lo logran.
En las bacterias, las tres polimerasas presentan actividad exonucleasas. La polimerasa I tiene actividad en dos direcciones: 5’-3’ y 3’-5’, mientras que la II y la III solamente presenten actividad en sentido 3’-5’.
La actividad 5’-3’ permite que la enzima retire el primer del ARN, añadido por una enzima denominada primasa. Posteriormente, la brecha creada será rellenada con nucleótidos recién sintetizados.
El primer es un molécula formada por unos pocos nucleótidos que permite dar inicio a la actividad de la ADN polimerasa. Por lo que siempre estará presente en el evento de replicación.
En caso de que la ADN polimerasa añada un nucleótido que no corresponde, puede corregirlo gracias a la actividad de la exonucleasa.
Las cinco polimerasas en estos organismos se denotan usando letras griegas. Solamente la gamma, delta y épsilon presentan actividad exonucleasa, todas en dirección 3’-5’.
La ADN polimerasa gamma se relacionada con la replicación del ADN mitocondrial, mientras que las dos restantes participan en la replicación del material genético ubicado en el núcleo y en la reparación del mismo.
Las exonucleasas son enzimas claves en eliminar ciertas moléculas de ácidos nucleicos que ya no son necesarias para el organismo.
En algunos casos, la célula debe evitar que la acción de estas enzimas afecte a los ácidos nucleicos que sí deben ser conservados.
Por ejemplo, en el ARN mensajero se añade una “caperuza”. Esta consiste en la metilación de una guanina terminal y dos unidades de ribosa. Se cree que la función de la caperuza es la protección del ADN frente a la acción de la exonucleasa 5’.
Una de las exonucleasas esenciales para el mantenimiento de la estabilidad genética es la exonucleasa humana I, abreviada como hExo1. Esta enzima se encuentra en distintas rutas de reparación del ADN. Es relevante para el mantenimiento de los telómeros.
Esta exonucleasa permite el arreglo de las brechas en ambas cadenas, que, en caso de no ser reparadas, pueden llevar a rearreglos cromosomales o deleciones que se traducen en un paciente con cáncer o envejecimiento prematuro.
Algunas exonucleasas son de uso comercial. Por ejemplo la exonucleasa I que permite la degradación de primers en banda simple (no puede degradar sustratos en doble banda), la exonucleasa III se usa para la mutagénesis sitio-dirigida y la exonucleasa lambda puede usarse para la remoción de un nucleótido ubicado en el extremo 5’ de un ADN doble banda.
Históricamente, las exonucleasas fueron elementos determinantes en el proceso de dilucidar la naturaleza de los enlaces que mantenían unidos a los bloques estructurales de los ácidos nucleicos: los nucleótidos.
Además, en algunas técnicas antiguas de secuenciación se acoplaba la acción de las exonucleasas con el uso de la espectrometría de masas.
Como el producto de la exonucleasa es la liberación progresiva de oligonucleótidos, representaba una herramienta conveniente para el análisis de la secuencia. Aunque el método no funcionaba muy bien, era útil para secuencias cortas.
De esta manera, las exonucleasas son consideradas como herramientas muy flexibles e inestimables en el laboratorio para la manipulación de los ácidos nucleicos.
Las exonucleasas tienen una estructura extremadamente variada, por lo que no es posible generalizar sus características. Lo mismo se puede extrapolar para los distintos tipos de nucleasas que encontramos en los organismos vivos. Por ello, describiremos la estructura de una enzima puntual.
La exonucleasa I (ExoI) tomada del organismo modelo Escherichia coli es una enzima monomérica, implicada en la recombinación y reparación del material genético. Gracias a la aplicación de técnicas cristalográficas se logró ilustrar su estructura.
Además del dominio exonucleasa de la polimerasa, la enzima incluye otros dominios denominados SH3. Las tres regiones se combinan de manera que forman una especie de C, aunque algunos segmentos hacen lucir a la enzima similar a uno O.
- Breyer, W. A., & Matthews, B. W. (2000). Structure of Escherichia coli exonuclease I suggests how processivity is achieved. Nature Structural & Molecular Biology, 7(12), 1125.
- Brown, T. (2011). Introduction to genetics: A molecular approach. Garland Science.
- Davidson, J., & Adams, R. L. P. (1980). Bioquímica de los ácidos nucleicos de Davidson. Reverté.
- Hsiao, Y. Y., Duh, Y., Chen, Y. P., Wang, Y. T., & Yuan, H. S. (2012). How an exonuclease decides where to stop in trimming of nucleic acids: crystal structures of RNase T–product complexes. Nucleic acids research, 40(16), 8144-8154.
- Khare, V., & Eckert, K. A. (2002). The proofreading 3′→ 5′ exonuclease activity of DNA polymerases: a kinetic barrier to translesion DNA synthesis. Mutation Research/Fundamental and Molecular Mechanisms of Mutagenesis, 510(1-2), 45–54.
- Kolodner, R. D., & Marsischky, G. T. (1999). Eukaryotic DNA mismatch repair. Current opinion in genetics & development, 9(1), 89–96.
- Nishino, T., & Morikawa, K. (2002). Structure and function of nucleases in DNA repair: shape, grip, and blade of the DNA scissors. Oncogene, 21(58), 9022.
- Orans, J., McSweeney, E. A., Iyer, R. R., Hast, M. A., Hellinga, H. W., Modrich, P., & Beese, L. S. (2011). Structures of human exonuclease 1 DNA complexes suggest a unified mechanism for nuclease family. Cell, 145(2), 212–223.
- Yang, W. (2011). Nucleases: diversity of structure, function, and mechanism. Quarterly reviews of Biophysics, 44(1), 1-93.
