Hidrocarburos aromáticos: propiedades, ejemplos, aplicaciones
Los hidrocarburos aromáticos o arenos son un conjunto de compuestos orgánicos que se componen únicamente de carbonos e hidrógenos, y que se caracterizan por tener unidades de anillos bencénicos en sus estructuras moleculares.
Algunos, tal como recalca su nombre, despiden olores dulces y agradables; razón por la que los primeros químicos orgánicos se referían a ellos como aromáticos. El gas metano, por ejemplo, es un hidrocarburo inodoro; mientras que el tolueno, líquido volátil, presenta un olor bastante peculiar y fuerte.
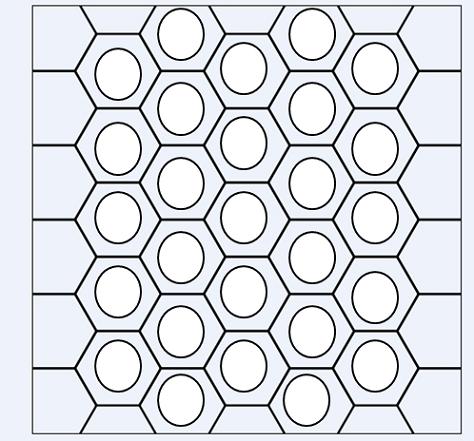
En la imagen superior tenemos una especie de red o malla compuestas por anillos bencénicos. Nótese sus geometrías hexagonales y el círculo en su interior. Este círculo representa lo que se conoce como aromaticidad, la cual es una propiedad enteramente química y no física, independiente de los olores de estos hidrocarburos.
Los hidrocarburos aromáticos están entre las sustancias más importantes, extraídas o producidas, del petróleo y los minerales del carbono. El benceno es la piedra angular de estos hidrocarburos y sus aplicaciones, pues de él derivan sinfines de compuestos que se utilizan como materia prima para la producción de fertilizantes, plásticos, adhesivos, detergentes, perfumes, medicamentos, etc.
Índice del artículo
- 1 ¿Cómo se nombran los hidrocarburos aromáticos?
- 2 Propiedades de los hidrocarburos aromáticos
- 3 Ejemplos de hidrocarburos aromáticos
- 4 Aplicaciones/usos
- 5 Referencias
Para los hidrocarburos aromáticos tenemos la particularidad de que sus nombres tradicionales, o comunes, suelen prevalecer sobre los regidos por la nomenclatura IUPAC.
Todos contienen el anillo bencénico, o un anillo que cumpla con la propiedad de aromaticidad. Los más simples pueden nombrarse en función del benceno y las posiciones relativas de sus sustituyentes.
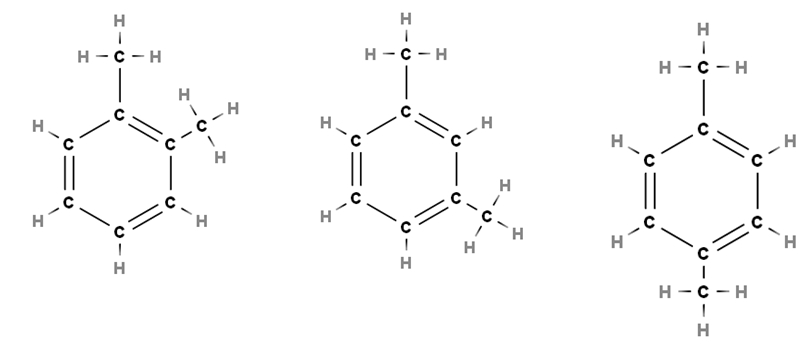
Por ejemplo, considérese la imagen superior. En las tres estructuras vemos el anillo hexagonal del benceno, el cual posee dos sustituyentes metilos, CH3. Así, este compuesto se llama dimetilbenceno, pues consta de un benceno con dos metilos.
De izquierda a derecha, vemos que la separación entre ambos CH3 se hace mayor, lo cual no solo afecta las propiedades físicas de la molécula, sino también modifica sus respectivos nombres. Para poder diferenciarlas, ya que todas se llaman dimetilbenceno, se utilizan los prefijos orto (o-), meta (m-) y para (p-).
Por lo tanto, y nuevamente, de izquierda a derecha tenemos: orto-dimetilbenceno, meta-dimetilbenceno y para-dimetilbenceno. Sin embargo, el nombre tradicional para este compuesto es el xileno, por lo que los nombres vienen a ser: orto-xileno, meta-xileno y para-xileno.
Si hay más de dos sustituyentes diferentes, se recurre a enumerar los carbonos siguiendo las mismas reglas de nomenclatura que para todos los hidrocarburos.
Para los hidrocarburos aromáticos con más de un anillo bencénico, los nombres tradicionales se vuelven todavía más importantes. Esto se debe porque los nombres sistemáticos que describen sus estructuras son engorrosos y difíciles de memorizar. Considérese el ejemplo del naftaleno:
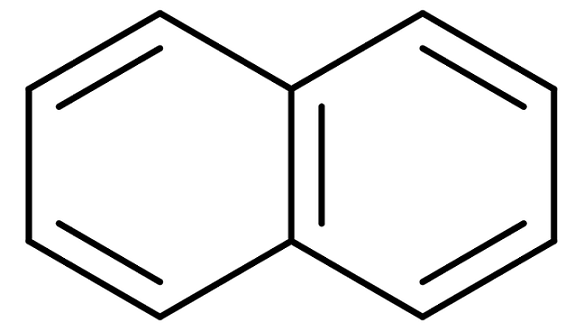
Al naftaleno también se le conoce comercialmente como naftalina o alcanfor blanco. Sin embargo, su nombre sistemático es: Biciclo [4,4,0] deca-1,3,5,7,9 pentaeno. Y esto solamente para un compuesto con dos anillos bencénicos fusionados; la nomenclatura se torna mucho más complicada para compuestos con tres o más anillos.
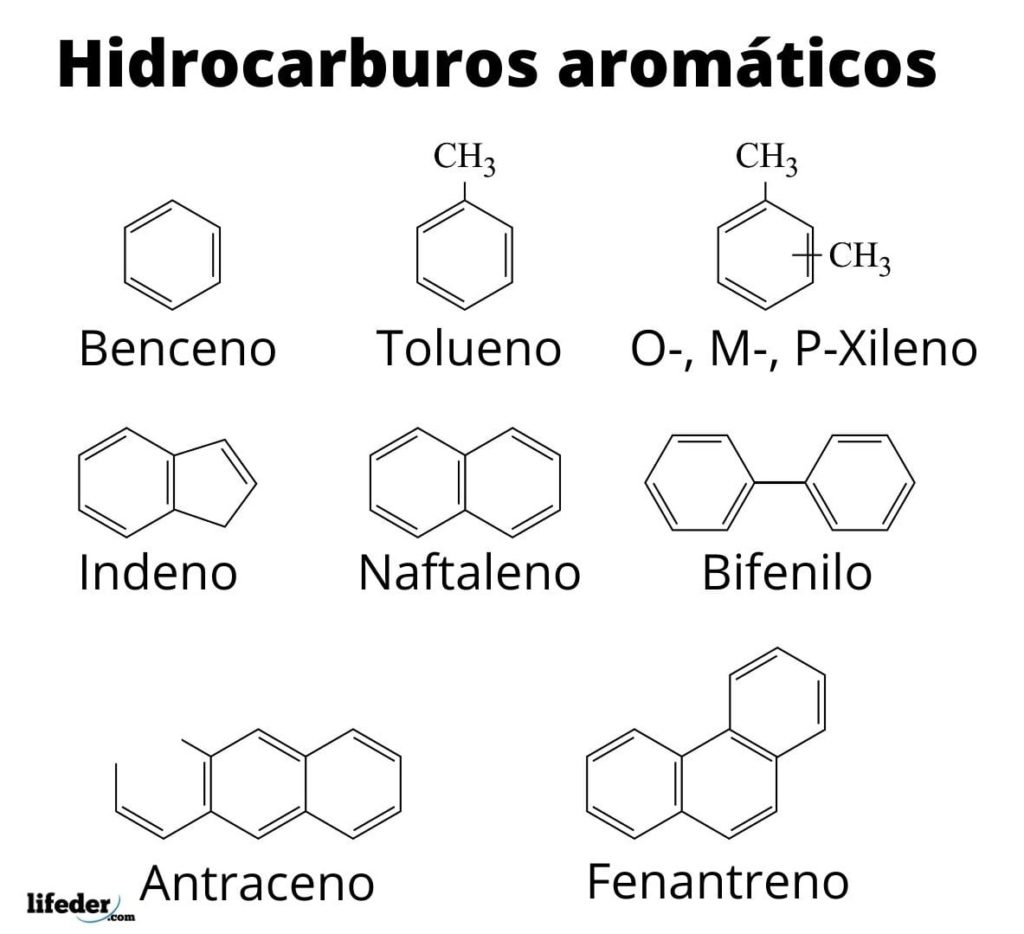
Los hidrocarburos aromáticos contienen anillos que obedecen las reglas de Huckel. Es decir, sus anillos deben poseer átomos con hibridaciones sp2, ser lo más plano posible, y tener un número de electrones π deslocalizados igual a 4n + 2. Por ejemplo, el benceno es aromático porque tiene 6 electrones deslocalizados para n=1 (4·1 + 2= 6).
Las relaciones C/H para los hidrocarburos aromáticos son altas o superiores a 1. Por ejemplo, para el benceno, C6H6, su C/H es igual a 6/6 o 1. Mientras, para el naftaleno, C10H8, su C/H es igual a 10/8 o 1.25. ¿Qué significa esto? Que estos hidrocarburos están muy “carbonados” en comparación a otros compuestos.
Precisamente a causa de sus relaciones C/H altas, cuando se queman los hidrocarburos aromáticos despiden llamas amarillentas, producto de las partículas de carbón formadas (hollín).
Los hidrocarburos aromáticos pueden sustituir sus átomos de hidrógeno por cualquier otro sustituyente. Esto se logra mediante dos tipos de reacciones orgánicas: la sustitución electrofílica aromática (SEAr), o la sustitución nucleofílica aromática (SNAr).
Los hidrocarburos aromáticos, como su nombre sugiere, se caracterizan por tener olores dulces o fuertes. Esta propiedad permitió diferenciarlos, en principio, de los hidrocarburos gaseosos y de algunas parafinas cerosas.
Los hidrocarburos aromáticos, estrictamente hablando, atañen solo a aquellos que se componen de carbono e hidrógeno. No debe haber heteroátomos (O, P, N, S, etc.). Por lo tanto, los siguientes ejemplos que se mencionarán dejan por fuera a compuestos tales como la piridina, el furano o el fenol.
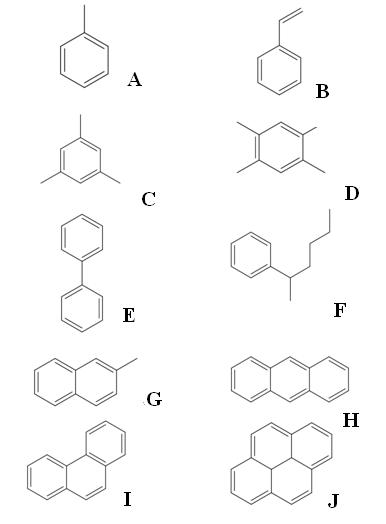
Arriba tenemos diez ejemplos de hidrocarburos aromáticos. Nótese que todos poseen por lo menos un anillo bencénico. Sus nombres son:
A: Tolueno
B: Estireno
C: Mesitileno
D: Dureno
E: Bifenilo
F: 2-Fenilhexano
G: 2-Metilnaftaleno
H: Antraceno
I: Fenantreno
J: Pireno
De todos ellos, el tolueno es el de mayor valor industrial.
La mayoría de las aplicaciones de los hidrocarburos aromáticos consiste en servir como materia prima para la síntesis, o producción, de productos con alto valor comercial. Casi todas ellas parten del benceno, al cual se le somete a varias reacciones orgánicas para obtener derivados funcionales.
Del benceno se produce ciclohexano, que posteriormente se transforma en otros compuestos para sintetizar el nylon 6 o nylon 66. Por otro lado, del benceno también puede obtenerse el estireno, que consiste en el monómero del poliestireno. Así, tenemos polímeros necesarios para la producción de fibras y plásticos.
Del benceno, asimismo, puede sintetizarse el bisfenol A, con el cual, siguiendo diversas rutas de síntesis, se producen resinas epóxicas, pegamentos, adhesivos, e inclusive pinturas.
Los alquilbencenos con largas cadenas laterales sirven para la producción de detergentes; entre ellos, los alquilbencenosulfonatos.
A partir del tolueno se puede producir TNT: trinitrotolueno, uno de los explosivos más conocidos.
Del tolueno se obtiene como derivado el ácido benzoico, compuesto esencial para las formulaciones de muchos perfumes, medicinas y alimentos.
El benceno, tolueno y xileno (BTX), son los solventes orgánicos más utilizados en las investigaciones del petróleo.
Los hidrocarburos aromáticos también forman parte de la composición de la gasolina, teniendo como rol principal el elevar su índice de octano u octanaje.
- Graham Solomons T.W., Craig B. Fryhle. (2011). Organic Chemistry. (10th edition.). Wiley Plus.
- Carey F. (2008). Química Orgánica. (Sexta edición). Mc Graw Hill.
- Morrison y Boyd. (1987). Química orgánica. (Quinta edición). Addison-Wesley Iberoamericana.
- Wikipedia. (2020). Aromatic compound. Recuperado de: en.wikipedia.org
- Ed Vitz et al. (08 de septiembre de 2020). Aromatic Hydrocarbons. Chemistry LibreTexts. Recuperado de: chem.libretexts.org
- Wyman Elizabeth. (2020). Aromatic Hydrocarbons: Definition, Examples & Uses. Study. Recuperado de: study.com
- Boluda, C. J., Macías, M., & González Marrero, J. (2019). La complejidad química de las gasolinas de automoción. Ciencia, Ingenierías y Aplicaciones, 2(2), 51-79. Doi: doi.org/10.22206/cyap.2019.v2i2.pp51-79
