Nivel químico: definición, características y ejemplos
¿Qué es el nivel químico?
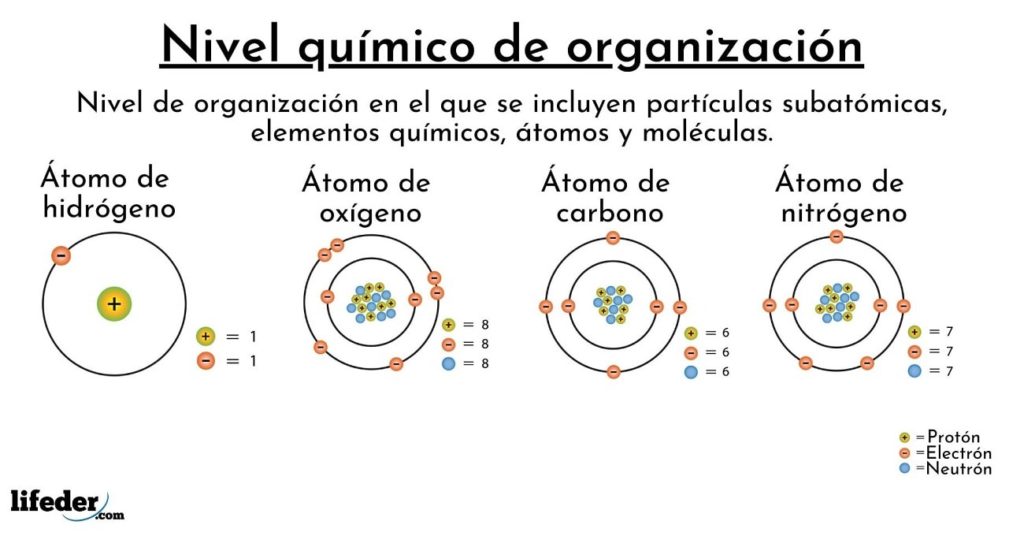
El nivel químico es el escalón más simple y básico en el que se organiza la materia, y comprende lo que entendemos por elementos químicos, átomos, moléculas, etc. Debido a que se trata del nivel más básico de la materia, es el mismo para todos los rincones del Cosmos, aplicando tanto en la Tierra como en otros planetas y galaxias.
Los átomos de hidrógeno que tenemos en el cuerpo, por ejemplo, son idénticos (en lo que respecta al núcleo) a los que se encuentran en las estrellas, como el Sol. Asimismo, nuestros átomos de carbono no difieren de los que forman parte de los hidrocarburos del petróleo, pues el que estemos vivos no modifica los núcleos ni las características electrónicas (valencias) de dichos átomos.
Hablar del nivel químico es referirse y recorrer la tabla periódica, conocerse sus 118 elementos, los átomos de tales elementos, sus uniones o interacciones para originar moléculas pequeñas o grandes, y luego sus aglomeraciones y conexiones en el nivel biológico.
Todos los seres vivos tenemos en principio el mismo nivel químico, el cual se basa en el átomo de carbono y el agua, con pequeñas pero esenciales variaciones que definen el fenómeno de la vida; aquí en la Tierra, y también fuera de ella.
Características del nivel químico
El nivel de organización químico tiene varias características:
Es invariable
El nivel químico se caracteriza por ser invariable, ya que depende de los núcleos atómicos, que son los encargados de definir la identidad de un elemento químico.
Cada elemento tiene un átomo con su propio núcleo personal o distintivo; unos más pequeños y livianos (como el de hidrógeno), y otros más pesados e inestables (como el de plomo o uranio).
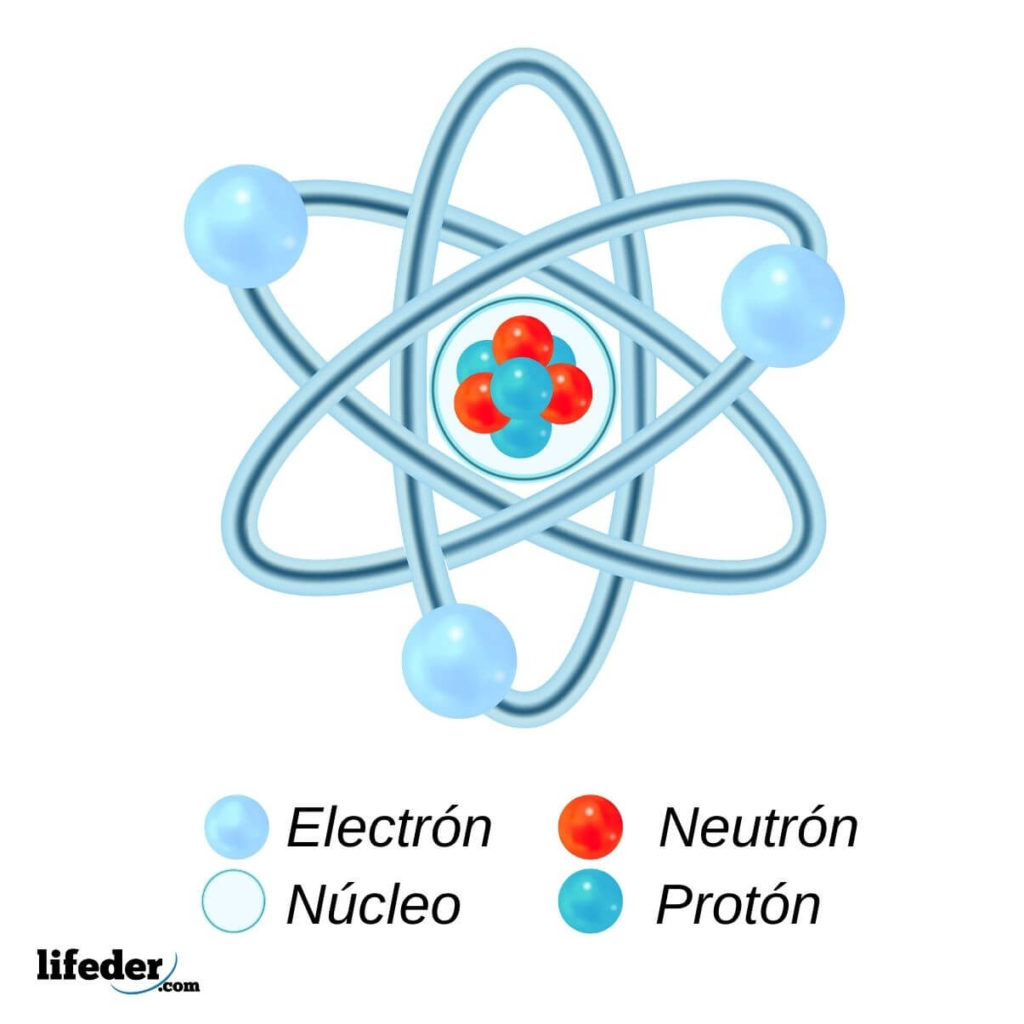
Los núcleos atómicos, y por lo tanto los átomos de los elementos, son los mismos en todas las partes del Universo. Lo que sí cambia es el modo en que se combinan o unen para formar moléculas. Y aun así, las moléculas, aunque muy variables, también son las mismas en cualquier lugar donde se consideren.
Por ejemplo, las moléculas de agua de nuestro cuerpo, H2O, son exactamente las mismas que se descubrieron recientemente en la Luna, o las mismas que se desprenden como vapor de agua en las colas de los cometas.
Es muy pequeño
El nivel químico puede manifestarse en distintas escalas, pero su naturaleza será la misma, pues es invariable.
Volvamos al agua. Una gota de agua pura, químicamente hablando, es idéntica a una cascada, un río, un océano, o todo un planeta formado por esta misma agua (si ignoramos las sales disueltas, los microorganismos o la fauna marina).
El nivel químico del agua se reduce a su simple molécula de H2O, la cual es extraordinariamente pequeña: tiene un diámetro de 0.27 nanómetros (esos son 0.00000000027 metros).
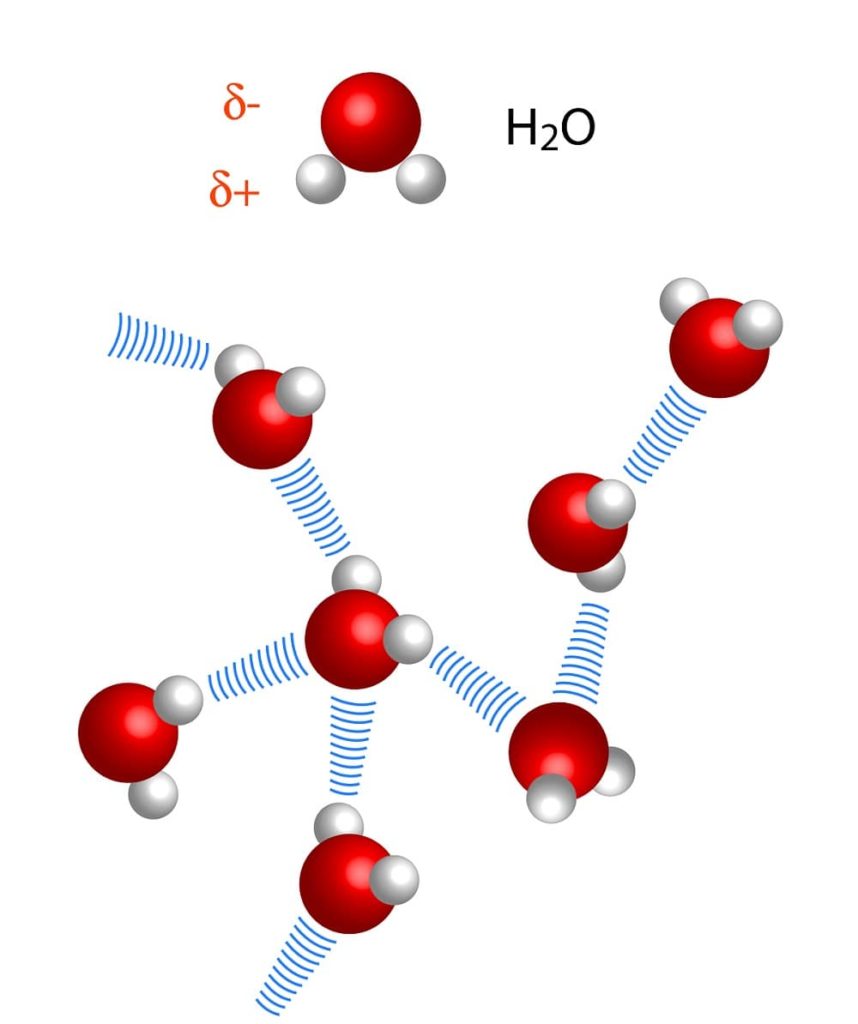
Por lo tanto, dado que los componentes del nivel químico (átomos, moléculas, neutrones, etc.) son increíblemente pequeños, este siempre se describe a escalas muy pequeñas y con unidades tales como nanómetros (nm) o picómetros (pm).
Es definitorio
El nivel químico es invariable, pequeño y, además definitorio. Es decir, el nivel químico es el responsable de definir las propiedades físicas y químicas de las sustancias que conocemos hoy en día. No es lo mismo, por ejemplo, una moneda de cobre (Cu) compuesta por átomos de cobre, que un cristal de cuarzo, compuesto por redes ordenadas de sílice (SiO2).
No obstante, en lo que concierne a la vida, la situación se vuelve compleja, siendo necesario enfoques más apropiados del nivel biológico (como el ADN y sus genes).
Está en todas partes
Y finalmente, el nivel químico, como es de esperarse, está en todas partes: cualquier manifestación de la materia se debe gracias a la masa de sus átomos.
Biológicas
El nivel químico sustenta la vida y las células mediante átomos que interaccionan de manera excepcionalmente fuerte y estable. Hablamos de los átomos de carbono, los cuales se enlazan para formar cadenas o unidades C-C difíciles de romper. Asimismo, tenemos moléculas muy estables como la del agua, que compone el 60% de nuestros cuerpos.
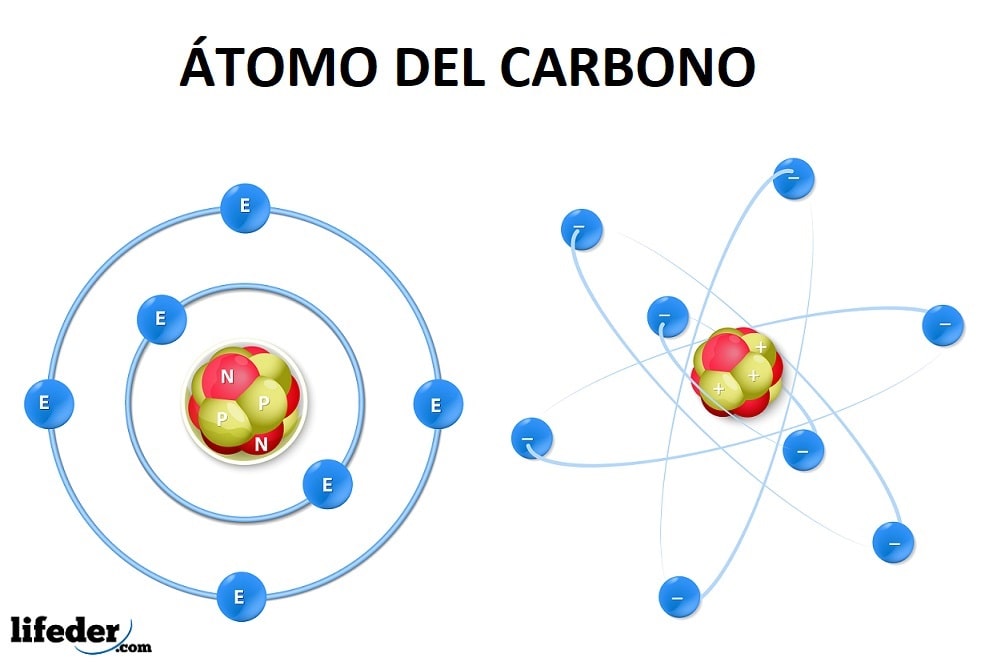
Muchos de los elementos de la tabla periódica se encuentran en los seres vivos, pero no todos juegan un papel esencial para su funcionamiento.
Por ejemplo, en los seres vivos el nitrógeno (N) está presente en las proteínas y enzimas, así como el calcio (Ca) y el magnesio (Mg) en los huesos y tejidos, o el potasio (K) en las neuronas, el fósforo (P) en las moléculas de ATP, y el hierro (Fe) en la hemoglobina como facilitador del transporte del oxígeno a través de la sangre.
Ejemplos del nivel químico de organización
Aclarado qué es el nivel químico y sus características, se procederá a mencionar sus “escalones internos” o subniveles, y algunos ejemplos de cada uno.
Subatómico
En el subnivel subatómico tenemos partículas más pequeñas que el mismo átomo. Entre ellas tenemos los protones (positivos), los neutrones (neutros) y los electrones (negativos). Los protones y neutrones integran el núcleo atómico, mientras los electrones orbitan a grandísimas velocidades alrededor del núcleo.
Atómico
En el subnivel atómico tenemos los átomos, y por lo tanto, todos los 118 elementos de la tabla periódica. Así por ejemplo, un átomo con un solo protón y un electrón corresponde al del elemento hidrógeno (H). Asimismo tenemos átomos de helio (He), litio (Li), berilio (Be), boro (B), carbono (C), nitrógeno, oxígeno (O), flúor (F), neón (Ne), sodio (Na), etc.
Molecular
Las moléculas se combinan o se unen entre sí mediante enlaces covalentes en los que participan los electrones de sus capas más externas (las de valencia).
De esta manera, surgen moléculas como la del hidrógeno, H2, la del oxígeno, O2 (O=O), o la del nitrógeno, N2 (N≡N). Existen millones de moléculas, las cuales estudian distintas ramas de la química (como la inorgánica y orgánica).
Macromolecular
Uno de los últimos escaños del nivel químico es el subnivel macromolecular. Aquí tenemos las moléculas de mayor tamaño, las cuales muchas se encuentran dentro de los seres vivos; es decir, algunas pueden llamarse como biomoléculas. Entre ellas tenemos:
- Polisacáridos, como el glucógeno.
- Proteínas, como la insulina.
- Ácidos nucleicos, como el ARN.
- Lípidos, como los fosfolípidos y glucolípidos.
Las macromoléculas se aglomeran para formar supramoléculas, las cuales a su vez van construyendo los diferentes compartimientos que componen las células (organelos).
A partir de entonces tocamos las puertas del nivel biológico, que se sustenta sobre el nivel químico: no están divorciados, sino entrelazados, más de lo que se puede creer.
Referencias
- Whitten, Davis, Peck & Stanley. (2008). Química. (8va ed.). CENGAGE Learning.
- Khan Academy. (2021). Matter, elements and atoms. Recuperado de: khanacademy.org
- María Estela Raffino. (16 de julio de 2020). Niveles de organización de la materia. Recuperado de: concepto.de
- Ana Zita. (2021). Niveles de organización de la materia. Recuperado de: todamateria.com
- Joshua Halpern. (05 de septiembre de 2020). Classification of Matter. Chemistry LibreTexts. Recuperado de: chem.libretexts.org
