Ley de Raoult: principio y fórmula, ejemplos, ejercicios
La ley de Rauolt es aquella que se utiliza para explicar el descenso o abatimiento de la presión de vapor, presente sobre una solución, debido a la disolución de un soluto no volátil, tal como una sal o un compuesto orgánico.
También se utiliza esta ley para analizar y describir la composición de solventes volátiles en la fase gaseosa, ubicada en el espacio sobre una solución que presenta una mezcla de ellos. La ley lleva su nombre en honor a su creador, François-Marie Rauolt (1830-1901).
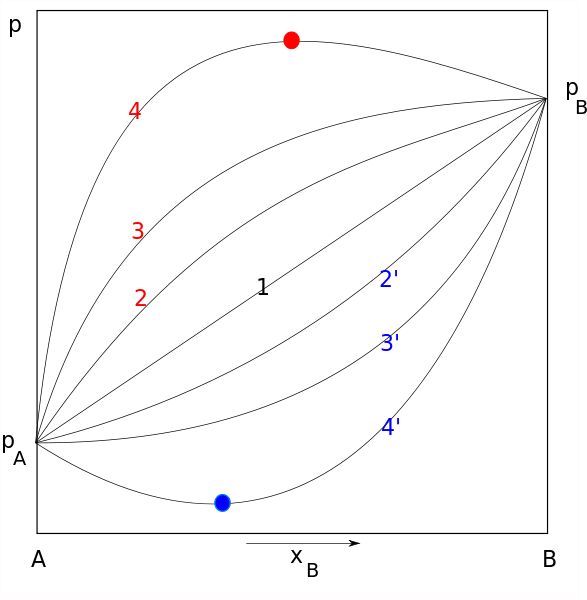
La ley de Rauolt aplica para soluciones ideales que cumplen con algunas características, entre ellas la siguiente: las fuerzas intermoleculares entre moléculas iguales (fuerzas cohesivas) deben ser iguales a las fuerzas intermoleculares entre moléculas distintas o disímiles (fuerzas adhesivas).
Muchas de las soluciones no son ideales, lo cual explica las desviaciones de la ley de Rauolt observadas en algunas mezclas de solventes volátiles. Por ejemplo, la mezcla de cloroformo (CH3Cl) y acetona (CH3COCH3), presenta una desviación negativa de la ley de Raoult.

La presión de vapor en la fase gaseosa en tales casos es menor a la predicha por la ley, explicable por la formación de puentes de hidrógeno entre los componentes de la mezcla.
Índice del artículo
La ley de Rauolt señala que la presión parcial de vapor ejercida por un componente o solvente volátil de la mezcla gaseosa, encima de la solución, está relacionada con la presión de vapor ejercida por el componente o solvente volátil puro, y sus respectivas fracciones molares.
La siguiente ecuación resumen lo anterior dicho:
Psv = Psvº · Xsv
Donde Psv es la presión parcial del solvente volátil en la mezcla gaseosa, Psvº la presión del solvente volátil puro, y Xsv la fracción molar en la solución del solvente volátil.
Si se tiene una mezcla de dos solventes volátiles (A y B) en la solución, se puede calcular la presión de vapor que ellos originan en la fase gaseosa, encima de la solución. Esta será una suma de las presiones parciales que ejercen los gases A y B:
PA = XA · PAº
PB = XB · PBº
Por lo que sumando las presiones de A y B obtenemos la presión P total:
P = XA · PAº + XB · PBº
Donde P es la presión de vapor de la mezcla gaseosa encima de la solución, XA y XB las fracciones molares de los solventes volátiles A y B en la mezcla, y PAº y PBº las presiones de vapor de los solventes volátiles puros A y B.
La presión parcial de un solvente volátil en la fase gaseosa viene dado por la expresión:
P = PAº · XA
En presencia de un soluto B en la solución, la fracción molar de B se expresa de la forma siguiente:
XB = 1 – XA
Luego, mediante un tratamiento matemático sencillo, se llega a la expresión:
ΔP = PAº · XB (1)
Donde ΔP es la disminución de la presión parcial del solvente en la fase gaseosa.
La expresión matemática (1) señala la disminución de la presión de vapor de un solvente por la presencia en la solución de un soluto B no volátil. Se ha explicado la disminución de la presión de vapor del solvente por la ubicación de las moléculas del soluto B en la superficie de la solución.
La presencia de moléculas del soluto B produciría una disminución en la concentración de las moléculas del solvente A en la superficie de la solución, limitando su evaporación; y explicándose así, la disminución de su presión de vapor en la fase gaseosa.
La ley de Raoult sirve para calcular la presión de vapor de un componente volátil de una solución, como etanol, benceno, tolueno, etano, propano, etc., en el espacio sobre la solución.
Puede utilizarse para calcular la presión de vapor que se genera en el espacio sobre una solución, como consecuencia de la mezcla de líquidos volátiles, ya sea benceno y tolueno, etano y propano, acetona y etanol, etc.
Asimismo, con esta ley se puede determinar cuál será la disminución de la presión de vapor si, por ejemplo, se disolviera sacarosa en el agua, siendo un soluto no volátil.
Calcular la presión de vapor de una solución elaborada disolviendo 60 g de cloruro de sodio (NaCl) en 400 g de agua (H2O). La presión del vapor de agua (PH2Oº) a 37 ºC es 47,1 mmHg. Peso molecular H2O = 18 g/mol y peso molecular NaCl = 58,5 g/mol.
Calculamos primero los moles de agua y cloruro de sodio para poder determinar sus fracciones molares:
Moles de H2O = gramos de H2O / PM H2O
= 400 g / (18 g/mol)
= 22,22 moles
Moles de NaCl = g de NaCl / pm NaCl
= 60 g / (58,5 g/mol)
= 1,03 moles
El NaCl es un compuesto electrolítico que se disocia en Na+ + Cl–. Por lo tanto, 1,03 moles de NaCl se disocian en 1,03 moles de Na+ y 1,03 moles de Cl–.
Tenemos la expresión:
Pv = XH2O · PH2Oº
Nos falta por lo tanto la fracción molar del agua:
XH2O = moles de H2O / (moles de H2O + moles de Na+ + moles de Cl–)
= 22,2 moles / 22,22 moles + 1,03 moles + 1,03 moles
= 0,896
Y calculamos Pv:
Pv = 47,1 mmHg · 0.896
Pv = 42,20 mmHg
Siendo el descenso de la presión de vapor por la presencia de cloruro de sodio:
ΔPv = 47,1 mmHg – 42,20 mmHg
= 4,9 mmHg
A una temperatura de -100 ºC el etano (CH3CH3) y el propano (CH3CH2CH3) son líquidos. A esa temperatura, la presión vapor del etano puro (Petanoº) es de 394 mmHg, mientras que la presión de vapor del propano puro (Ppropanoº) es de 22 mmHg. ¿Cuál será la presión de vapor sobre una solución que contiene cantidades equimolares de ambos compuestos?
El planteamiento del problema señala que la solución contiene cantidades equimolares de los compuestos. Esto implica que la fracción molar de los compuestos etano y propano es forzosamente igual a 0,5.
Nuevamente, la solución viene por la expresión:
Pv = Petano + Ppropano
Calculamos las presiones parciales tanto del etano como del propano:
Petano = Petanoº · Xetano
= 394 mmHg · 0,5
= 197 mmHg
Ppropano = Ppropanoº · Xpropano
= 22 mmHg · 0,5
= 11 mmHg
Y así calculamos finalmente Pv:
Pv = Petano + Ppropano
= 197 mmHg + 11 mmHg
= 208 mmHg
- Whitten, Davis, Peck & Stanley. (2008). Química. (8va ed.). CENGAGE Learning
- Wikipedia. (2020). Raoult’s law. Recuperado de: en.wikipedia.org
- Helmenstine, Anne Marie, Ph.D. (11 de febrero de 2020). Raoult’s Law Definition in Chemistry. Recuperado de: thoughtco.com
- Encyclopædia Britannica. (2020). Raoult’s law. Recuperado de: britannica.com
- Clark J., Ly I., & Khan S. (18 de mayo de 2020). Raoult’s law. Chemistry LibreTexts. Recuperado de: chem.libretexts.org
