Metales alcalinotérreos: qué y cuáles son, propiedades, aplicaciones
¿Qué son los metales alcalinotérreos?
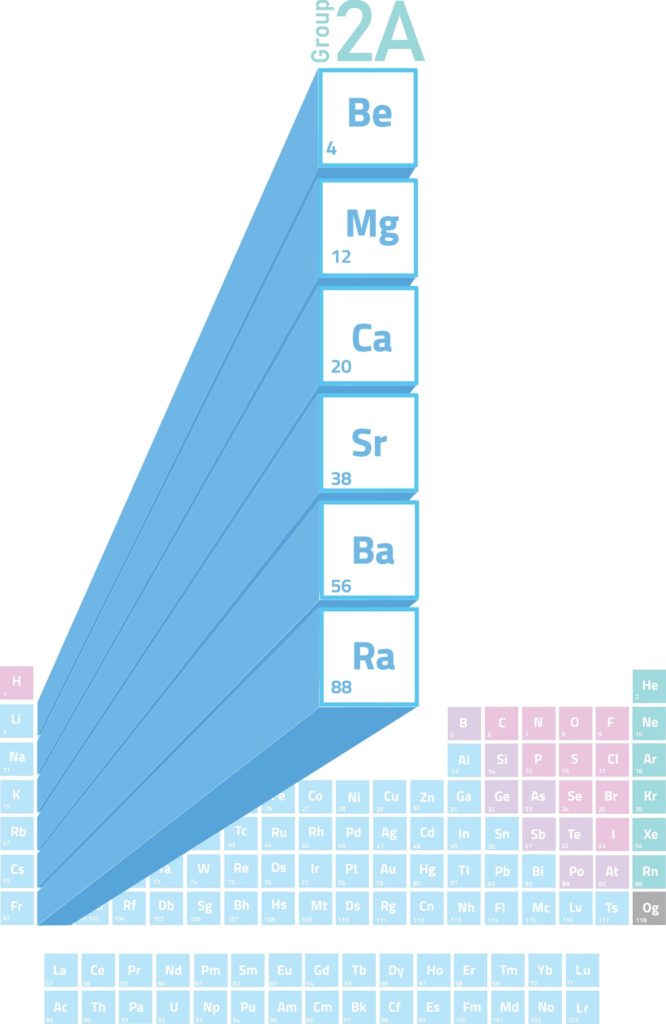
Los metales alcalinotérreos son los elementos del grupo 2 (antiguamente llamado grupo 2A) de la tabla periódica. Es decir que están formados por los 6 elementos de la segunda columna de la tabla periódica que van desde el berilio (Be) hasta el radio (Ra).
Son un grupo de elementos metálicos bastante reactivos y relativamente comunes. Poseen solo dos electrones de valencia ubicados en un orbital s. Por esta razón, pertenecen al bloque s de la tabla periódica.
El nombre “alcalinotérreo” proviene de la unión de las palabras “alcalino”, que es otra forma de decir básico, y tierra, que es como se les decía antes a los óxidos. Así que metales alcalinotérreos significa, literalmente, metales que forman óxidos básicos.
Estos metales tienen muchas aplicaciones que los hacen importantes en nuestra sociedad actual, en especial el magnesio. Estas aplicaciones se deben a sus propiedades particulares, las cuales se describen a continuación.
Propiedades de los metales alcalinotérreos
Tienen apariencia metálica
Todos los metales alcalinotérreos presentan color plateado con brillo metálico. El radón además es radiactivo por lo que brilla en la oscuridad emitiendo una luz verde característica.
Son metales poco densos
Todos los metales alcalinotérreos son más densos que el agua, pero son menos densos que la mayoría de los demás elementos metálicos de la tabla periódica.
Las densidades en este grupo van desde 1,54 g/cm3 para el calcio hasta 5,5 g/cm3 para el radio, lo que es considerablemente menor que las densidades de otros metales como el hierro (7,9 g/cm3), el cobre (9,0 g/cm3), el plomo (11,3 g/cm3) y el mercurio (13,5 g/cm3), por mencionar algunos.
Tienen puntos de fusión y ebullición relativamente bajos
Al ser metales, sus puntos de fusión y ebullición son mayores que los de la mayoría de los no metales. Sin embargo, son menores que los puntos de fusión y ebullición de la mayoría de los demás metales, con algunas excepciones.
Tienen valencia +2
Debido a su configuración electrónica, estos metales tienden a perder dos electrones cuando reaccionan con otros elementos como los no metales. Por esta razón, su única valencia es +2.
Son relativamente reactivos
Los metales alcalinotérreos son mucho más reactivos que metales como el hierro o el cobre, pero son menos reactivos que los metales alcalinos (los elementos del grupo 1). Mientras más abajo esté en el grupo, más reactivo es el metal.
Por ejemplo, el berilio (el primero del grupo) no reacciona con agua mientras que los dos siguientes pueden reaccionar con agua caliente y los últimos incluso pueden reaccionar con agua fría.
Reaccionan con el aire para formar óxidos básicos
Estos metales tienden a formar óxidos básicos cuando reaccionan con el oxígeno del aire. De hecho, es por esto que se llaman alcalinotérreos. Estos óxidos, al disolverse en agua, se convierten en hidróxidos que producen soluciones alcalinas o básicas.
Aplicaciones de los metales alcalinotérreos
En la industria tecnológica
Algunos de los metales alcalinotérreos se utilizan en la manufactura de semiconductores. Estos son esenciales en la construcción de circuitos electrónicos tales como los que contienen prácticamente todos los aparatos eléctricos modernos, desde las computadoras y teléfonos móviles, hasta las lavadoras, los autos y demás.
En la industria alimenticia
El calcio es un nutriente esencial para la vida. Forma parte de la estructura de los huesos y tiene otras funciones importantes en el cuerpo. Por esta razón, este elemento se añade como fortificante a muchos alimentos desde cereales hasta productos lácteos. Además, también se utiliza en la fabricación de queso.
En la industria automovilística
Algunos de los metales alcalinotérreos tienen muy buenas propiedades mecánicas, lo que significa que son duros y resistentes. Además, son resistentes a la corrosión, por lo que se utilizan frecuentemente en la fabricación de rines de lujo para automóviles así como en otras partes de los mismos.
En la industria militar
Por sus propiedades mecánicas y su baja densidad, metales como el magnesio y el berilio se utilizan en la construcción de aviones de combate, satélites y helicópteros.
Además, por sus propiedades eléctricas se utilizan también en la fabricación de distintos tipos de sensores y sistemas ópticos y electrónicos que la industria militar utiliza para crear armas y sistemas de comunicaciones.
Los seis metales alcalinotérreos
Existen solo seis metales alcalinotérreos. A continuación, se presenta una breve descripción de cada uno de ellos:
Berilio (Be)
Es el elemento número 4 de la tabla periódica y el primero del grupo de los metales alcalinotérreos. Es un metal muy ligero, fuerte y con propiedades únicas que lo hacen útil en la fabricación de semiconductores.
Magnesio (Mg)
El magnesio es un metal plateado, relativamente ligero, con un bajo punto de fusión y ebullición (comparado a otros metales). Es muy duro y resistente y se utiliza frecuentemente en la fabricación de partes para automóviles y como aditivo en la preparación de aleaciones como ciertos tipos de acero.
Es el segundo metal alcalinotérreo y el elemento número 12 de la tabla periódica. Al igual que otros elementos en este grupo, es un nutriente esencial para la vida.
Calcio (Ca)
El calcio es el 5to elemento más abundante en la corteza terrestre. Se encuentra como carbonato de calcio en muchos minerales y rocas y también es un elemento esencial para la vida debido a su participación en la formación de los huesos y su importancia en el sistema nervioso.
Este metal es el elemento número 20 de la tabla periódica, se encuentra en el cuarto período y es el tercer metal alcalinotérreo.
Estroncio (Sr)
El elemento número 38 y cuarto metal alcalinotérreo es el estroncio. Es más pesado que el calcio, pero se le parece mucho en términos de sus propiedades químicas y físicas. De hecho, el estroncio puede reemplazar al calcio en los huesos.
Esto es especialmente problemático cuando nos exponemos al estroncio radiactivo que se produce luego de una reacción nuclear, ya que, al adherirse a los huesos, es muy difícil de eliminar del cuerpo y nos va envenenando con radiación poco a poco.
Bario (Ba)
Este elemento tiene número atómico 56 y también tiene propiedades bastante similares a las del calcio y el estroncio. Es un metal bastante blando y muy reactivo que no se encuentra en forma elemental en la naturaleza. Es uno de los metales alcalinotérreos con mayor carácter metálico.
Radio (Ra)
El último elemento del grupo de los alcalinotérreos es el radio, un metal radiactivo (de allí su nombre) que emite una luz tenue de color verde que es fácil de observar en la oscuridad.
Se solía utilizar mucho en la preparación de pinturas que brillan en la oscuridad, pero luego que se descubrió lo peligrosa que es la radioactividad para la salud, se prohibió su uso.
