Guanina: características, estructura, formación y funciones
La guanina es una base nitrogenada que sirve para la biosíntesis del guanilato 5’-monofosfato y del deoxiguanilato 5’-monofosfato. Ambas sustancias forman parte, respectivamente, del ARN y del ADN, las cuales almacenan la información genética de las células.
El ácido ribonucleico (ARN) y el ácido desoxirribonucleico (ADN) están formados por nucleótidos, los cuales están constituidos por una base nitrogenada unida a un azúcar y a un grupo fosfato.
La guanina, además de formar parte de los ácidos nucleicos, en sus formas de nucleósidos monofosfato, difosfato y trifosfatos (GMP, GDP y GTP) participa en procesos tales como el metabolismo energético, la traducción de la señal intracelular, la fisiología de los fotoreceptores y la fusión de vesículas.
Índice del artículo
- 1 Estructura química
- 2 Características
- 3 Biosíntesis
- 4 Función
- 5 Enfermedades relacionadas
- 6 Referencias
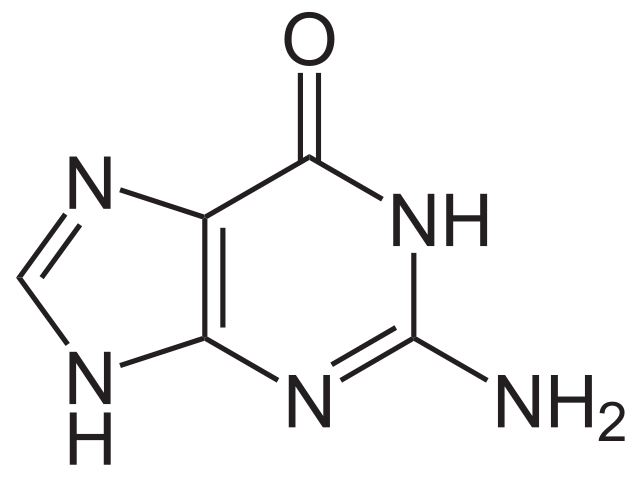
La estructura química de la guanina (2-amino-6-hidroxipurina) es un anillo heterocíclico de purina, que consiste en un sistema de dos anillos unidos: un anillo es pirimidina y el otro anillo es imidazol.
El anillo heterocíclico de la guanina es plano y con algunos dobles enlaces conjugados. Adicionalmente, tiene dos formas tautoméricas, las forma ceto y enol, entre los grupos C-1 y N-6.
Las características de la guanina son las siguientes:
– La guanina es una sustancia apolar. Es insoluble en agua, pero es soluble en soluciones concentradas de ácidos o bases fuertes.
– Puede ser aislada como un sólido blanco, con fórmula empírica C5H5N5O, y peso molecular 151,3 g/mol.
– La propiedad de absorber luz a 260 nm del ADN se debe, en parte, a la estructura química de la guanina.
– En el ADN, la guanina forma tres enlaces de hidrógeno. El grupo carbonilo C-6 es un aceptor de enlace hidrógeno, el grupo N-1 y el grupo amino de C-2 son donadores de enlace de hidrógeno.
Por esta razón, se necesita más energía para romper un enlace entre una guanina y una citosina, que el de una adenina con una timina, ya que este último par se encuentra unido por solo dos puentes de hidrógeno.
– En la célula, siempre se encuentra formando parte de los ácidos nucleicos o como GMP, GDP y GTP, nunca en su forma libre.
La molécula de guanina, como otras purinas, es sintetizada de novo a partir de 5-fosforibosil-1-pirofosfato (PRPP), mediante reacciones catalizadas por enzimas.
El primer paso consiste en la adición de un grupo amino, proveniente de la glutamina, al PRPP y se forma 5-fosforibosilamina (PRA).
Posteriormente, en una secuencia ordenada, ocurre la adición de glicina, aspartato, glutamina, formiato y dióxido de carbono al PRA. De esta manera, se forma un metabolito intermediario denominado inosina 5’-monofosfato (IMP).
Durante este proceso, se utiliza la energía libre de la hidrólisis del ATP (adenosina 5’-trifosfato), que produce ADP (adenosina 5’-difosfato) y Pi (fosfato inorgánico).
Una oxidación del IMP dependiende de NAD+ (dinucleótido de nicotinamida y adenina), produce xantina 5’-monofosfato (XMP). La posterior adición de un grupo amino al XMP, produce la molécula de guanilato.
La regulación de la biosíntesis de guanilato se lleva a cabo al inicio, cuando se forma PRA, y al final, cuando ocurre la oxidación del IMP. La regulación ocurre mediante retroalimentación negativa: un nucleótido de GMP inhibe las enzimas en ambas etapas.
Durante la degradación metabólica de los nucleótidos, las bases nitrogenadas son recicladas. El GMP se forma mediante la enzima hipoxantina-guanina fosforibosiltransferasa, transfiriendo un grupo fosribosil desde el PRPP a la guanina.
Debido a que la guanina no se encuentra en su forma libre, sus funciones están asociadas al GMP, GDP y GTP. A continuación se mencionan algunas de ellas:
– La guanosina 5’-trifosfato (GTP) actúa como un reservorio de energía libre. El grupo gamma fosfato del GTP puede ser transferido a la adenosina 5’-trifosfato (ADP), para formar ATP. Esta reacción es reversible, y es catalizada por la nucleosido difosfato quinasa.
– El GMP es la forma más estable del nucleótido que contiene guanina. Mediante hidrólisis, el GMP forma GMP cíclico (GMPc), el cual es un segundo mensajero durante la señalización intracelular, en la vias de traducción. Por ejemplo, en las células fotoreceptoras y quimiorreceptoras del olfato.
– El GMPc participa en la relajación de los vasos sanguíneos del músculo liso, durante la biosíntesis de óxido nítrico en las células del endotelio.
– La hidrólisis del fosfato gamma de GTP sirve como fuente de energía libre para la biosíntesis de proteínas en los ribosomas.
– Las enzimas helicasas necesitan la energía libre de la hidrólisis de GTP para separar la doble hélice de ADN, durante la replicación y la transcripción del ADN.
– En las neuronas del hipocampo, la acción de los canales de sodio dependientes de voltaje es regulada por la hidrólisis de GTP a GDP.
Los altos niveles de ácido úrico en sangre y orina han sido asociados a tres defectos metabólicos diferentes, que veremos a continuación.
Se caracteriza por la deficiencia de HPRT (hipoxantina-guanina fosforibosil tranferasa), una enzima importante para el reciclamiento de la hipoxantina y la guanina. En este caso, aumenta los niveles de PRPP y no se forma IMP y GMP, dos reguladores importantes de la etapa inicial de síntesis de purinas. Todo ello favorece la biosíntesis de novo de las purinas.
Esto produce un incremento en los niveles de PRPP. Este metabolito actúa como un activador de la glutamina PRPP-amidotranferasa, que se encarga de la síntesis de 5-fosforibosilamina, incrementando la biosíntesis de novo de purinas.
Se trata de una enfermedad relacionada con el almacenamiento de glucógeno tipo I. Los pacientes que padecen este síndrome poseen una glucosa 6-fosfatasa defectuosa. Esto produce un incremento en los niveles de glucosa 6-fosfato, que sirve para la síntesis de ribosa 5-fosfato, vía pentosas fosfato.
La ribosa 5-fosfato es el metabolito de partida para la biosíntesis de PRPP. De forma similar a los dos casos anteriores, esto conduce a un incremento de la biosíntesis de novo de las purinas.
El aumento de ácido úrico en sangre y orina ocasiona síntomas que son comúnmente conocidos como gota. En el caso del síndrome Lesch Nyhan, los pacientes carecen por completo de la actividad de la enzima HPRP, lo que conduce a la manifestación de otros síntomas que incluyen parálisis y retraso mental.
El gen de la HPRP se encuentra en el cromosoma X. Por ello, las mutaciones en este gen afecta a varones. No existe tratamiento para tratar los problemas neurológicos. Los síntomas asociados con el incremento de ácido úrico son tratados con alopurinol.
- Dawson, R. et al. 1986. Data for Biochemical Research. Clarendon Press, Oxford.
- Horton, R; Moran, L; Scrimgeour, G; Perry, M. And Rawn, D. 2008. Principios de Bioquimica. 4ta Edicion. Pearson Education.
- Mathews, Van Holde, Ahern. 2001. Biochemistry. 3th Edition.
- Murray, R; Granner, D; Mayes, P. And Rodwell, V. 2003. Harper’s Illustrated Biochemistry. 26th Edition. McGraw-Hill Companies.
- Nelson, DL and Cox, M. 1994. Lehninger. Principles of Biochemistry. 4th Edition. Ed Omega.
- Sigma-Aldrich. 2019. Guanine Chemical Sheet. Word Wide Web address: sigmaaldrich.com.
