Inmunidad humoral: teoría, mecanismos efectores, ejemplos
La inmunidad humoral, también conocida como la respuesta inmune mediada por anticuerpos, es uno de los mecanismos de defensa más importantes de los organismos frente a la invasión por microorganismos o toxinas extracelulares.
Concretamente, la inmunidad humoral hace referencia a la inmunidad mediada por factores sanguíneos, que son proteínas del suero conocidas como “anticuerpos” que funcionan en las respuestas a infecciones y que son producidas específicamente en respuesta a la presencia de “antígenos”.
El sistema inmune de un mamífero puede dividirse en sistema inmune innato y sistema inmune adaptativo. El sistema inmune innato consiste en los distintos elementos que funcionan como barreras físicas y químicas contra el ingreso de agentes invasores al cuerpo.
Entre tales barreras están los epitelios y algunas de las sustancias producidas por estos; también participan algunos tipos de células específicos que, en conjunto, representan el primer sistema de defensa del cuerpo.
El sistema inmune adaptativo o específico es un poco más complejo y “evolucionado”, pues se desencadena en respuesta a la exposición a agentes infecciosos o al contacto con determinados microorganismos, aunque ambos sistemas usualmente trabajan en conjunto.
Se dice que es un sistema específico porque ocurre en respuesta a determinantes definidos y está mediado por células sumamente especializadas que, además, tienen la capacidad de “recordar” y responder más rápidamente y con más “fuerza” o “eficacia” a exposiciones reiteradas al mismo agente invasor.
La inmunidad humoral es una de las subcategorías de la inmunidad adaptativa o específica, que también se clasifica en inmunidad celular. Ambos tipos de respuestas se diferencian entre sí según el componente del sistema inmunitario que participa.
Índice del artículo
La teoría de la inmunidad humoral, que fue producto de intensos años de investigación y debate, propone que la inmunidad está mediada por sustancias presentes en los fluidos corporales o los “humores”.
Esta teoría fue desarrollada por muchos científicos, que independientemente estudiaron y describieron a muchos de los efectores implicados en tales mecanismos de la respuesta.
Paul Ehrlich fue quizá uno de los más influyentes, pues fue quien realizó los estudios más profundos sobre la complementariedad antígeno-anticuerpo a principios de 1900.
El reconocido inmunólogo Rudolph Virchow, en 1858, estableció que todas las patologías corporales se debían al mal funcionamiento de los elementos celulares responsables de la protección, más que a un “desajuste de los humores” solubles.
Poco más de 25 años después, en 1884, Eli Metchnikoff llevó a la luz la primera publicación de la teoría fagocítica, que hoy da forma y sustenta las bases principales de la teoría de la inmunidad mediada por células (inmunidad celular).
Muchos detractores de Metchnikoff trataron de “desmentir” sus afirmaciones y fue en 1888 cuando George Nuttall, realizando una serie de experimentos diseñados para poner a prueba las teorías de Metchnikoff, observó que el suero de animales normales poseía una “toxicidad natural” frente a ciertos microorganismos.
De tal forma, se popularizó en el mundo científico que fluidos libres de células provenientes de animales “sanos” o “especialmente inmunizados” podían matar bacterias, de tal suerte que no era necesario recurrir a la teoría celular para explicar la inmunidad innata y la adquirida.
Los primeros en comprobar experimentalmente la existencia de una respuesta inmune humoral fueron Emil von Behring y Shibasaburo Kitasato en la última década de 1800. Von Behring y Kitasato demostraron que las respuestas inmunes disparadas por la difteria y el tétano se debían a la presencia de anticuerpos contra la exotoxina.
A principios de 1900, Karl Landsteiner y otros investigadores se dieron cuenta de que otras toxinas y sustancias de origen no bacteriano podían producir la inmunidad humoral.
El término “anticuerpo” fue acuñado poco tiempo después como una generalidad, para hacer referencia a aquellas sustancias específicas que podían funcionar como antitoxinas contra los “antígenos”.
La palabra antígeno fue el término empleado para definir las sustancias que disparan la producción de los anticuerpos humorales.
Tanto las respuestas inmunes humorales como las respuestas inmunes celulares están mediadas por un tipo de células conocidas como linfocitos.
Los principales protagonistas de la inmunidad celular son los linfocitos T, mientras que son los linfocitos B los que responden a la presencia de antígenos extraños y se transforman en las células productoras de anticuerpos características de la inmunidad humoral.
La inmunidad humoral es el principal mecanismo de defensa contra microorganismos extracelulares y otras toxinas, entretanto la inmunidad celular contribuye a la eliminación de patógenos intracelulares, que son “inaccesibles” al reconocimiento por anticuerpos.
Así como la respuesta inmune celular, la respuesta humoral puede dividirse en tres fases: una de reconocimiento, otra de activación y otra de efectuación.
La fase de reconocimiento consiste en la unión de los antígenos a receptores de membrana específicos en la superficie celular de los linfocitos B maduros.
Los anticuerpos funcionan como dichos “receptores” y son capaces de reconocer proteínas, polisacáridos, lípidos y otras sustancias extracelulares “extrañas”.
La fase de activación comienza con la proliferación de los linfocitos tras el reconocimiento de los antígenos y continúa con la diferenciación, bien en otras células efectoras capaces de eliminar antígenos, o en células de memoria capaces de inducir respuestas más rápidas tras una nueva exposición al mismo antígeno.
Durante la fase efectora, los linfocitos que ejercen las funciones de eliminación de antígenos se conocen como “células efectoras”, aunque usualmente participan otras células, que también participan en la respuesta inmune innata, y que fagocitan y eliminan los agentes extraños.
Los anticuerpos producidos por los linfocitos o células B tienen la función fisiológica de neutralizar y eliminar el antígeno que indujo su formación y el sistema inmune humoral puede responder a multiplicidad de antígenos diferentes.
Los linfocitos B se originan en la médula ósea en respuesta a un antígeno definido (son específicos) y ello ocurre antes de la estimulación antigénica. La expresión de anticuerpos determinados dispara las respuestas de proliferación y diferenciación de más células B secretoras de anticuerpos.
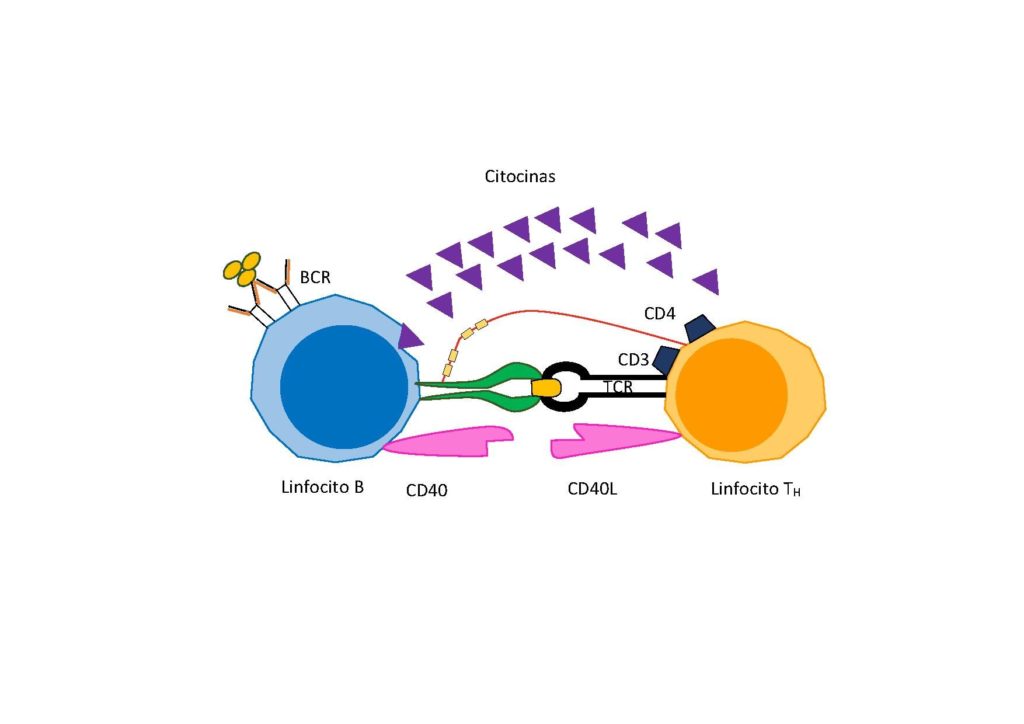
No obstante, dependiendo de la naturaleza del antígeno, se necesita una señal adicional para la diferenciación y la proliferación que está dada por un tipo especial de linfocito T llamado “linfocito T colaborador” que secreta factores de activación para las células B.
En vista de que se encuentran principalmente en los fluidos sanguíneos, los anticuerpos producidos por las células B se denominan inmunoglobulinas. Estas moléculas de naturaleza proteica poseen dos cadenas glicoproteicas pesadas y dos livianas unidas entre sí a través de puentes disulfuro (S-S).
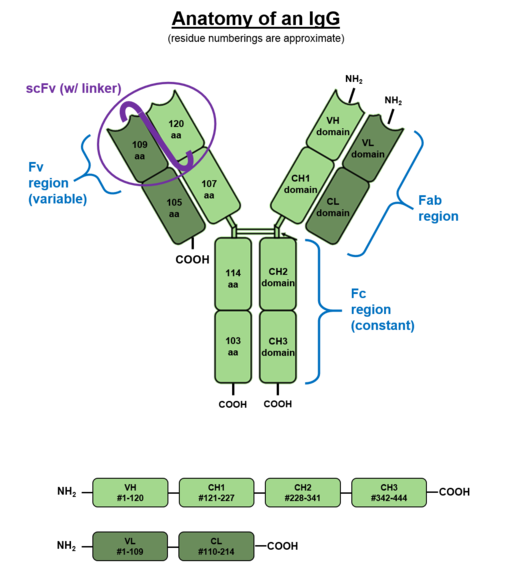
Las cadenas livianas se conocen como “kappa” y “lambda”, pero existen 5 tipos de cadenas pesadas a las que se ha denominado gamma (G), mu (M), alfa (A), delta (D) y épsilon (E).
La combinación de cadenas livianas y pesadas termina con la formación de las inmunoglobulinas IgG, IgM, IgA, IgD e IgE. El anticuerpo más abundante en el suero de los mamíferos en la inmunoglobulina IgG (aproximadamente un 70%).
Cada cadena de un anticuerpo posee un extremo amino terminal y otro carboxilo terminal. La porción capaz de unirse a los antígenos se encuentra en el extremo amino terminal, empero la región carboxilo terminal es la que dictamina la actividad biológica.
La región carboxilo terminal de los anticuerpos tipo IgG es reconocida específicamente por células fagocíticas como los neutrófilos y los macrófagos, que poseen receptores especiales para ello.
Este reconocimiento implica contacto entre el receptor y el anticuerpo y es esta unión la que facilita la fagocitosis y degradación de los antígenos en el interior de las células fagocíticas.
A diferencia de las IgG, las otras clases de inmunoglobulinas no se encuentran en las secreciones y los tejidos. Sin embargo, estas son igual de útiles en la elicitación de la respuesta inmune.
Las inmunoglobulinas IgM (10% de las inmunoglobulinas séricas) son potentes activadores del sistema de complemento, por lo que funcionan en la lisis de antígenos e incremento de la resistencia.
Las inmunoglobulinas IgA (20% de las inmunoglobulinas séricas) son producidas en los tejidos linfoides y son procesadas y transportadas hacia las mucosas pulmonares y del tracto gastrointestinal. Estas funcionan en la neutralización de virus y otros antígenos que ingresan por las superficies mucosas.
La IgD está unida a los linfocitos B y funciona como receptor de antígenos, mientras que la IgE (conocida como el anticuerpo alérgico) está unida a la superficie de los mastocitos y basófilos a través de receptores específicos. Ambas inmunoglobulinas están en muy baja concentración en el suero.
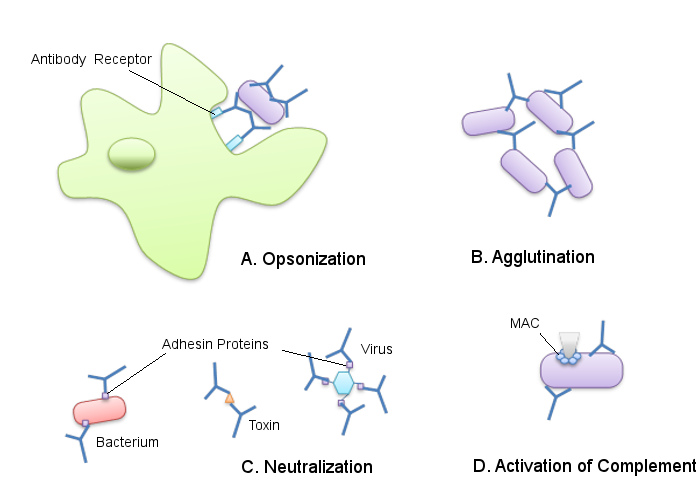
Los anticuerpos producidos por los principales efectores de la respuesta inmune humoral (linfocitos B) tienen la capacidad de “inducir” o “activar” diferentes mecanismos de respuesta frente a diferentes tipos de amenazas.
Por ejemplo, las inmunoglobulinas IgG son activadores de lo que se conoce como la “cascada de complemento”, que trabaja en la neutralización de partículas virales, previniendo así su unión a las células del hospedador.
Durante el embarazo, la madre transfiere anticuerpos al feto a través de las células trofoblásticas de la placenta, que poseen receptores con alta afinidad por el extremo carboxilo terminal de inmunoglobulinas como las IgG.
La respuesta humoral frente a bacterias que poseen “cápsulas” compuestas por polisacáridos está mediada por la inmunoglobulina M, que promueve la fagocitosis de estos microorganismos.
Otro ejemplo importante de inmunidad humoral es la respuesta sistémica a parásitos, donde la IgE “dirige” la destrucción de los mismos a través de células eosinófilas.
- Abbas, A., Lichtman, A., & Pober, J. (1999). Inmunología Celular y Molecular (3rd ed.). Madrid: McGraw-Hill.
- Carroll, M. C., & Isenman, D. E. (2012). Regulation of Humoral Immunity by Complement. Immunity, 37(2), 199–207.
- Kindt, T., Goldsby, R., & Osborne, B. (2007). Inmunología de Kuby (6th ed.). México D.F.: McGraw-Hill Interamericana de España.
- Klein, T. (2007). The acquired immune response. In xPharm: The Comprehensive Pharmacology Reference (pp. 1–5).
- Lishner, H., & DiGeorge, A. (1969). Role of the thymus in humoral immunity. The Lancet, 2, 1044–1049.
- Medzhitov, R., & Janeway, C. (2000). Innate immunity. The New England Journal of Medicine, 338–344.
- Merlo, L. M. F., & Mandik-Nayak, L. (2013). Adaptive Immunity: B Cells and Antibodies. In Cancer Immunotherapy: Immune Suppression and Tumor Growth: Second Edition (pp. 25–40).
- Silverstein, A. M. (1979). History of Immunology. Cellular versus Humoral Immunity: Determinants and Consequences of an Epic 19th Century Battle. Cellular Immunology, 48(1), 208–221.
- Steinman, R. M. (2008). Linking innate to adaptive immunity through dendritic cells. In Innate Immunity to Pulmonary Infection (pp. 101–113).
- Tan, T. T., & Coussens, L. M. (2007). Humoral immunity, inflammation and cancer. Current Opinion in Immunology, 19(2), 209–216.
- Twigg, H. L. (2005). Humoral immune defense (antibodies): Recent advances. Proceedings of the American Thoracic Society, 2(5), 417–421.
- Wherry, E. J., & Masopust, D. (2016). Adaptive Immunity: Neutralizing, Eliminating, and Remembering for the Next Time. In Viral Pathogenesis: From Basics to Systems Biology: Third Edition (pp. 57–69).
