Trinitrotolueno (TNT): estructura, propiedades, usos, riesgos, explosión
El trinitrotolueno es un compuesto orgánico formado por carbono, oxígeno, hidrógeno y nitrógeno con tres grupos nitro –NO2. Su fórmula química es C6H2(CH3)(NO2)3 o también la fórmula condensada C7H5N3O6.
Su nombre completo es 2,4,6-trinitrotolueno, pero comúnmente es conocido como TNT. Es un sólido blanco cristalino que puede explotar al ser calentado por encima de cierta temperatura.

La presencia en el trinitrotolueno de los tres grupos nitro –NO2 favorece el hecho de que explote con cierta facilidad. Por ello, ha sido muy utilizado en artefactos explosivos, proyectiles, bombas y granadas.
También se ha usado para realizar voladuras bajo el agua, en pozos profundos y para explosiones de tipo industrial o no bélico.
El TNT es un producto delicado que puede explotar también por golpes muy fuertes. Además es tóxico para los seres humanos, animales y plantas. Los lugares donde han ocurrido sus explosiones han quedado contaminados y se están realizando investigaciones para eliminar los restos de este compuesto.
Una forma que puede resultar efectiva y económica de reducir la concentración en el medio ambiente contaminado de TNT es mediante el uso de algunos tipos de bacterias y hongos.
Índice del artículo
- 1 Estructura química
- 2 Nomenclatura
- 3 Propiedades
- 4 Proceso de explosión del TNT
- 5 Obtención del TNT
- 6 Usos del TNT
- 7 Riesgos del TNT
- 8 Contaminación del ambiente con TNT
- 9 Referencias
El 2,4,6-trinitrotolueno está formado por una molécula de tolueno C6H5–CH3, a la cual se han añadido tres grupos nitro –NO2.
Los tres grupos nitro –NO2 están situados de forma simétrica en el anillo bencénico del tolueno. Se encuentran en las posiciones 2, 4 y 6, donde la posición 1 corresponde al metilo –CH3.
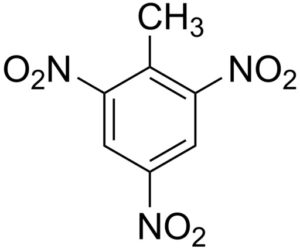
– Trinitrotolueno
– 2,4,6-Trinitrotolueno
– TNT
– Trilita
– 2-Metil-1,3,5-trinitrobenceno
Sólido cristalino incoloro a amarillo pálido. Cristales en forma de agujas.
227,13 g/mol.
80,5 ºC.
No hierve. Se descompone con una explosión a 240 ºC.
No es posible medirlo porque explota.
1,65 g/cm3
Casi insoluble en agua: 115 mg/L a 23 °C. Muy poco soluble en etanol. Muy soluble en acetona, piridina, benceno y tolueno.
Puede descomponerse de forma explosiva al ser calentado. Al llegar a 240 °C explota. También puede explotar al sufrir golpes muy fuertes.
Cuando se calienta hasta descomposición produce gases tóxicos de óxidos de nitrógeno NOx.
La explosión del TNT conlleva una reacción química. Básicamente es un proceso de combustión en el cual se libera energía de forma muy rápida. Además se emiten gases los cuales son agentes para transferir energía.

Para que se produzca una reacción de combustión (oxidación) deben estar presentes el combustible y el oxidante.
En el caso del TNT, ambos se encuentran en la misma molécula, pues los átomos de carbono (C) e hidrógeno (H) son los combustibles y el oxidante es el oxígeno (O) de los grupos nitro –NO2. Esto permite que la reacción sea más rápida.
Durante la reacción de combustión del TNT los átomos se rearreglan y el oxígeno (O) queda más cerca del carbono (C). Además, el nitrógeno del –NO2 se reduce y pasa a formar nitrógeno gaseoso N2 que es un compuesto mucho más estable.
La reacción química de explosión del TNT puede resumirse así:
2 C7H5N3O6 → 7 CO↑ + 7 C + 5 H2O↑ + 3 N2↑
Se produce carbón (C) durante la explosión, en forma de una nube negra, y además se forma monóxido de carbono (CO), lo que se debe a que en la molécula no hay suficiente oxígeno para oxidar completamente todos los átomos de carbono (C) e hidrógeno (H) presentes.
El TNT es un compuesto preparado únicamente de manera artificial por el ser humano.
No se encuentra de forma natural en el ambiente. Se produce solo en algunas instalaciones militares.
Se prepara mediante nitración del tolueno (C6H5–CH3) con una mezcla de ácido nítrico HNO3 y ácido sulfúrico H2SO4. Primero se obtiene una mezcla de orto– y para-nitrotoluenos que por nitración enérgica ulterior forman el trinitrotolueno simétrico.
El TNT es un explosivo que se ha utilizado en dispositivos bélicos y explosiones militares.
Se utiliza para llenar proyectiles, granadas y bombas aerotransportadas, ya que es suficientemente insensible al impacto recibido para salir del cañón de un arma, pero puede explotar al ser impactado por un mecanismo detonador.

No está diseñado para producir fragmentación significativa o lanzar proyectiles.
Se ha utilizado para explosiones de interés industrial, en voladuras bajo el agua (por su insolubilidad en agua) y explosiones de pozo profundo. En el pasado se utilizaba con mayor frecuencia para demoliciones. Actualmente se emplea junto con otros compuestos.

También ha sido intermediario para colorantes y químicos fotográficos.
Puede explotar si se expone a calor intenso, fuego o a golpes muy fuertes.
Es irritante de ojos, piel y tracto respiratorio. Es un compuesto muy tóxico tanto para el ser humano como para los animales, plantas y muchos microorganismos.
Los síntomas de exposición al TNT incluyen dolor de cabeza, debilidad, anemia, hepatitis tóxica, cianosis, dermatitis, daño al hígado, conjuntivitis, falta de apetito, náuseas, vómitos, diarrea, entre otros.
Es un mutágeno, es decir, puede cambiar la información genética (ADN) de un organismo causando cambios que pueden relacionarse con la aparición de enfermedades hereditarias.
También ha sido clasificado como carcinógeno o generador de cáncer.
El TNT ha sido detectado en suelos y aguas en zonas de operaciones bélicas militares, en lugares de manufactura de municiones y donde se realizan operaciones de entrenamiento militar.

La contaminación con TNT es peligrosa para la vida de los animales, seres humanos y plantas. Aunque el TNT se emplea actualmente en menor cantidad, es uno de los compuestos nitroaromáticos que más han sido utilizados en la industria de los explosivos.
Por ello es uno de los que más contribuye a la contaminación ambiental.
La necesidad de “limpiar” regiones contaminadas con TNT ha motivado el desarrollo de varios procesos de remediación. La remediación es la remoción de contaminantes del medio ambiente.
Muchos microorganismos son capaces de bioremediar TNT como, por ejemplo, las bacterias del género Pseudomonas, Enterobacter, Mycobacterium y Clostridium.
Se ha encontrado además que hay ciertas bacterias que han evolucionado en lugares contaminados con TNT y que pueden sobrevivir y también degradarlo o metabolizarlo como fuente nutriente.
La Escherichia coli por ejemplo ha demostrado una destacada capacidad de biotransformación de TNT, pues posee múltiples enzimas para atacarlo, demostrando a la vez una alta tolerancia hacia su toxicidad.
Además algunas especies de hongos pueden biotransformar al TNT, convirtiéndolo en minerales no dañinos.
Por otra parte, algunos investigadores han encontrado que el alga Spirulina platensis tiene la capacidad de adsorber sobre la superficie de sus células y asimilar hasta un 87% del TNT presente en aguas contaminadas con este compuesto.
La tolerancia de esta alga hacia el TNT y su habilidad para limpiar el agua contaminada con este indican el alto potencial de esta alga como fitoremediador.
- U.S. National Library of Medicine. (2019). 2,4,6-Trinitrotoluene. Recuperado de pubchem.ncbi.nlm.nih.gov.
- Murray, S.G. (2000). Explosives. Mechanism of Explosion. In Encyclopedia of Forensic Sciences 2000, Pages 758-764. Recuperado de sciencedirect.com.
- Adamia, G. et al. (2018). About possibility of alga Spirulina application for phytoremediation of water polluted with 2,4,6-trinitrotoluene. Annals of Agrarian Science 16 (2018) 348-351. Recuperado de reader.elsevier.com.
- Serrano-González, M.Y. et al. (2018). Biotransformation and degradation of 2,4,6-trinitrotoluene by microbial metabolism and their interaction. Defence Technology 14 (2018) 151-164. Recuperado de pdf.sciencedirectassets.com.
- Iman, M. et al. (2017). Systems Biology Approach to Bioremediation of Nitroaromatics: Constraint-Based Analysis of 2,4,6-Trinitrotoluene Biotransformation by Escherichia coli. Molecules 2017, 22, 1242. Recuperado de mdpi.com.
- Windholz, M. et al. (editors) (1983). The Merck Index. An Encyclopedia of Chemicals, Drugs, and Biologicals. Tenth Edition. Merck & CO., Inc.
- Morrison, R.T. and Boyd, R.N. (2002). Organic Chemistry. 6th Edition. Prentice-Hall.
