Peroxidasas: estructura, funciones y tipos
Las peroxidasas son, en su mayoría, hemoproteínas con actividad enzimática que catalizan la oxidación de una gran variedad de sustratos orgánicos e inorgánicos empleando para ello peróxido de hidrógeno u otras sustancias relacionadas.
En su sentido más amplio, el término “peroxidasa” incluye a enzimas como las NAD- y las NADP-peroxidasas, las ácido graso-peroxidasas, las citocromo-peroxidasas, las glutatión-peroxidasas y muchas otras enzimas no específicas.
No obstante, se emplea más comúnmente para referirse a las enzimas inespecíficas de diferentes fuentes que tienen actividad oxidorreductasa y que emplean peróxido de hidrógeno y otros sustratos para catalizar sus reacciones de oxido-reducción.
Las “hemo-peroxidasas” son sumamente comunes en la naturaleza. Se encuentran en animales, plantas superiores, levaduras, hongos y bacterias.
En los mamíferos, estas son producidas por los leucocitos, el útero, el bazo y el hígado, las glándulas salivales, las paredes estomacales, los pulmones, las glándulas tiroideas y otros tejidos.
En las plantas, las especies vegetales más ricas en peroxidasas son el rábano picante y el árbol de higo. La peroxidasa purificada a partir del rábano picante ha sido extensamente estudiada y empleada para diversos propósitos en la biología y la bioquímica experimental.
En las células eucariotas, estas importantes enzimas usualmente se encuentran en el interior de orgánulos especializados conocidos como “peroxisomas”, que están rodeados por una membrana sencilla y que se hallan implicados en numerosos procesos metabólicos celulares.
Índice del artículo
A pesar de la poca homología que existe entre las diferentes clases de peroxidasas, se ha determinado que su estructura secundaria y la forma en que esta se organiza está bastante conservada entre las diferentes especies.
Existen alguna excepciones, pero la mayoría de las peroxidasas son glicoproteínas y se cree que los carbohidratos contribuyen a su estabilidad frente a elevadas temperaturas.
Estas proteínas tienen pesos moleculares que van desde los 35 hasta los 150 kDa, lo que equivale a 250 y 730 residuos aminoacídicos aproximadamente.
Con la excepción de la mieloperoxidasa, todas las moléculas de este tipo contienen en su estructura un grupo hemo que en estado de reposo presenta un átomo de hierro en estado de oxidación Fe+3. Las plantas poseen un grupo prostético conocido como ferroporfirina XI.
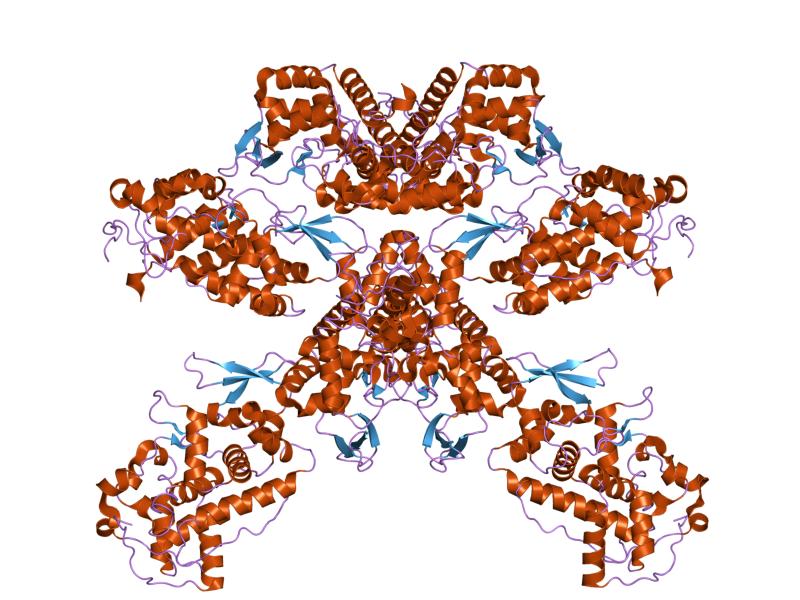
Las peroxidasas poseen dos dominios estructurales que “envuelven” el grupo hemo y cada uno de estos dominios es producto de la expresión de un gen que sufrió un evento de duplicación. Dichas estructuras están compuestas por más de 10 hélices alfa unidas por bucles y giros polipeptídicos.
El plegamiento adecuado de la molécula parece depender de la presencia de residuos conservados de glicina y prolina, así como de un residuo de ácido aspártico y otro de arginina que forman un puente salino entre ellos que conecta ambos dominios estructurales.
La función principal de las enzimas peroxidasas es la remoción del peróxido de hidrógeno del entorno celular, que puede producirse por diferentes mecanismos y que podría representar serias amenazas para la estabilidad intracelular.
Sin embargo, en dicho proceso de remoción de esta especie reactiva de oxígeno (en la cual el oxígeno posee un estado de oxidación intermedio) las peroxidasas emplean la capacidad oxidante de esta sustancia para cumplir otras funciones importantes para el metabolismo.
En las plantas, estas proteínas son parte importante de los procesos de lignificación y de los mecanismos de defensa en tejidos infectados con patógenos o que han sufrido daños físicos.
En el contexto científico, nuevas aplicaciones han surgido para las peroxidasas y entre estas se incluyen el tratamiento de aguas residuales que contienen compuestos fenólicos, la síntesis de compuestos aromáticos y la remoción del peróxido de materiales alimenticios o de desecho.
En términos analíticos y de diagnóstico, la peroxidasa de rábano picante es quizá la enzima más utilizada para la preparación de anticuerpos conjugados que se emplean para las pruebas inmunológicas de absorción como ELISA (del inglés “Enzyme-linked immunosorbent assay”) y también para la determinación de varios tipos de compuestos.
El proceso catalítico de las peroxidasas ocurre a través de pasos secuenciales que comienzan con la interacción entre el sitio activo de la enzima y peróxido de hidrógeno, lo que oxida el átomo de hierro en el grupo hemo y genera un compuesto intermediario inestable conocido como compuesto I (CoI).
La proteína oxidada (CoI) tiene, entonces, un grupo hemo con un átomo de hierro que pasó del estado de oxidación III al estado IV y para este proceso se redujo el peróxido de hidrógeno a agua.
El compuesto I es capaz de oxidar a un sustrato donador de electrones, formando un radical de sustrato y convirtiéndose en una nueva especie química conocida como el compuesto II (CoII), que es posteriormente reducido por una segunda molécula de sustrato, regenerando el hierro en estado III y produciendo otro radical.
Las peroxidasas se agrupan en tres clases dependiendo del organismo donde se encuentren:
– Clase I: peroxidasas procariotas intracelulares.
– Clase II: peroxidasas fúngicas extracelulares.
– Clase III: peroxidasas vegetales secretadas.
Contrario a las proteínas de la clase I, las de las clases II y III poseen en sus estructuras puentes disulfuros construidos entre residuos de cisteína, lo que les otorga una rigidez considerablemente mayor.
Las proteínas de las clases II y III se diferencian también de las de la clase I en que por lo general poseen glicosilaciones en su superficie.
Mecanísticamente hablando, las peroxidasas también pueden ser categorizadas de acuerdo con la naturaleza de los átomos que se encuentran en su centro catalítico. De esta forma se han descrito las hemoperoxidasas (las más comunes), las vanadio-haloperoxidasas y otras.
Hemoperoxidasas
Como ya se comentó, estas peroxidasas tienen un grupo prostético en su centro catalítico conocido como grupo hemo. El átomo de hierro en este lugar está coordinado mediante cuatro enlaces con los átomos de nitrógeno.
Vanadio-Haloperoxidasas
En lugar de un grupo hemo, las vanadio-haloperoxidasas poseen vanadato como grupo prostético. Estas enzimas han sido aisladas de organismos marinos y de algunos hongos terrestres.
El vanadio en este grupo está coordinado por tres oxígenos no-proteicos, un nitrógeno proveniente de un residuo de histidina y un nitrógeno de un enlace azida.
Otras peroxidasas
En este grupo se categorizan muchas haloperoxidasas bacterianas que tienen grupos prostéticos distintos al hemo o al vanadio. En este grupo también se encuentran las glutatión peroxidasas, que contienen un grupo prostético seleno-cisteínico y algunas enzimas capaces de oxidar lignina.
- Alberts, B., Dennis, B., Hopkin, K., Johnson, A., Lewis, J., Raff, M., … Walter, P. (2004). Essential Cell Biology. Abingdon: Garland Science, Taylor & Francis Group.
- Banci, L. (1997). Structural properties of peroxidases. Journal of Biotechnology, 53, 253–263.
- Deurzen, M. P. J. Van, Rantwijk, F. Van, & Sheldon, R. A. (1997). Selective Oxidations Catalyzed by Peroxidases. Tetrahedron, 53(39), 13183–13220.
- Dunford, H. B., & Stillman, J. S. (1976). On the Function and Mechanism of action of Peroxidases. Coordination Chemistry Reviews, 19, 187–251.
- Hamid, M., & Rehman, K. (2009). Potential applications of peroxidases. Food Chemistry, 115(4), 1177–1186.
- Rawn, J. D. (1998). Biochemistry. Burlington, Massachusetts: Neil Patterson Publishers.
- Stansfield, W. D., Colomé, J. S., & Cano, R. J. (2003). Molecular and Cell Biology. (K. E. Cullen, Ed.). McGraw-Hill eBooks.
