Tritio: qué es, estructura, propiedades, usos
¿Qué es el tritio?
El tritio es el nombre que se le ha otorgado a uno de los isótopos del elemento químico hidrógeno, cuyo símbolo suele ser T o 3H, aunque también se le denomina hidrógeno-3. Este es ampliamente utilizado en una gran cantidad de aplicaciones, especialmente en el campo nuclear.
Asimismo, en la década de 1930 se originó por vez primera este isótopo, partiendo del bombardeo con partículas de elevada energía (llamadas deuterones) de otro isótopo del mismo elemento llamado deuterio, gracias a los científicos P. Harteck, M. L. Oliphant y E. Rutherford.
Estos investigadores no tuvieron éxito en el aislamiento del tritio a pesar de sus ensayos, los cuales sí arrojaron resultados concretos en manos de Cornog y Álvarez, descubriendo a su vez las cualidades radiactivas de esta sustancia.
En este planeta la producción de tritio es sumamente rara en la naturaleza, originándose únicamente en proporciones tan pequeñas que se consideran trazas por medio de las interacciones atmosféricas con la radiación de tipo cósmico.
Estructura del tritio
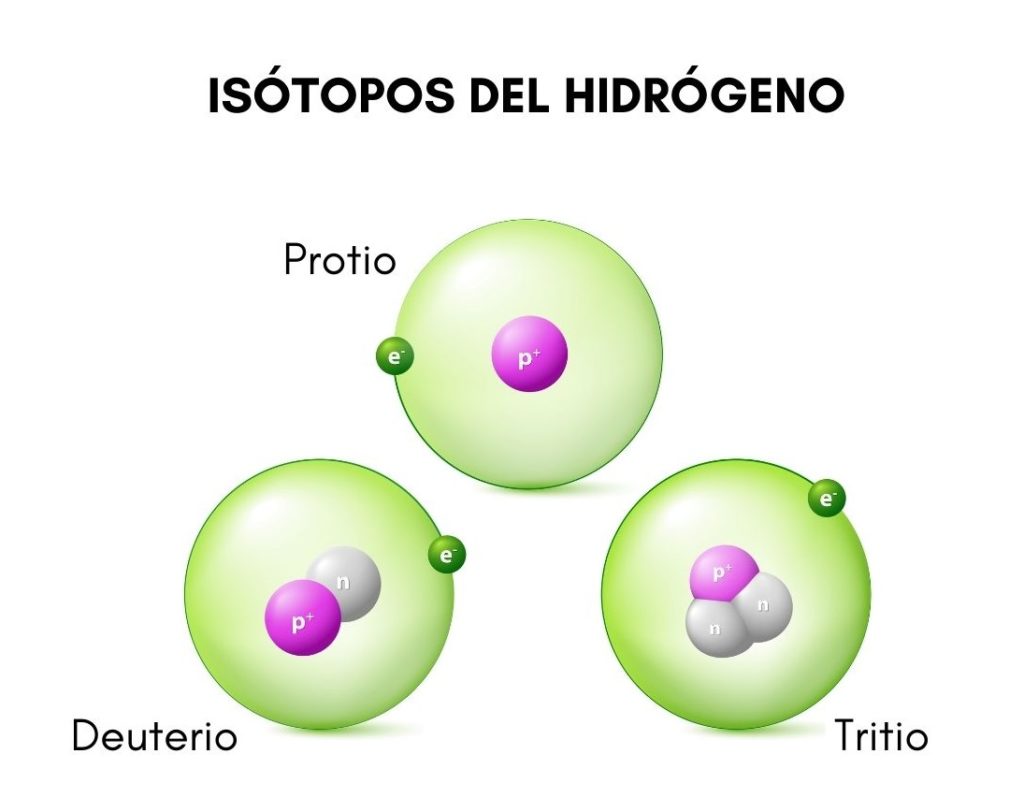
Cuando se habla de la estructura del tritio lo primero que debe notarse es su núcleo, poseedor de dos neutrones y un único protón, que le confiere una masa tres veces mayor a la del hidrógeno ordinario.
Este isótopo posee propiedades físicas y químicas que lo distinguen de las otras especies isotópicas provenientes del hidrógeno, a pesar de sus similitudes estructurales.
Además de poseer un peso atómico o masa de alrededor de 3 g, esta sustancia manifiesta radiactividad, cuyas características cinéticas muestran una vida media de aproximadamente 12,3 años.
En la imagen superior se comparan las estructuras de los tres isótopos conocidos del hidrógeno, llamados protio (la especie de mayor abundancia), deuterio y tritio.
Las características estructurales del tritio le permiten coexistir con el hidrógeno y el deuterio en el agua que proviene de la naturaleza, cuya producción se debe posiblemente a la interacción que se da entre la radiación cósmica y el nitrógeno de origen atmosférico.
En este sentido, en el agua de origen natural se presenta esta sustancia en una proporción de 10-18 con relación al hidrógeno ordinario; es decir, una abundancia ínfima que solo se puede reconocer como trazas.
Algunos datos sobre el tritio
Se han investigado y utilizado varias maneras de producir tritio debido a su alto interés científico por las propiedades radiactivas y de aprovechamiento energético que presenta.
De este modo, la siguiente ecuación muestra la reacción general mediante la cual se produce este isótopo, a partir del bombardeo de átomos de deuterio con deuterones de elevada energía:
D + D → T + H
Asimismo, puede llevarse a cabo como una reacción exotérmica o endotérmica a través de un proceso denominado activación de neutrones de determinados elementos (como litio o boro), y dependiendo del elemento que se esté tratando.
Además de estos métodos, raramente se puede obtener tritio a partir de la fisión nuclear, la cual consiste en la división del núcleo de un átomo considerado como pesado (en este caso, isótopos de uranio o plutonio) para obtener dos o más núcleos de menor tamaño, produciéndose enormes cantidades de energía.
En este caso la obtención de tritio se da como producto colateral o subproducto, pero no es la finalidad de este mecanismo.
A excepción del proceso que se describió previamente, todos estos procesos de producción de esta especie isotópica se llevan a cabo en reactores nucleares, en los cuales se controlan las condiciones de cada reacción.
Propiedades del tritio
– Produce una enorme cantidad de energía cuando se origina a partir del deuterio.
– Presenta propiedades de radiactividad, lo cual continúa despertando el interés científico en las investigaciones de la fusión nuclear.
– Este isótopo se representa en su forma molecular como T2 o 3H2, cuyo peso molecular se encuentra alrededor de 6 g.
– De manera similar al protio y al deuterio, esta sustancia presenta dificultad para ser confinada.
– Cuando esta especie se combina con el oxígeno, se origina un óxido (representado como T2O) que se encuentra en fase líquida y es comúnmente conocido como agua superpesada.
– Es capaz de experimentar fusión con otras especies ligeras con mayor facilidad que la mostrada por el hidrógeno ordinario.
– Presenta un peligro para el medio ambiente si se emplea de manera masiva, especialmente en reacciones de procesos de fusión.
– Puede formar con el oxígeno otra sustancia conocida como agua semisúperpesada (representada como HTO), la cual también es radiactiva.
– Se considera un generador de partículas de baja energía, conocidas como radiación beta.
– Cuando se han presentado casos de consumo de agua tritiada, se ha observado que su vida media en el cuerpo se mantiene en el rango de 2,4 a 18 días, excretándose posteriormente.
Usos/aplicaciones
Entre las aplicaciones del tritio destacan los procesos relacionados con reacciones de tipo nuclear. Seguidamente se muestra una lista con sus usos más importantes:
– En el área de la radioluminiscencia se emplea el tritio para producir instrumentos que permitan la iluminación, especialmente la nocturna, en diferentes dispositivos de uso comercial como relojes, cuchillos, armas de fuego, entre otros, a través de la autoalimentación.
– En el campo de la química nuclear, las reacciones de este tipo se emplean como fuente de energía en la fabricación de armas nucleares y termonucleares, además de ser utilizado en combinación con el deuterio para procesos de fusión nuclear bajo control.
– En el área de la química analítica este isótopo puede ser empleado en el proceso de marcaje radiactivo, donde se coloca tritio en una especie o molécula determinada y se le – puede realizar un seguimiento para estudios que se desee practicarle a esta.
– En el caso del medio biológico, se emplea el tritio como trazador de tipo transitorio en los procesos oceánicos, lo cual permite la investigación de la evolución de los océanos en la Tierra en los ámbitos físico, químico e incluso biológico.
– Entre otras aplicaciones, esta especie se ha utilizado para la fabricación de una batería de carácter atómico con el fin de producir energía eléctrica.
