Alquilo: concepto, radicales más comunes, estructura
Un alquilo es un grupo o sustituyente que deriva de un alcano mediante la eliminación de uno de sus hidrógenos. Está compuesto por lo tanto de carbono e hidrógeno, y su fórmula general es CnH2n+1, en lugar de CnH2n+2 para todos los alcanos no cíclicos, es decir, de cadenas lineales o ramificadas.
El alquilo, como grupo, se simboliza con la letra R. Así, la estructura molecular de muchos compuestos orgánicos se puede generalizar con la introducción de R. En ellos, R es tan solo una parte de la molécula, enlazado a su esqueleto o a un grupo funcional reactivo.
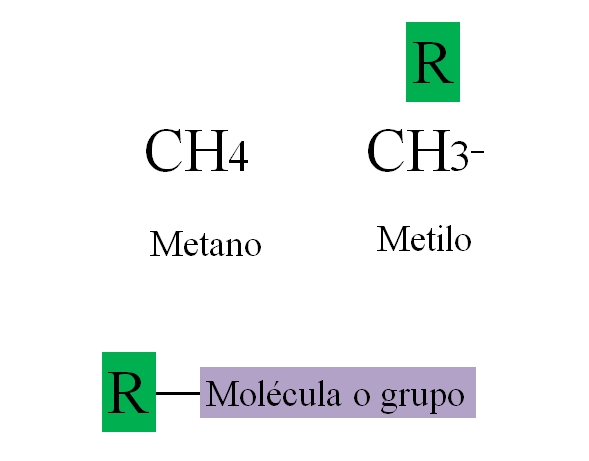
La imagen superior ejemplifica lo anterior comentado. El metano, CH4, es un alcano, y cuando pierde uno de sus hidrógenos, enlazándose a una molécula o grupo, se transforma en el metilo, CH3-. El metilo no es un compuesto: no existe como molécula libre; a menos que se trate del radical metilo, CH3·, el cual es altamente reactivo.
El alquilo, simbolizado con R, forma un enlace covalente con el resto de una molécula. Así, los compuestos alquílicos se representan como RG, donde G es un grupo que engloba la totalidad de la molécula. Por ejemplo, los alcoholes tienen fórmula ROH, por lo que son compuestos alquílicos.
Índice del artículo
- 1 Nomenclatura
- 2 Radicales alquilo más comunes
- 3 Estructura
- 4 Propiedades
- 5 Ejemplos de compuestos alquílicos
- 6 Referencias
La nomenclatura de los alquilos nada tiene que ver con la renta de una propiedad. Esta procede de la misma nomenclatura del alcano del cual deriva. En la imagen de arriba, por ejemplo, el metano se transforma en el grupo metilo. Así, basta con sustituir la terminación –ano, del nombre del alcano, por la terminación –ilo.
Otro ejemplo lo tenemos del etano, CH3CH3. Al perder uno de sus hidrógeno y enlazarse a una molécula o grupo, se transforma en el grupo etilo, CH3CH2-.
De igual modo ocurre con todos los demás alcanos, incluso aquellos que constan de cadenas cíclicas como el ciclohexano, el cual se transforma en ciclohexilo.
Los radicales alquilos son aquellas “piezas sueltas y reactivas” que se obtienen cuando R se separa de una molécula. Sus abundancias son proporcionales a la de los grupos alquilos de los que derivan. Por ejemplo, el grupo metilo, CH3– y el radical metilo, CH3·, son relativamente iguales de comunes.
En general, los radicales o grupos alquilos que provengan de alcanos que contengan en su esqueleto menos de cinco átomos de carbono, son los más comunes. Es decir, que por encima del pentano y todos sus isómeros, estos radicales se vuelven más difíciles de encontrar.
¿Por qué? Hay dos razones. La primera es que las moléculas de hidrocarburos, en condiciones de alta energía, tienden a sufrir rupturas de enlaces, por lo que se reducen sus tamaños y masas moleculares.
Y la segunda, es que en la naturaleza se tienen “sopas de isómeros”, las cuales son muy difíciles de purificar por destilación a causa de la pequeña diferencia que existe entre sus puntos de ebullición.
Es así pues, que los alquilos y sus radicales más abundantes son los de cadena corta, con un número de átomos de carbono menores a seis. Ejemplos de estos alquilos son: CH3-, CH3CH2-, CH3CH2CH2-, CH3CH2CH2CH2-, y sus isómeros posibles.
Hasta ahora los alquilos abordados han tenido estructuras de cadena lineales. Sus estructuras, como es de esperar, son las mismas que las de los alcanos de los que proceden.
Alcanos lineales darán lugar a grupos alquilos lineales. Alcanos ramificados, por otra parte, generarán alquilos ramificados. Sucede lo mismo con los alcanos cíclicos.
No obstante, los alcanos lineales también pueden originar alquilos aparentemente ramificados, dependiendo de cuál de sus átomos de carbono pierde el hidrógeno. Considérese el ejemplo del propano:
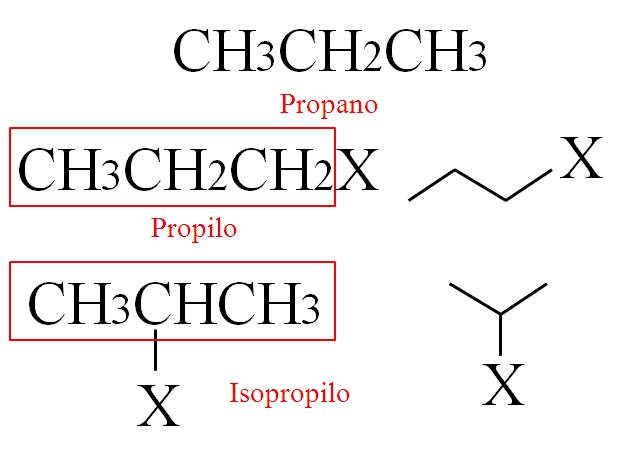
Si pierde un hidrógeno de cualquiera de sus carbonos primarios, es decir, de los de sus extremos, se obtiene el grupo propilo, CH3CH2CH2-.
Mientras, si el hidrógeno lo pierde de su carbono secundario o central, se obtiene el grupo isopropilo, (CH3)2CH-. En la imagen se muestran dos compuestos RX, con R siendo el propilo o isopropilo.
Los grupos alquilos no suelen reaccionar porque sus enlaces C-C o C-H no son fáciles de romper. Sin importar cuál sea su estructura molecular, todos comparten una propiedad en común: la hidrofobicidad. Es decir, no muestran afinidad por el agua ni por ningún solvente polar. Pero sí lo hacen por las grasas.
Cuando el grupo alquilo R es muy grande, o cuando hay muchos de ellos en una molécula, su hidrofobicidad se incrementa. Esto es lo mismo decir que aumenta su lipofilicidad (amor por las grasas). Entonces, mientras más “alquilada” esté una molécula, más afinidad tendrá esta por la grasa, y más difícil será removerla con agua.
El término ‘compuestos alquílicos’ es en extremo ambiguo en lo que respecta a la química orgánica. Siempre se le da prioridad al grupo o a la molécula a la que esté enlazado el grupo alquilo R. Y son estos grupos o moléculas además los que definen las familias de los compuestos orgánicos.
No obstante, cuando estos grupos son más comunes en química inorgánica, como sucede con los halógenos y sulfatos, se le da cierta importancia al componente alquílico. Se mencionarán algunos ejemplos para aclarar este punto.
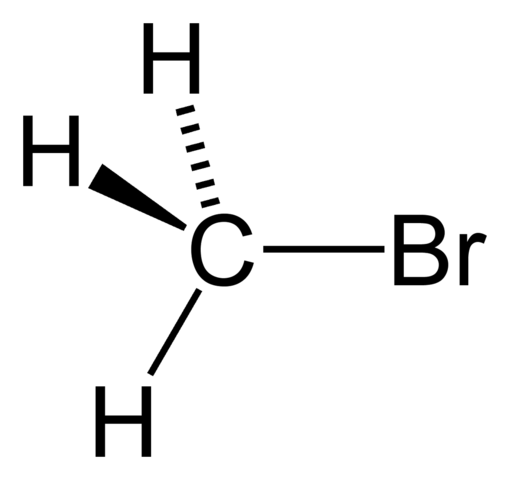
Los haluros de alquilo tienen una fórmula general RX, donde X es un átomo de halógeno (F, Cl, Br y I), y R cualquier grupo o sustituyente alquilo. Por ejemplo, CH3Br es el bromuro de metilo.
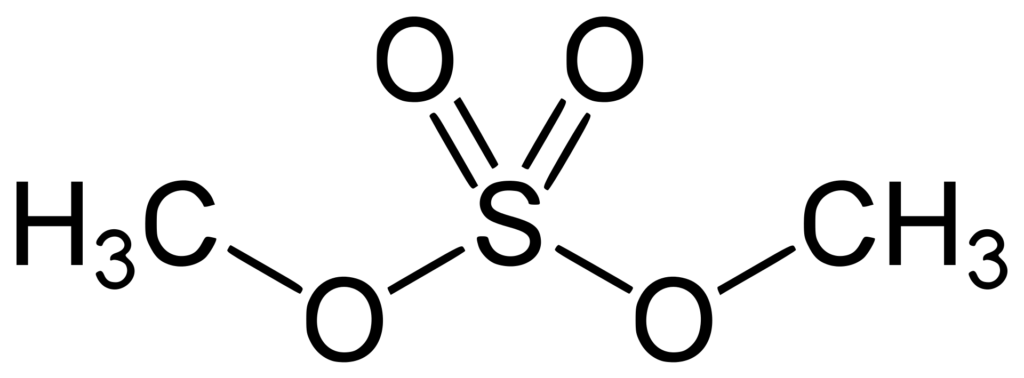
Los sulfatos de alquilo tienen una fórmula general ROSO3R’, donde R y R’ son dos grupos alquilos que pueden ser iguales o distintos. Así, tenemos al sulfato de dimetilo, CH3OSO3CH3 o Me2SO4.
Los boratos de alquilos tienen una fórmula general (RO3)B. Por ejemplo, el (CH3CH2O)3B o (EtO)3B se llama borato de etilo.
De modo similar, tenemos los triaquilboranos, cuya fórmula general es R3B. Por ejemplo, el (CH3)3B o Me3B se llama trimetilborano (TMB).
Los alcoholes también son compuestos alquílicos, y su fórmula general es ROH. Sin embargo, la sola presencia del grupo OH resta importancia a los grupos alquilos. A los alcoholes no se les llama ‘hidróxidos de alquilo’, pues los alquilos como tal no son las partes más fundamentales de sus moléculas, sino el OH.
En cambio, en los ejemplos anteriores sí se hace hincapié en la presencia de los grupos alquilos R; porque, al fin de cuenta, los halógenos, sulfatos, boranos y boratos se les encuentra mucho en compuestos inorgánicos interaccionando con cationes metálicos, y no con segmentos hidrocarbonados de alcanos.
- Morrison, R. T. y Boyd, R, N. (1987). Química Orgánica. 5ta Edición. Editorial Addison-Wesley Interamericana.
- Carey F. (2008). Química Orgánica. (Sexta edición). Mc Graw Hill.
- Graham Solomons T.W., Craig B. Fryhle. (2011). Organic Chemistry. (10th edition.). Wiley Plus.
- Wikipedia. (2020). Alkyl. Recuperado de: en.wikipedia.org
- Danielle Reid. (2020). Alkyl Group: Definition & Overview. Study. Recuperado de: study.com
- Chemistry LibreTexts. (06 de abril de 2020). Alkyl Groups. Recuperado de: chem.libretexts.org
