Adenina: estructura, biosíntesis, funciones
La adenina es una base nitrogenada de tipo purina, hallada en los ácidos ribonucleico (ARN) y desoxirribonucleico (ADN) de los organismos vivos y de los virus. Algunas de las funciones de estos biopolímeros (ARN y ADN) son el almacenamiento, la replicación, la recombinación y la transferencia de la información genética.
Para constituir los ácidos nucleicos, en primer lugar el átomo de nitrógeno 9 de la adenina forma un enlace glucosídico con el carbono 1 prima (C1′) de la ribosa (del ARN) o de la 2′-desoxirribosa (del ADN). De esta forma, la adenina forma nucleósido adenosina o adenosina.
En segundo lugar, el grupo oxidrilo (-OH) del carbono 5′ del azúcar (ribosa o 2′-desoxirribosa), de la adenosina, forma un enlace éster con un grupo fosfato.
En las células vivas, dependiendo del número de grupos fosfatos presentes, puede ser adenosín-5′-monofosfato (AMP), adenosín-5′-difosfato (ADP) y adenosín-5′-trifosfato (ATP). Los equivalentes que poseen 2′-desoxirribosa también existen. Por ejemplo, desoxiadenosín-5′-monofosfato (dAMP), etc.
Índice del artículo
- 1 Estructura y características
- 2 Biosíntesis
- 3 Funciones en el metabolismo oxidativo y reductor
- 4 Funciones en la expresión del gen
- 5 Funciones en el metabolismo energético
- 6 Otras funciones
- 7 Síntesis prebiótica
- 8 Uso como factor de cultivo celular y terapéutico
- 9 Referencias
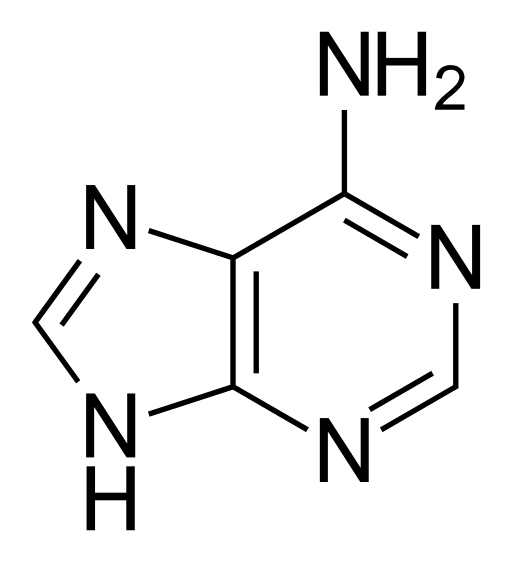
La adenina, denominada 6-aminopurina, posee la fórmula empírica C5H5N5, y tiene un peso molecular de 135,13 g/mol, siendo purificada como un sólido color amarillo tenue, con un punto de ebullición de 360ºC.
Su molécula cuenta con una estructura química de doble anillo con dobles enlaces conjugados, que es la fusión de una pirimidina con un grupo imidazol. Debido a ello, la adenina es una molécula heterocíclica plana.
Tiene una solubilidad relativa de 0,10 g/mL (a 25 ºC), en soluciones acuosas ácidas y básicas, con un pKa de 4,15 (a 25 ºC).
Por esta misma razón, es susceptible de ser detectada por absorbancia a 263 nm (con un coeficiente de absorción de E1,2 mM = 13,2 M-1.cm-1 en HCl 1,0 M), zona del espectro electromagnético correspondiente a ultravioleta cercano.
La biosíntesis de nucleótidos purínicos es idéntica en prácticamente todos los seres vivos. Comienza con la transferencia de un grupo amino desde la glutamina al sustrato 5-fosforribosil-1-pirofosfato (PRPP), y produce 5-fosforribosilamina (PRA).
Esta es una reacción catalizada por la glutamina-PRPP transferasa, una enzima clave en la regulación de esta vía metabólica.
Luego de adiciones secuenciales de los aminoácidos glutamina, glicina, metenil-folato, aspartato, N10-formil-folato al PRA, que incluyen condensaciones y cierre de anillos, se produce inosín-5′-monofosfato (IMP), cuya unidad heterocíclica es la hipoxantina (6-oxipurina).
Estas adiciones son impulsadas por la hidrólisis del ATP hasta ADP y fosfato inorgánico (Pi). Posteriormente, al IMP se le añade un grupo amino desde el aspartato, en una reacción acoplada a la hidrólisis de guanosín-trifosfato (GTP), para generar finalmente AMP.
Este último ejerce control de esta ruta biosintética mediante retroalimentación negativa, actuando sobre las enzimas que catalizan la formación de PRA y la modificación del IMP.
Al igual que ocurre con la degradación de otros nucleótidos, la base nitrogenada de los nucleótidos de adenosina pasa por un proceso denominado “reciclaje”.
El reciclaje consiste en la transferencia de un grupo fosfato desde PRPP a la adenina, y forma AMP y pirofosfato (PPi). Es un solo paso catalizado por la enzima fosforribosiltransferasa de la adenina.
La adenina forma parte de varias moléculas importantes en el metabolismo oxidativo, las cuales son las siguientes:
- El dinucleótido de flavina y adenina (FAD/FADH2) y el dinucleótido de nicotinamida adenina (NAD+/NADH), los cuales participan en reacciones de oxido-reducción transfiriendo iones hidruro (:H–).
- La coenzima A (CoA), que participa en la activación y transferencia de grupos acilo.
Durante el metabolismo oxidativo, el NAD+ funciona como sustrato aceptor de electrones (iones hidruro) y forma NADH. Mientras que el FAD es un cofactor que acepta electrones y se convierte en FADH2.
Por otra parte, la adenina forma el dinucleótido fosfato de nicotinamida adenina (NADP+/NADPH), que participa en el metabolismo reductor. Por ejemplo, el NADPH es un sustrato donador de electrones durante la biosíntesis de lípidos y de desoxiribonucleotidos.
La adenina forma parte de las vitaminas. Por ejemplo, la niacina es el precursor de NAD+ y del NADP+ y la riboflavina es el precursor de FAD.
La adenina forma parte de la S-adenosilmetionina (SAM), que es un donador de radicales metil (-CH3) y participa en la metilación de residuos de adenina y citosina en las procariotas y eucariotas.
En los procariotas, la metilación provee un sistema de reconocimiento del ADN propio, con lo cual protege el ADN de sus propias enzimas restrictivas.
En los eucariotas, la metilación determina la expresión de los genes; es decir, establece cuáles genes se deben expresar y cuáles no. Además, las metilaciones de adenina pueden marcar zonas de reparación del ADN dañado.
Muchas proteínas que se unen al ADN, como los factores de transcripción, poseen residuos de aminoácidos glutamina y asparagina que forman enlaces de hidrógeno con el átomo de N7 de la adenina.
La adenina forma parte del ATP, que es una molécula con alta energía; es decir, su hidrólisis es exergónica, y la energía libre de Gibbs es un valor alto y negativo (-7.0 Kcal/mol). En las células, el ATP participa en muchas reacciones que requieren energía, tales como:
– Impulsar las reacciones químicas endergónicas catalizadas por enzimas que participan en el metabolismo intermediario y en el anabolismo, mediante la formación de intermediarios de alta energía o reacciones acopladas.
– Impulsar la biosíntesis de proteínas en los ribosomas, al permitir la esterificación de los aminoácidos con sus correspondientes ARN de transferencia (ARNt), para formar los aminoacil-ARNt.
– Impulsar el movimiento de sustancias químicas a través de membranas celulares. Hay cuatro tipos de proteínas transportadoras: P, F, V y ABC. Los tipos P, F y V transportan iones y el tipo ABC transporta sustratos. Por ejemplo, la ATPasa de Na+/K+, de clase P, necesita un ATP para bombear hacia el interior celular dos K+ y hacia afuera tres Na+.
– Impulsar la contracción muscular. Proporciona la energía que dirige el deslizamiento de filamentos de actina sobre la miosina.
– Impulsar el transporte nuclear. Cuando la subunidad beta del receptor heterodimérico se une al ATP, interactúa con componentes del complejo de poro nuclear.
La adenosina sirve como ligando de proteínas receptoras presentes en neuronas y células del epitelio intestinal, donde actúa como mensajero extracelular o neuromodulador, al ocurrir cambios en el metabolismo energético celular.
La adenina está presente en poderosos agentes antivirales como la arabinosiladenina (araA), que es producida por algunos microorganismos. Además, está presente en la puromicina, un antibiotico que inhibe la biosíntesis de proteínas y es producida por microorganismos del género Streptomyces.
En el AMP sirve como sustrato de reacciones que generan el segundo mensajero AMP cíclico (AMPc). Este compuesto producido por la enzima adenilato ciclasa, es imprescindible en gran parte de las cascadas de señalizaciones intracelulares, necesarias para la proliferación y supervivencia celular, así como inflamación y muerte celular.
El sulfato en su estado libre no es reactivo. Una vez que entra en la célula se convierte en adenosín-5’-fosfosulfato (APS), y posteriormente en 3’-fosfoadenosín-5’-fosfosulfato (PAPS). En los mamíferos, PAPS es el donador de grupos sulfato y forma ésteres de sulfatos orgánicos tales como los de heparina y condroitina.
En la biosíntesis de cisteína, la S-adenosilmetionina (SAM) sirve como precursor de la sintesis de S-adenosilhomocisteína, la cual es transformada mediante varios pasos, catalizados por enzimas, en cisteína.
Experimentalmente se ha demostrado que manteniendo encerrados cianuro de hidrógeno (HCN) y amoníaco (NH3), en condiciones de laboratorio similares a las que reinaban en la Tierra primitiva, se produce adenina en la mezcla resultante. Esto ocurre sin necesidad de que alguna célula viva o material celular esté presente.
Las condiciones prebióticas incluyen ausencia de oxígeno molecular libre, atmósfera altamente reductora, radiación ultravioleta intensa, grandes arcos eléctricos como los generados en las tormentas, y altas temperaturas. Esto supone que la adenina fue la principal y más abundante base nitrogenada formada durante la química prebiótica.
Así, la síntesis de adenina constituiría un paso clave que haría posible el origen de las primeras células. Estas debían poseer una membrana que formaba un compartimiento cerrado, en cuyo interior se encontrarían las moléculas requeridas para construir los primeros polímeros biológicos necesarios para la autoperpetuación.
La adenina es, junto a otros compuestos químicos orgánicos e inorgánicos, un ingrediente esencial de la receta utilizada en todos los laboratorios de bioquímica, genética, biología molecular y microbiología del mundo, para cultivar células viables en el tiempo.
Esto es debido a que las variedades normales silvestres de las células, pueden detectar y captar del medio circundante la adenina disponible y utilizarla para sintetizar su propios nucleósidos de adenina.
Esto supone una forma de supervivencia celular, que economiza los recursos internos sintetizando moléculas biológicas más complejas a partir de precursores sencillos tomados desde el exterior.
En los modelos experimentales de la enfermedad renal crónica, los ratones poseen una mutación en el gen fosforribosiltransferasa de la adenina que produce una enzima no activa. A estos ratones se le administran disoluciones comerciales contentivas de adenina, citrato de sodio y glucosa, por vía intravenosa, para promover su recuperación rápida.
Este tratamiento se basa en que el PRPP, el metabolito inicial para la biosíntesis de purinas, es sintetizado a partir de ribosa-5-fosfato mediante la vía pentosa fosfato, cuyo metabolito de partida es la glucosa-6-fosfato. Sin embargo, muchas de estas disoluciones no están aprobadas por organismos reguladores internacionales para uso humano.
- Burnstock, G. 2014. Purines and Purinoceptors. Molecular Biology Overview. References Modules in Biomedical Sciences. Word Wide Web address: https://doi.org/10.1016/B978-0-12-801238-3.04741-3
- Claramount, D. et al. 2015. Animal models of pediatric chronical disease. Nefrología,35(6):517-22.
- Coade, S. y Pearson, J. 1989. Metabolism of adenine nucleotides. Circulation Research, 65:531-37
- Dawson, R. et al. 1986. Data for Biochemical Research. Clarendon Press, Oxford.
- DrougBank. 2019. Adenine Chemichal Sheet. Word Wide Web address: https://www.drugbank.ca/drugs/DB00173
- Horton, R; Moran, L; Scrimgeour, G; Perry, M. y Rawn, D. 2008. Principios de Bioquímica. 4ta Edicion. Pearson Education.
- Knight, G. 2009. Purinergic Receptors. Encyclopedia of Neuroscience. 1245-52. Word Wide Web address: https://doi.org/10.1016/B978-008045046-9.00693-8
- Mathews, Van Holde, Ahern. 2001. Biochemistry. 3th Edition.
- Murgola, E. 2003. Adenine. Encyclopedia of Genetics. Word Wide Web address: https://doi.org/10.1006/rwgn.2001.0008
- Murray, R; Granner, D; Mayes, P. And Rodwell, V. 2003. Harper’s Illustrated Biochemistry. 26th Edition. McGraw-Hill Companies.
- Nelson, DL & Cox, M. 1994. Lehninger. Principles of Biochemistry. 4th Edition. Ed Omega.
- Sigma-Aldrich. 2019. Adenine Chemical Sheet. Word Wide Web address: https://www.sigmaaldrich.com/catalog/product/aldrich/ga8626?lang=en
