Vía extrapiramidal: componentes, función, recorrido, enfermedades
La noción de la vía extrapiramidal o del sistema extrapiramidal (SEP) surgió a raíz de los estudios anatómicos y fisiológicos destinados a comprender la manera de como el sistema nervioso central controlaba la actividad de la musculatura esquelética, con el objetivo de que el cuerpo asumiera la postura corporal adecuada y produjera los movimientos voluntarios.
En ese proceso se fue descubriendo que el control de la actividad muscular requería del control de las motoneuronas del asta anterior de la médula, única conexión entre el sistema nervioso central y las fibras musculares esqueléticas, y que dicho control lo ejercían proyecciones nerviosas de centros cerebrales superiores.
Entre esas proyecciones, una vía importante es la formada por algunos axones que se originan en las áreas motoras de la corteza cerebral y descienden directamente, es decir, sin escalas, hasta la médula espinal, juntándose, a su paso por el bulbo raquídeo, en unas prominencias a las que por su forma se les dio el nombre de “pirámides”.
A este tracto se le llamó “tracto piramidal” o “corticoespinal” y se le involucró en el control de los movimientos finos y habilidosos ejecutados por las porciones distales de los miembros, mientras que se reconoció la existencia de estructuras con función motora pero no incluidas en esta vía (extra).
El término “sistema motor extrapiramidal”, obsoleto ya desde el punto de vista fisiológico, es todavía utilizado en el argot clínico para referirse a esas estructuras del cerebro y del tallo encefálico que colaboran en el control motor, pero que no forman parte del sistema piramidal o corticoespinal directo.
Índice del artículo
- 1 Componentes anatómicos y función de la vía piramidal
- 2 Enfermedades de los ganglios basales
- 3 Referencias
La vía extrapiramidal puede describirse como organizada en dos grupos de componentes: uno estaría constituido por un conjunto de núcleos del tallo encefálico y sus proyecciones hacia la médula espinal, y el otro lo integrarían los núcleos subcorticales conocidos como núcleos o ganglios basales.
En el tallo cerebral existen grupos de neuronas cuyos axones se proyectan hacia la sustancia gris de la médula espinal y que se han descrito como organizados en dos sistemas: uno medial y otro lateral.
Sistema medial
El sistema medial está formado por los fascículos vestibuloespinales, retículoespinales y tectoespinal que descienden por los cordones ventrales de la médula y ejercen un control sobre los músculos axiales o del tronco, además de los proximales de las extremidades implicados en la postura corporal.
Sistema lateral
El sistema lateral tiene como componente más importante al haz rubro-espinal, cuyos axones se proyectan desde el núcleo rojo mesencefálico, descienden por el cordón lateral de la médula y terminan influyendo sobre las motoneuronas que controlan los músculos distales de las extremidades.
De lo expuesto se deduce que el sistema medial colabora en los ajustes posturales básicos, necesarios para la actividad motora voluntaria, mientras que el lateral se ocupa, junto con la vía corticoespinal directa, de los movimientos de las extremidades dirigidos a una finalidad como alcanzar y manipular objetos.
Los ganglios basales son estructuras neuronales subcorticales que están implicadas en el procesamiento de información motora como la planificación y programación de movimientos habilidosos complejos, y cuyas alteraciones dan manifestaciones clínicas que se agrupan en síndromes conocidos como “extrapiramidales”.
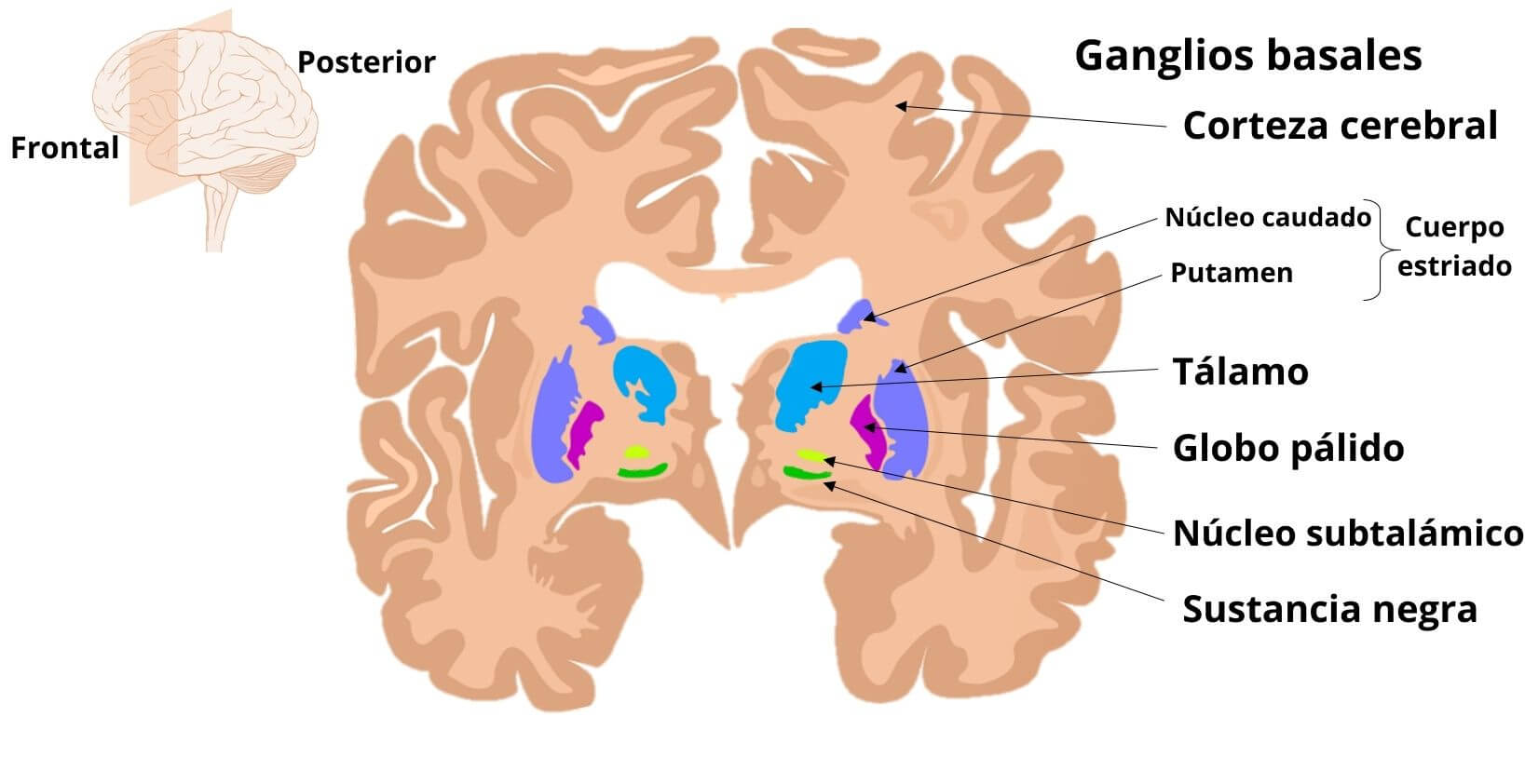
Entre los ganglios se incluye el cuerpo estriado, que está compuesto por el putamen y el núcleo caudado; el globo pálido, que tiene una porción externa (GPe) y una interna (GPi); la sustancia negra, organizada en una porción compacta (SNc) y otra reticulada (SNr), y el núcleo subtalámico o de Lewis.
Estas estructuras funcionan recibiendo información principalmente de diferentes regiones de la corteza cerebral; información que pone en marcha circuitos internos que afectan una actividad neuronal de salida que vuelve, por vía de la porción motora del tálamo, a la corteza cerebral.
La información aferente a los ganglios ingresa por el cuerpo estriado (caudado y putamen). Desde allí parten vías que se conectan con los núcleos de salida que son el GPi y la SNr, cuyos axones van a los núcleos ventroanterior y ventrolateral del tálamo, los cuales, a su vez, se proyectan a la corteza.
Las distintas etapas del circuito son cubiertas por neuronas que pertenecen a un sistema neuroquímico particular y que pueden tener un efecto inhibitorio o excitatorio. Las conexiones cortico-estriadas, las tálamo-corticales y las fibras subtalámicas liberan glutamato y son excitatorias.
Las neuronas cuyos axones salen del cuerpo estriado utilizan ácido gamma amino butírico (GABA) como neurotransmisor principal y son inhibitorias. Existen dos subpoblaciones: una sintetiza sustancia P como cotransmisor [GABA (+Sust. P)] y la otra encefalina [GABA (+Encef.)].
Neuronas GABA (+Sust. P)
Las neuronas GABA (+Sust. P) tienen receptores dopaminérgicos D1 y son excitadas por la dopamina (DA); establecen, además, una conexión inhibitoria directa con las salidas de los ganglios basales (GPi y SNr) que son también GABAérgicas pero “+ dinorfina” e inhiben a las células glutamatérgicas de proyección tálamo-cortical.
Neuronas GABA (+Encef.)
Las neuronas GABA (+Encef.) tienen receptores dopaminérgicos D2 y son inhibidas por la dopamina. Establecen conexión excitatoria indirecta con las salidas (GPi y SNr), ya que se proyectan al GPe inhibiendo a sus neuronas GABAérgicas, que inhiben a las glutamatérgicas del núcleo subtalámico, cuya función es activar las salidas (GPi y SNr).
La parte compacta de la sustancia negra (SNc) posee neuronas dopaminérgicas (DA) que se conectan con el estriado haciendo conexiones, como ya se mencionó, D1 excitatorias sobre células GABA (+Sust. P) y D2 inhibidoras sobre células GABA (+Encef.).
Entonces, y de acuerdo con lo anterior, una activación de la vía directa termina inhibiendo las salidas de los ganglios basales y liberando la actividad en las conexiones tálamo-corticales, mientras que la activación de la vía indirecta activa las salidas y reduce la actividad tálamo-cortical.
Aunque las interacciones y el funcionamiento conjunto exacto de las vías directa e indirecta recién consideradas no están esclarecidos, la organización anatómica y neuroquímica descritas nos sirven para entender, al menos en parte, algunos cuadros patológicos producto de la disfunción de los núcleos basales.
Aunque los procesos patológicos que asientan en los ganglios basales son de naturaleza diversa y afectan no solo ciertas funciones motoras sino también funciones cognitivas, asociativas y emocionales, en los cuadros clínicos las alteraciones de la motricidad ocupan un lugar resaltante y la mayor parte de la investigación se ha centrado en ellas.
Las alteraciones del movimiento propias de la disfunción de los ganglios basales se pueden clasificar en uno de tres grupos, a saber:
– Hipercinesias, como la enfermedad o corea de Huntington y el hemibalismo.
– Hipocinesias, como la enfermedad de Parkinson.
– Distonías, como la atetosis.
En líneas generales, puede decirse que los trastornos hipercinéticos, caracterizados por una actividad motora excesiva, cursan con una disminución de la inhibición que las salidas (GPi y SNr) ejercen sobre las proyecciones tálamo-corticales, las cuales se hacen más activas.
Los trastornos hipocinéticos, por otra parte, se acompañan de un aumento de esta inhibición, con reducción de la actividad tálamo-cortical.
Es un trastorno hipercinético caracterizado por sacudidas aleatorias involuntarias y espasmódicas de las extremidades y de la región orofacial, movimientos coreiformes o “de baile” que aumentan gradualmente e incapacitan al paciente, alteración del habla y desarrollo progresivo de demencia.
La enfermedad se acompaña tempranamente de una degeneración de las neuronas estriatales GABA (+Encef.) de la vía indirecta.
Como estas neuronas no inhiben más a las neuronas GABAérgicas del GPe, estas inhiben exageradamente al núcleo subtalámico, que deja de excitar a las salidas inhibitorias (GPi y SNr) y se desinhiben las proyecciones tálamo-corticales.
Consiste en las contracciones violentas de los músculos proximales de los miembros, que son proyectados con fuerza en movimientos de gran amplitud. El daño en este caso es la degeneración del núcleo subtalámico, lo que resulta en algo similar a lo descrito para la corea, aunque no por hiper inhibición, sino por destrucción del núcleo subtalámico.
Está caracterizada por dificultad y retardo en la iniciación de los movimientos (acinesia), enlentecimiento de los movimientos (hipocinesia), rostro inexpresivo o expresión facial en máscara, alteración de la marcha con disminución de los movimientos asociados de los miembros durante la misma y temblor involuntario de las extremidades en reposo.
El daño, en este caso, consiste en la degeneración del sistema nigroestriado, que son las proyecciones dopaminérgicas que parten de la región compacta de la sustancia negra (SNc) y se conectan con las neuronas estriatales que dan origen a las vías directa e indirecta.
La supresión de la excitación que las fibras dopaminérgicas ejercen sobre las células GABA (+Sust. P) de la vía directa, retira la inhibición que estas ejercen sobre las salidas GABAérgicas (GPi y SNr) hacia el tálamo, que es ahora inhibido con mayor intensidad. Se trata entonces de una desinhibición de las salidas.
Por otro lado, la supresión de la actividad inhibitoria que la dopamina ejerce sobre las células GABA (+Encef.) de la vía indirecta las libera y aumenta la inhibición que ejercen sobre las células GABA del GPe, lo cual desinhibe a las neuronas del núcleo subtalámico, que entonces hiperactivan las salidas.
Como se observa, el resultado final de los efectos de la degeneración dopaminérgica sobre las dos vías internas, directa e indirecta, es el mismo, bien se trate de desinhibición o de estimulación de las salidas (GPi y SNr) GABAérgicas que inhiben a los núcleos talámicos y reducen su salida hacia la corteza, lo cual explica la hipocinesia
- Ganong WF: Reflex & Voluntary Control of Posture & Movement, in: Review of Medical Physiology, 25th ed. New York, McGraw-Hill Education, 2016.
- Guyton AC, Hall JE: Contributions of the Cerebellum and Basal Ganglia to Overall Motor Control, in: Textbook of Medical Physiology, 13th ed, AC Guyton, JE Hall (eds). Philadelphia, Elsevier Inc., 2016.
- Illert M: Motorisches System: Basalganglien, In: Physiologie, 4th ed; P Deetjen et al (eds). München, Elsevier GmbH, Urban & Fischer, 2005.
- Luhmann HJ: Sensomotorische systeme: Kórperhaltung und Bewegung, in: Physiologie, 6th ed; R Klinke et al (eds). Stuttgart, Georg Thieme Verlag, 2010.
- Oertel WH: Basalganglienerkrankungen, in: Physiologie des Menschen mit Pathophysiologie, 31th ed, RF Schmidt et al (eds). Heidelberg, Springer Medizin Verlag, 2010.
- Wichmann T and DeLong MR: The Basal Ganglia, In: Principles of Neural Science, 5th ed; E Kandel et al (eds). New York, McGraw-Hill, 2013.
