Constantes de Antoine: fórmulas, ecuaciones, ejemplos
Las constantes de Antoine son tres parámetros que aparecen en una relación empírica entre la presión de vapor de saturación y la temperatura para sustancias puras. Dependen de cada sustancia y se suponen constantes en cierto rango de temperaturas.
Fuera de ese rango las constantes de Antoine cambian su valor. Las constantes están relacionadas mediante una ecuación creada en 1888 por el ingeniero francés Louis Charles Antoine (1825–1897).
Índice del artículo
- 1 Fórmulas y ecuaciones
- 2 Vapor de saturación
- 3 ¿Cómo se calculan las constantes de Antoine?
- 4 Ejemplos
- 5 Referencias
La forma más usual de expresar la función de Antoine es:
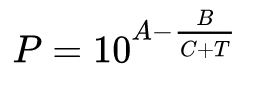
En esta fórmula P representa la presión de vapor de saturación expresada en milímetros de mercurio (mmHg), T es la temperatura que viene siendo la variable independiente y se expresa en ℃.
A, B y C son las constantes o parámetros de la fórmula de Antoine.
La importancia de esta fórmula que a pesar de ser empírica, da una expresión analítica sencilla que puede ser usada con facilidad en los cálculos termodinámicos.
La fórmula de Antoine no es única, hay expresiones más precisas que son extensiones de esta fórmula, pero con la desventaja que tienen seis o más parámetros y su expresión matemática es más compleja, los que las hace poco prácticas de usar en los cálculos termodinámicos.
Como la fórmula de Antoine mide la presión del vapor de saturación, es necesario explicar en qué consiste.
En una ampolla de vidrio u otro recipiente se coloca un líquido. Se extrae todo el aire de la ampolla. El conjunto se coloca en un baño térmico hasta que se alcance el equilibrio.
Al comienzo todo es líquido, pero debido a que hay vacío, las moléculas más rápidas comienzan a abandonar el líquido formando un gas de la misma sustancia del líquido.
El proceso anterior es la evaporación y en la medida que ocurre va aumentando la presión de vapor.
Algunas de las moléculas del vapor pierden energía y se reincorporan a la fase líquida de la sustancia, este es el proceso de condensación.
Entonces ocurren simultáneamente dos procesos, la evaporación y la condensación. Cuando salen igual número de moléculas del líquido a las que se incorporan al mismo se alcanza un equilibrio dinámico y en este momento ocurre la máxima presión de vapor conocida como presión de saturación.
Es esta presión de saturación de vapor la que predice la fórmula de Antoine para cada sustancia y cada temperatura.
En algunos sólidos se presenta un fenómeno semejante cuando se pasa de la fase sólida a la gaseosa directamente sin pasar por la fase líquida, en estos casos también puede medirse una presión de vapor de saturación.
No es fácil establecer un modelo teórico partiendo desde primeros principios ya que están involucrados cambios de energía cinética molecular, que puede ser de tipo traslacional, rotacional y vibracional, con la energía interna de enlace molecular. Es por este motivo que en la práctica se recurre a fórmulas empíricas.
No existe un método teórico para obtener las constantes de Antoine, debido a que se trata de una relación empírica.
Se obtienen a partir de la data experimental de cada sustancia y ajustando los tres parámetros A, B y C, de modo que minimicen la diferencia cuadrática (método de los mínimos cuadrados) de la predicción con los datos experimentales.
Para el usuario final, que generalmente son ingenieros químicos, existen tablas en los manuales de química donde se dan estas constantes para cada sustancia indicando los rangos máximos y mínimos de temperatura en la que son aplicables.
También hay disponibles servicios online que dan los valores de la constantes A, B y C como es el caso de DDBST GmbH Onlines Services.
Para una misma sustancia puede existir más de un rango de temperaturas de validez. Entonces dependiendo del rango de trabajo, se elige uno u otro grupo de constantes.
Las dificultades pueden aparecer si el rango de trabajo de temperaturas está entre dos rangos de validez de las constantes, debido a que las predicciones de presión de la fórmula no coinciden en la zona limítrofe.
Hallar la presión de vapor de agua a 25℃.
Solución
Consultamos las tablas para determinar las constantes de Antoine.
Hay dos rangos para el agua:
Entre 1℃y 100℃ y entre 99℃ hasta 374℃.
Como estamos interesados en 25℃ tomamos el primer rango en el cual el valor de las constantes de Antoine son:
A= 8,07131
B= 1730,63
C= 233,426
P= 10^(8,07131 – 1730,63/(25 + 233,426))
Cálculo del exponente
Calculemos primero el exponente: 1,374499
P= 10^1,374499 = 23,686 mmHg = 0,031166 atm
Interpretación de los resultados
Este resultados se interpretan así:
Supongamos que se coloca agua pura en un recipiente hermético al que se le ha extraído el aire mediante una bomba de vacío.
El recipiente con el agua se coloca en un baño térmico a temperatura de 25℃ hasta que alcance el equilibrio térmico.
El agua en el recipiente hermético se evapora parcialmente hasta alcanzar la presión de vapor de saturación, que no es otra cosa que la presión en la que se establece el equilibrio dinámico entre la fase líquida del agua y la fase de vapor.
Esa presión en este caso resultó ser 0,031166 atm a 25℃.
Hallar la presión de vapor de agua a 100℃.
Consultamos las tablas para determinar las constantes de Antoine. Hay dos rangos para el agua:
Entre 1℃y 100℃ y entre 99℃ hasta 374℃.
En este caso la temperatura de interés está en los dos rangos.
Usamos el primero de los rangos [1℃, 100℃]
A= 8,07131
B= 1730,63
C= 233,426
P= 10^(8,07131 – 1730,63/(100 + 233,426))
Cálculo del exponente
Calculemos primero el exponente: 2.8808
P= 10^1,374499 = 760,09 mmHg = 1,0001 atm
A continuación usamos el segundo de los rangos [99℃, 374℃]
En este caso las constantes son
A= 8,14019
B= 1810.94
C= 244.485
P= 10^(8.14019 – 1810.94/(100 + 244.485))
Calculemos primero el exponente: 2.88324
P=10^2.88324 = 764.2602 mmHg= 1,0056 atm
Hay una diferencia porcentual entre los dos resultados de 0,55%.
- Aplicación de las leyes de Raoult y Dalton y de la ecuación de Antoine. Recuperado de: misapuntesyacimientos.wordpress.com
- Calculadora en línea de la fórmula de Antoine. Recuperado de: ddbonline.ddbst.de/AntoineCalculation/AntoineCalculationCGI.exe
- Gecousb. Termodinámica y tablas de vapor / Constantes de Antoine. Recuperado de: gecousb.com.ve
- Propiedades térmicas de la materia. Recuperado de: webserver.dmt.upm.es
- Yaws and Yang. Tablas de constantes de Antoine para más de 700 compuestos orgánicos. Recuperado de: user.eng.umd.edu
- Wikipedia. Ecuación de Antoine. Recuperado de wikipedia.com
- Wikipedia. Ecuación de Clausius-Clapeyron. Recuperado de wikipedia.com
- Wisniak J. Historical development of the vapor pressure equation from dalton to antoine. Recuperado de: link.springer.com
