Reacción xantoproteica: fundamento, procedimiento, uso
La reacción xantoproteica es un procedimiento químico utilizado para determinar presencia o ausencia de aminoácidos aromáticos, tales como la tirosina y el triptófano, que pueden estar de forma libre o constituyendo proteínas solubles, péptidos o polipéptidos.
También se ha utilizado para detectar sustancias tóxicas a nivel de la sangre que contienen un grupo bencénico en su estructura. Esta prueba también se conoce como reacción xantoproteica de Becher.
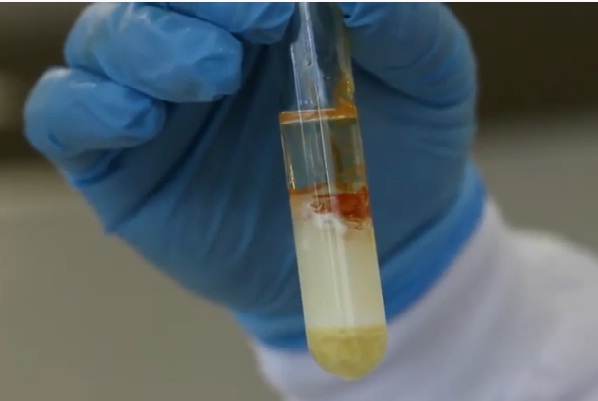
La reacción xantoproteica utiliza ácido nítrico concentrado, calor y un álcali neutralizador. Si al neutralizar la reacción la solución vira de color amarillo a naranja la prueba se considera positiva. La coloración observada es debida a la formación de compuestos nitrogenados derivados de la nitrificación de los grupos bencénicos.
Si se necesita cuantificar la cantidad de proteínas totales, es necesario utilizar otros métodos de determinación de proteínas, tal como el Biuret.
La reacción xantoproteica se utiliza principalmente cuando se están analizando sustancias a las que no se le conoce su composición química. Por lo general esta reacción forma parte de un conjunto de pruebas que ayudarán a determinar la composición química de una sustancia o extracto determinado. Es por ello que, es muy utilizado por los investigadores.
Por otra parte, la reacción xantoproteica de Becher se utiliza para detectar sustancias fenólicas e indólicas en la sangre, siendo posible predecir la aparición de una nefropatía, antes de que se aumenten otros parámetros más tardíos.
Índice del artículo
La reacción básicamente detecta la presencia del grupo bencénico, tanto en aminoácidos, como en proteínas y péptidos. El ácido nítrico actúa sobre el anillo bencénico de los aminoácidos que lo poseen, formando nitrocompuestos fenólicos.
La reacción necesita calor para llevarse a cabo, por lo general se forma un precipitado que enturbia el medio, volviéndolo lechoso. El precipitado puede ser blanco o amarillo. Finalmente, requiere un paso de alcalinización que acentúa el color. Para ello se utiliza una base como hidróxido de sodio al 40% o amoníaco.
La reacción será interpretada como positiva si se observa una coloración amarilla fuerte durante el proceso de calentamiento o naranja oscuro al alcalinizar la reacción. Los aminoácidos que detecta son principalmente tirosina y triptófano.
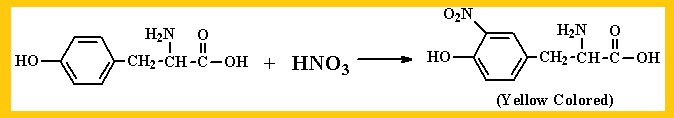
En el caso de la fenilalanina, aunque es un aminoácidos aromático, el núcleo bencénico de este aminoácido es difícil de ser nitratado en una reacción simple, por tanto, emitirá o una reacción negativa o débilmente positiva.
Por lo general la prueba xantoproteica se puede complementar con la prueba de Hopkins-Cole, la cual sirve para identificar específicamente triptófano. Si la prueba xantoproteica es positiva y la de Hopkins-Cole es negativa, se descarta la presencia de triptófano en esa solución, orientando a la presencia principalmente de tirosina. Así mismo, se puede complementar también con la reacción de Millon para la detección de tirosina, entre otras cosas.
Esta reacción también puede ser usada sobre muestras de sangre, plasma o suero desalbuminado para el diagnóstico de uremia o insuficiencia renal. En este caso, lo que se busca es la detección de sustancias tóxicas (fenólicas e indólicas) producidas a partir de la putrefacción intestinal.
Estas sustancias poseen el grupo bencénico y por tanto, dan una reacción xantoproteica positiva, a pesar que la sustancias reaccionante no es ni un aminoácido, ni una proteína.
Colocar 1 ml de la muestra problema en un tubo de ensayo limpio y seco.
-Agregar 0,5 ml de ácido nítrico concentrado.
-Incubar la mezcla en un baño de María a 70 °C por 2 minutos. Previamente preparar el baño de María a la temperatura mencionada.
-Al sacar el tubo del baño de María es posible observar que la solución se ha vuelto lechosa y ha tomado cierta coloración blanca amarillenta.
-Se enfría la solución dejando caer agua fría en la base del tubo.
-Se alcaliniza la preparación agregando lentamente (gota a gota) una solución de hidróxido de sodio a 40% hasta que haya un viraje de color.
-Si la prueba es positiva se formará un anillo color naranja oscuro en la interface de los líquidos.
-Si la reacción es negativa no habrá formación de color.
-Dispensar 5 cc de ácido tricloroacético al 20% sobre 5 cc de sangre venosa, plasma o suero, siendo este último el más indicado. Se mezcla bien y se filtra.
-Se toman 2 cc del filtrado y se mezcla con 0,5 cc de ácido nítrico. Luego se calienta hasta ebullición, para ello se coloca el tubo directamente sobre la llama del mechero por 30 segundos. Se enfría con agua y se agrega 1,5 de cloruro de sodio al 33%.
Se interpreta de la siguiente manera:
-Resultado negativo: color amarillento.
-Resultado positivo (+) amarillo limón.
-(++) amarillo oro.
-(+++) amarillo oscuro a marrón
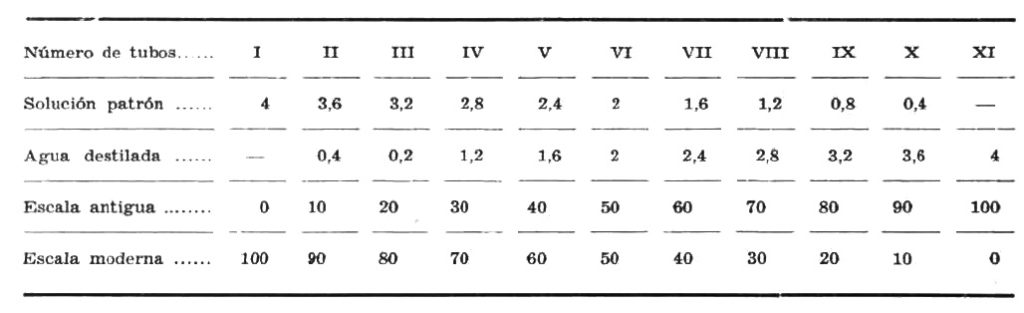
También se puede interpretar utilizando una escala colorimétrica referencial de Autenrieth, constituida por diversas concentraciones de bicromato de potasio. Esta se prepara en diluciones de 10 en 10 a partir de una solución madre de 0,03874%. Cada tubo representa un porcentaje.
Escalas de interpretación
Existen dos escalas de interpretación denominadas antigua y moderna. Los valores normales son:
Tabla antigua: entre 75 a 85%
Tabla moderna: entre 15 a 25%
Si el color del tubo problema se halla en el medio de dos tubos patrones se hace un promedio entre ambas medidas.
La solución patrón de dicromato de potasio se prepara de la siguiente manera: se mide 7.9 ml de dicromato potásico al 10 N y se enrasa hasta 100 ml en un balón aforado. Para las diluciones se sigue tal cual se muestra en la tabla colorimétrica de Autenrieth.
El uso de la reacción xantoproteica forma parte de un set de pruebas bioquímicas que ayudan a conocer la composición química de alguna sustancia desconocidas. Esta prueba aporta al análisis químico la detección de proteínas que contienen grupos bencénicos en su estructura.
Esta reacción es muy utilizada por los investigadores en diversos estudios de sustancias de interés.
En este sentido, Vásquez-Jorge y colaboradores utilizaron esta y otras reacciones para investigar el contenido proteico de fluidos extraídos del Ostión de mangle (Crassostrea rhizophorae).
Así mismo, Rojas y colaboradores (2009), utilizaron una serie de pruebas, entre la que se encuentra la reacción xantoproteica, para analizar glicomacropéptidos en precipitados de lactosueros de ricotta.
Por otra parte, la reacción xantoproteica de Becher fue modificada por Volhard para ser utilizada con otros fines. En este caso, para la detección de sustancias fenólicas e indólicas que pueden elevarse mucho antes (semanas o meses) de que se incrementen los niveles de urea y nitrógeno residual en sangre.
Estos desechos tóxicos se forman a partir de la putrefacción intestinal de los alimentos.
Estas sustancias se acumulan en la sangre cuando no son eliminadas correctamente, por tanto, una prueba xantoproteica positiva puede predecir la pronta instauración de una insuficiencia renal propiamente dicha o un estado de uremia.
Según la intensidad del color se puede determinar que tan avanzada está. En este caso la prueba es cuantitativa.
En personas sanas esta prueba da un leve color amarillo, correspondiente a los niveles normales de triptófano y tirosina que puede haber en la sangre.
Mientras que, en los pacientes renales la reacción xantoproteica da fuertemente positiva debido a la presencia de las siguientes sustancias: fenol, indol, paracresol, oxiácidos aromáticos, entre otros.
Esta prueba debe ser realizada por profesionales capacitados. Se deben considerar todas las normas de bioseguridad, debido a que los reactivos utilizados son ácidos y bases corrosivos.
Si por accidente caen unas gotas de ácido nítrico en la piel o en las uñas estas se tornarán de color amarillo, ya que ambas estructuras contienen proteínas. Además, sobre la piel y mucosas causa quemaduras graves.
Si ocurre un contacto con la piel, el protocolo a seguir debe ser lavar el área inmediatamente con agua y jabón por 20 minutos aproximadamente.
Si salpica hacia los ojos se debe lavar con abundante agua fresca, tratando de mantener los ojos abiertos.
- «Reacción xantoproteica» Wikipedia, La enciclopedia libre. 2 sep 2019, 17:49 UTC. 21 oct 2019, 20:31 wikipedia.org/
- Vásquez-Jorge Y, Guerra-Molina L, Quintana-Tamayo J, Ramírez-Arzuaga J, Fernando-Ballesteros R, Vásquez-Jorge Y. Caracterización fisicoquímica y contenido de proteínas de extractos fluidos del ostión de mangle (Crassostrea rhizophorae). Rev Cubana de Química, 2014; 26 (1): 66-74. Disponible en Redalyc.
- Rojas E, Valbuena E, Torres G, García A, Piñero M, Galindo L. Aislamiento y rendimiento del GMP mediante precipitación de lactosuero con ácido tricloroacético. Cient. (Maracaibo) 2009; 19 (3): 295-302. Disponible en: ve.scielo.
- Vásquez A. Reacción xantoproteica. Revista clínica española. 1949; 35 (5): 326-327. Disponible en: Elsevier
- Gálvez I, Gárate O. Las reacciones de Becher y de Andrewes en cirugía urinaria. Servicio de Urología del Hospital Español. Revista argentina de urología 395-404
