Hidróxido de cobre (II): estructura, propiedades, nomenclatura, usos
El hidróxido de cobre (II) o hidróxido cúprico es un sólido inorgánico cristalino azul pálido o azul verdoso cuya fórmula química es Cu(OH)2. Se obtiene como precipitado voluminoso azul al añadir un hidróxido alcalino a soluciones cúpricas (significa que contienen iones Cu2+). Es un compuesto poco estable.
Para incrementar su estabilidad se prepara en presencia de amoníaco (NH3) o fosfatos.Si se prepara en presencia de amoníaco se produce un material con buena estabilidad y gran tamaño de partícula.

Cuando se prepara partiendo de fosfato de cobre (II), Cu3(PO4)2, se obtiene un material con tamaño de partícula más fino y mayor área superficial. El hidróxido cúprico es ampliamente usado como fungicida y bactericida en agricultura y para tratar la madera, alargando su vida útil.
También se emplea como suplemento alimenticio para animales. Se usa como materia prima para la obtención de otras sales de cobre (II) y en galvanoplastia para recubrir superficies.
Se están realizando estudios para estimar su potencial para combatir infecciones bacterianas y fúngicas en el ser humano.
Índice del artículo
El hidróxido de cobre (II) contiene cadenas infinitas de iones cobre (Cu2+) unidos por puentes de grupos hidroxilo (OH–).
Las cadenas están tan empaquetadas que 2 átomos de oxígeno desde otras cadenas están por encima y por debajo de cada átomo de cobre, adoptando entonces una configuración octaédrica distorsionada, la cual es común en la mayoría de los compuestos de cobre (II).
En su estructura, cuatro átomos de oxígeno están a una distancia de 1,93 A; dos átomos de oxígeno están a 2,63 A; y la distancia Cu-Cu es de 2,95 A.
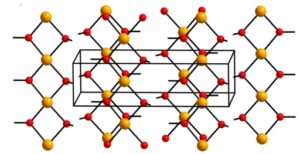
– Hidróxido de cobre (II).
– Hidróxido cúprico.
– Dihidróxido de cobre.
Sólido cristalino.
99,58 g/mol.
Se descompone antes de fundirse. Punto de degradación 229 ºC.
3,37 g/cm3
Es virtualmente insoluble en agua: 2,9 microgramos/L a 25 ºC. Soluble rápidamente en ácidos, en soluciones alcalinas concentradas y en hidróxido de amonio. Insoluble en solventes orgánicos. En agua caliente se descompone generando el óxido de cobre (II), el cual es más estable.
Es fácilmente soluble en ácidos fuertes y también en soluciones concentradas alcalinas de hidróxidos, para dar aniones de color azul profundo, probablemente del tipo [Cun(OH)2n+2]2-.
Su estabilidad depende del método de preparación.
Se puede descomponer dando óxido de cobre (II) negro (CuO) si permanece en reposo unos días o bajo calentamiento.
En presencia de un exceso de álcali se descompone sobre los 50 ºC.
El hidróxido de cobre (II) posee una amplia aplicación como fungicida y antibacteriano en cultivos agrícolas. A continuación algunos ejemplos:
– Sirve contra las manchas bacterianas (de Erwinia) en la lechuga, aplicándose como tratamiento foliar.
– Contra manchas bacterianas (de Xanthomonas pruni) en duraznos, para lo cual se aplica un tratamiento latente y foliar.
– Es empleado contra la plaga de hoja y tallo de los arándanos mediante aplicaciones latentes.
– Contra la putrefacción durante el almacenamiento de los arándanos causada por Monilinia oxycocci, mediante aplicación latente.
Para la aplicación en agricultura se utiliza el hidróxido de cobre (II) que se prepara en presencia de fosfatos debido a su pequeño tamaño de partícula.

La madera, por ser de naturaleza orgánica, es sensible al ataque de insectos y microorganismos. El hidróxido de cobre (II) se utiliza como biocida para los hongos que atacan la madera.
Generalmente se usa junto a un compuesto de amonio cuaternario (NH4+). El hidróxido de cobre actúa como fungicida y el compuesto de amonio cuaternario trabaja como insecticida.
De esta forma, la madera tratada aguanta o resiste las condiciones de servicio, alcanzando el nivel de desempeño requerido por el usuario. Sin embargo, la madera tratada con estos compuestos presenta un alto nivel de cobre y resulta muy corrosiva para el acero común, por lo que se requiere un tipo de acero inoxidable que pueda aguantar el procesamiento de la madera tratada.
A pesar de su utilidad, el hidróxido de cobre (II) es considerado un biocida ligeramente peligroso.
Por esta razón, existe la preocupación de que sea liberado de la madera tratada al ambiente en cantidades que puedan ser dañinas a los microorganismos presentes naturalmente en las aguas (ríos, lagos, humedales y mar) o el suelo.
Desde el siglo XIX se han empleado las soluciones amoniacales de hidróxido de cobre (II) para disolver la celulosa. Este es uno de los primeros pasos para la obtención de la fibra denominada rayón mediante la tecnología desarrollada por Bemberg en Alemania.
El hidróxido de cobre (II) se disuelve en una solución de amoníaco (NH3), formando una sal compleja.
Las fibras cortas refinadas de algodón se añaden a la solución amoniacal de cobre que contiene el hidróxido de cobre (II) en forma de sólido precipitado.
La celulosa del algodón forma un complejo con el hidróxido de cobre tetra-amonio disolviéndose en la solución.
Posteriormente, esta solución se coagula mientras se hace pasar por un dispositivo para extrusión.
Debido a su alto costo, esta tecnología ya ha sido superada por la de viscosa. La tecnología de Bemberg se utiliza actualmente solo en Japón.
Se emplea como trazas en alimentación animal, pues es una de las sustancias requeridas como micronutrientes para la completa nutrición de los animales.

Esto se debe a que en los seres vivos superiores el cobre es un elemento esencial, requerido para la actividad de una variedad de enzimas que contienen cobre.
Por ejemplo, es contenido en la enzima que participa en la producción de colágeno y en la enzima requerida para la síntesis de melanina, entre otras.
Es un compuesto generalmente reconocido como seguro cuando se añade a niveles consistentes con una buena práctica de alimentación.

Activo precursor en la producción de los siguientes compuestos de cobre (II): naftenato de cobre (II), 2-etilhexanoato de cobre (II) y jabones de cobre. En estos casos se emplea el hidróxido de cobre (II) que se sintetiza en presencia de amoníaco.
Se usa en la estabilización del nylon, en electrodos de baterías; como fijador de colores en operaciones de teñido; como pigmento; en insecticidas; en el tratamiento y tinción de papel; en catalizadores, como catalizador en la vulcanización de goma de polisulfuro; como pigmento antiincrustante; y en electrólisis, en galvanoplastia.
El hidróxido de cobre (II) forma parte de los compuestos de cobre que se están estudiando en forma de nanopartículas para la eliminación de bacterias como la E. coli, K. pneumoniae, P. aeruginosa, Salmonella spp., entre otras, causantes de enfermedades en el ser humano.
Se ha encontrado también que las nanopartículas de cobre pueden ser efectivas contra la Candida albicans, un hongo que es causa común de patologías humanas.
Esto indica que la nanotecnología del cobre puede jugar un rol importante contra las bacterias y hongos causantes de infecciones en humanos, y el hidróxido de cobre (II) podría ser muy útil en estos campos.
- Cotton, F. Albert and Wilkinson, Geoffrey. (1980). Advanced Inorganic Chemistry. Fourth Edition. John Wiley & Sons.
- Kirk-Othmer (1994). Encyclopedia of Chemical Technology. Volume 7. Fourth Edition. John Wiley & Sons.
- Ullmann’s Encyclopedia of Industrial Chemistry. (1990). Fifth Edition. Volume A7. VCH Verlagsgesellschaft mbH.
- Bailar, J.C.; Emeléus, H.J.; Sir Ronald Nyholm and Trotman-Dickenson, A.F. (1973). Comprehensive Inorganic Chemistry. Volume 3. Pergamon Press.
- National Library of Medicine. (2019). Copper(II) Hydroxyde. Recuperado de: pubchem.ncbi.nlm.nih.gov
- Schiopu, N. and Tiruta-Barna, L. (2012). Wood preservatives. In Toxicity of building materials. Chapter 6. Recuperado de sciencedirect.com.
- Mordorski, B. and Friedman, A. (2017). Metal Nanoparticles for Microbial Infection. In Functionalized Nanomaterials for the Management of Microbial Infection. Chapter 4. Recuperado de sciencedirect.com.
- Takashi Tsurumi. (1994). Solution spinning. In Advanced fiber spinning technology. Chapter 3. Recuperado de sciencedirect.com.
